名校
1 . 将等物质的量浓度等体积的甘氨酸溶液与盐酸混合,发生反应: ,取上述溶液(含0.04mol
,取上述溶液(含0.04mol  ),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以
),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以 的形式存在)。
的形式存在)。
 ,取上述溶液(含0.04mol
,取上述溶液(含0.04mol  ),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以
),滴加NaOH溶液,pH的变化如下图所示(注:b点溶液中甘氨酸以 的形式存在)。
的形式存在)。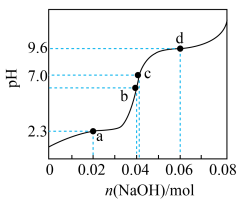
A. 中解离出 中解离出 的能力: 的能力: |
B.b点溶液pH<7,推测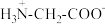 中 中 解离出 解离出 的程度大于-COO-水解的程度 的程度大于-COO-水解的程度 |
C.c点溶液中存在: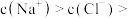 c( c(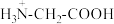 ) )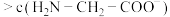 |
D.由d点可知: 的 的 |
您最近一年使用:0次
2024-04-10更新
|
634次组卷
|
5卷引用:2024届宁夏石嘴山市第三中学高三下学期四模理综试题-高中化学
2 . 判断下列选项正确的是
| A.NaHCO3属于碱式盐,其水溶液显碱性 |
| B.NaHSO3属于酸式盐,其水溶液显酸性 |
C.NaHSO4属于正盐,水溶液显酸性的原因是HSO 的电离程度大于HSO 的电离程度大于HSO 的水解程度 的水解程度 |
D.NaHC2O4水溶液显酸性的原因是H2C2O4 的电离程度大于HC2O 的水解程度 的水解程度 |
您最近一年使用:0次
2022-08-25更新
|
77次组卷
|
2卷引用:宁夏石嘴山第三中学2021-2022学年高二下学期期末考试化学试题
名校
3 . 为探究温度对盐类水解的影响,利用手持技术测定0.1mol•L-1Na2CO3溶液温度由20℃升高到60℃过程的pH,130s后的曲线如图所示(已知pKw=pH+pOH)。下列说法正确的是


| A.加热升温时,溶液中的c(OH-)降低 |
B.加热过程中,n(H2CO3)+n(HCO )+n(CO )+n(CO )逐渐增大 )逐渐增大 |
C.常温下,Kh1(CO )为10-4.6 )为10-4.6 |
D.Kw受温度的影响程度大于Kh1(CO ) ) |
您最近一年使用:0次
2022-01-15更新
|
443次组卷
|
4卷引用:宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题
宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题福建省泉州市2021-2022学年高三上学期1月普通高中毕业班质量监测(二)化学试题(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题



