解题方法
1 . 废旧锌锰电池中的黑锰粉含有MnO2、MnO(OH)、NH4Cl和少量ZnCl2、Fe2O3及炭黑等,为了保护环境、充分利用锰资源,通过如下流程制备MnSO4。

回答下列问题:
(1)Mn的原子结构示意图为___________ 。
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因___________ 。
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、___________ 、洗涤、干燥,得NH4Cl固体。

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为___________ 。
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是___________ ,实验II中H2O2的作用是___________ 。
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是___________ 。
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加___________ (填试剂),观察到___________ (填现象)。

回答下列问题:
(1)Mn的原子结构示意图为
(2)“滤液a”的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①用离子方程式表示“滤液a”呈酸性的原因
②根据下图所示的溶解度曲线,将“滤液a”蒸发结晶、

(3)“焙炒”的目的是除炭、氧化MnO(OH)等。空气中O2氧化MnO(OH)的化学方程式为
(4)探究“酸浸”中MnO2溶解的适宜操作。
实验I.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
实验II.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①实验I中MnO2的作用是
②由实验可知,“酸浸”溶解MnO2时加入试剂的顺序是
(5)加入MnO调pH时,证明MnSO4溶液中Fe3+沉淀完全的实验步骤及现象:取少量溶液,滴加
您最近一年使用:0次
解题方法
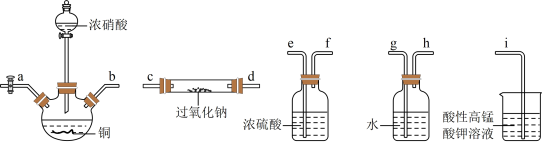
2 . 在生活中亚硝酸钠(NaNO2)应用十分广泛,少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长,还可用于治疗氰化物中毒等。某化学兴趣小组利用下列装置设计制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
已知:①2NO+Na2O2=2NaNO2
②NO能被酸性高锰酸钾氧化为NO ,但不能被浓硫酸氧化。
,但不能被浓硫酸氧化。
回答下列问题:
(1)盛装浓硝酸的仪器名称是___________ ;铜元素位于元素周期表的________ 区。
(2)上述仪器连接顺序为______________ (气流方向从左向右,用小写字母表示)。
(3)若没有盛装浓硫酸的洗气瓶,硬质玻璃管中可能发生的副反应的化学方程式为___________ 。
(4)反应结束后需要打开止水夹a,继续通入一段时间氮气,目的是____________ 。
(5)酸性高锰酸钾溶液中发生反应的离子方程式为__________________ 。
(6)NaNO2溶液呈碱性,原因是_____________ (用离子方程式表示)。
(7)为测定产品的纯度,需配制体积为200mL的一定物质的量浓度的样品溶液,配制过程中,必须使用的玻璃仪器有烧杯、玻璃棒、_____________________ 。

已知:①2NO+Na2O2=2NaNO2
②NO能被酸性高锰酸钾氧化为NO
 ,但不能被浓硫酸氧化。
,但不能被浓硫酸氧化。回答下列问题:
(1)盛装浓硝酸的仪器名称是
(2)上述仪器连接顺序为
(3)若没有盛装浓硫酸的洗气瓶,硬质玻璃管中可能发生的副反应的化学方程式为
(4)反应结束后需要打开止水夹a,继续通入一段时间氮气,目的是
(5)酸性高锰酸钾溶液中发生反应的离子方程式为
(6)NaNO2溶液呈碱性,原因是
(7)为测定产品的纯度,需配制体积为200mL的一定物质的量浓度的样品溶液,配制过程中,必须使用的玻璃仪器有烧杯、玻璃棒、
您最近一年使用:0次



