1 . 一定温度下,硫酸盐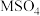 (
(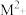 代表
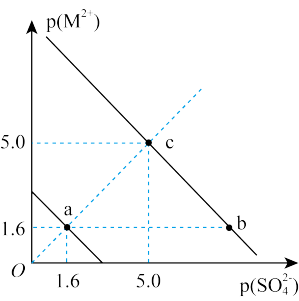
代表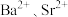 )的沉淀溶解平衡曲线如图所示。已知:
)的沉淀溶解平衡曲线如图所示。已知: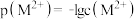 ,
,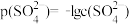 。向10mL 0.01 mol/L
。向10mL 0.01 mol/L 溶液中滴入1滴(约0.05 mL) 0.01 mol/L
溶液中滴入1滴(约0.05 mL) 0.01 mol/L 溶液出现白色浑浊,而滴入1滴(约0.05 mL) 0.01 mol/L
溶液出现白色浑浊,而滴入1滴(约0.05 mL) 0.01 mol/L 溶液无浑浊出现。下列说法中错误的是
溶液无浑浊出现。下列说法中错误的是
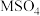 (
(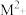 代表
代表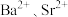 )的沉淀溶解平衡曲线如图所示。已知:
)的沉淀溶解平衡曲线如图所示。已知: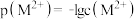 ,
,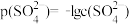 。向10mL 0.01 mol/L
。向10mL 0.01 mol/L 溶液中滴入1滴(约0.05 mL) 0.01 mol/L
溶液中滴入1滴(约0.05 mL) 0.01 mol/L 溶液出现白色浑浊,而滴入1滴(约0.05 mL) 0.01 mol/L
溶液出现白色浑浊,而滴入1滴(约0.05 mL) 0.01 mol/L 溶液无浑浊出现。下列说法中错误的是
溶液无浑浊出现。下列说法中错误的是
A.欲使c点对应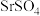 溶液移向a点,可加浓 溶液移向a点,可加浓 溶液 溶液 |
| B.BaSO4和SrSO4两沉淀可以相互转化 |
| C.向等浓度的BaCl2溶液和SrCl2溶液中滴入Na2SO4溶液,先生成溶液SrSO4沉淀 |
D.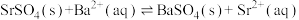 的平衡常数为 的平衡常数为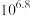 |
您最近一年使用:0次
名校
2 . 工业上常先以 为原料制得
为原料制得 溶液,通过添加过量难溶电解质
溶液,通过添加过量难溶电解质 ,使含有的
,使含有的 、
、 、
、 等金属离子形成硫化物沉淀,经过滤除去包括
等金属离子形成硫化物沉淀,经过滤除去包括 在内的沉淀,再经蒸发,结晶,可得纯净的
在内的沉淀,再经蒸发,结晶,可得纯净的 ,根据上述实验事实,下列分析正确的是
,根据上述实验事实,下列分析正确的是
 为原料制得
为原料制得 溶液,通过添加过量难溶电解质
溶液,通过添加过量难溶电解质 ,使含有的
,使含有的 、
、 、
、 等金属离子形成硫化物沉淀,经过滤除去包括
等金属离子形成硫化物沉淀,经过滤除去包括 在内的沉淀,再经蒸发,结晶,可得纯净的
在内的沉淀,再经蒸发,结晶,可得纯净的 ,根据上述实验事实,下列分析正确的是
,根据上述实验事实,下列分析正确的是A. 的 的 小于 小于 、 、 、 、 等硫化物的 等硫化物的 |
B.除杂试剂 也可用 也可用 代替 代替 |
C. 与 与 反应的离子方程式是 反应的离子方程式是 |
| D.整个过程中涉及的反应类型有复分解反应和氧化还原反应 |
您最近一年使用:0次
2020-09-13更新
|
193次组卷
|
3卷引用:山东省德州市2019-2020学年高二上学期期末考试化学试题
名校
解题方法
3 . 下列解释实验现象的反应方程式不正确的是
| A.切开的金属 Na 暴露在空气中,光亮表面逐渐变暗:4Na+O2=2Na2O |
| B.向 AgCl 悬浊液中滴加 Na2S 溶液,白色沉淀变为黑色:2AgCl(s)+S2–(aq)= Ag2S(s)+2Cl–(aq) |
C.向 Na2CO3 溶液中滴入酚酞,溶液变红: CO +2H2O +2H2O H2CO3+2OH– H2CO3+2OH– |
D.向NaHSO4溶液中逐滴加入 Ba(OH)2 溶液恰好至溶液呈中性: H++SO +Ba2++OH–=BaSO4↓+H2O +Ba2++OH–=BaSO4↓+H2O |
您最近一年使用:0次



