1 . 电解尿素( )是一种低能耗制氢气的方法,工作原理如图:
)是一种低能耗制氢气的方法,工作原理如图:
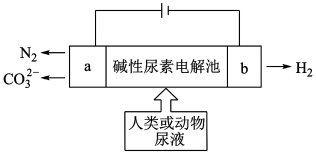
(1)溶液中 的移动方向为
的移动方向为___________ 。
A.a→b B.b→a
(2)写出b电极的电极方程式___________ 。
(3)已知尿素中C元素为+4价,一段时间后在a电极收集到标况下4.48L气体,则整个电路中转移的电子数为___________ 个。
(4)___________ 极的材料可用铁棒,
A.a B.b
且铁棒能够较长时间保持光亮不生锈,该防腐原理称为___________ 。
(5)若将电路中的电源换成导线,此时铁棒会逐渐被腐蚀,写出腐蚀过程中另一电极材料(石墨)上发生的电极方程式:___________ 。
(6)与铵态氮肥相比,写出施用尿素的两个优点:___________ 。
 )是一种低能耗制氢气的方法,工作原理如图:
)是一种低能耗制氢气的方法,工作原理如图:
(1)溶液中
 的移动方向为
的移动方向为A.a→b B.b→a
(2)写出b电极的电极方程式
(3)已知尿素中C元素为+4价,一段时间后在a电极收集到标况下4.48L气体,则整个电路中转移的电子数为
(4)
A.a B.b
且铁棒能够较长时间保持光亮不生锈,该防腐原理称为
(5)若将电路中的电源换成导线,此时铁棒会逐渐被腐蚀,写出腐蚀过程中另一电极材料(石墨)上发生的电极方程式:
(6)与铵态氮肥相比,写出施用尿素的两个优点:
您最近一年使用:0次
名校
2 . 下列实例中,不存在氧化还原反应的是
| A.海水晒盐 | B.炸药爆炸 | C.漂白粉消毒 | D.钢铁生锈 |
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.完成下列问题
(1)理论上不能设计为原电池的化学反应是___________ 。
a.
b.
c.
d.
(2) 电池比能量高,可用于汽车、航天等领域。电池反应式为:
电池比能量高,可用于汽车、航天等领域。电池反应式为: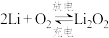 ,放电时,下列说法正确的是
,放电时,下列说法正确的是___________ 。
a.电能转化成化学能 b. 在正极发生氧化反应
在正极发生氧化反应
c.正离子由负极移向正极 d. 在负极失去电子
在负极失去电子
(3)下列关于金属腐蚀与防护的说法不正确的是___________ 。

a.图①,放置于干燥空气中的铁钉不易生锈
b.图②,若断开电源,钢闸门将发生吸氧腐蚀
c.图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
d.图③,若金属 比
比 活泼,可防止输水管腐蚀
活泼,可防止输水管腐蚀
Ⅱ.某实验小组为探究 与
与 能否发生氧化还原反应,设计如下双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下双液原电池(盐桥中为饱和 溶液的琼脂)。
溶液的琼脂)。

(4)该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动。(填“甲”或“乙”)
Ⅲ.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(5)写出氢气所在电极的电极反应式___________ 。
(6)石墨电极为___________ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,___________ (填“铁极”或“石墨极”)区的溶液先变红。
(7)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将___________ (填“增大”“减小”或“不变”)。当甲装置消耗标准状况下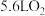 时,丙装置中纯铜电极增重
时,丙装置中纯铜电极增重___________ g。
(1)理论上不能设计为原电池的化学反应是
a.

b.

c.

d.

(2)
 电池比能量高,可用于汽车、航天等领域。电池反应式为:
电池比能量高,可用于汽车、航天等领域。电池反应式为: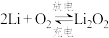 ,放电时,下列说法正确的是
,放电时,下列说法正确的是a.电能转化成化学能 b.
 在正极发生氧化反应
在正极发生氧化反应c.正离子由负极移向正极 d.
 在负极失去电子
在负极失去电子(3)下列关于金属腐蚀与防护的说法不正确的是

a.图①,放置于干燥空气中的铁钉不易生锈
b.图②,若断开电源,钢闸门将发生吸氧腐蚀
c.图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
d.图③,若金属
 比
比 活泼,可防止输水管腐蚀
活泼,可防止输水管腐蚀Ⅱ.某实验小组为探究
 与
与 能否发生氧化还原反应,设计如下双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下双液原电池(盐桥中为饱和 溶液的琼脂)。
溶液的琼脂)。
(4)该装置石墨棒上发生的电极反应式为
 向
向Ⅲ.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(5)写出氢气所在电极的电极反应式
(6)石墨电极为
(7)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
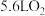 时,丙装置中纯铜电极增重
时,丙装置中纯铜电极增重
您最近一年使用:0次
名校
解题方法
4 . 下列与金属腐蚀有关的说法正确的是
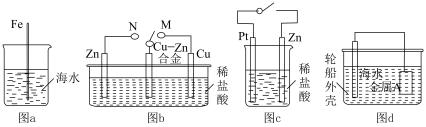

| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Pt上放出气体 |
| D.图d中,钢铁轮船外壳连接一块金属A(铜块)可以减缓船体外壳腐蚀速度 |
您最近一年使用:0次
名校
5 . 某小组按下图所示的装置探究铁的吸氧腐蚀。
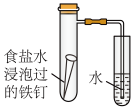
(1)写出正、负极反应的方程式。正极:_______ ,负极:_______ 。
(2)按图装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是_______ 。
a.用纯氧气代替具支试管内的空气
b.用纯铁代替铁钉
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(3)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施_______ (填“可行”或“不行”),原因是_______ 。

(1)写出正、负极反应的方程式。正极:
(2)按图装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是
a.用纯氧气代替具支试管内的空气
b.用纯铁代替铁钉
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(3)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施
您最近一年使用:0次
名校
6 . 电化学知识在工业生产、科技研究中应用广泛。可采用电化学防护技术减缓海水中钢铁设施的腐蚀,下图是钢铁桥墩部分防护原理示意图,请根据图示信息完成(1)(2)小题。
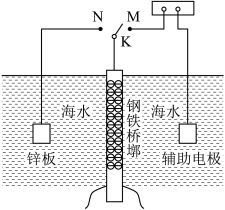
(1)K与M连接时钢铁桥墩的电化学防护方法为______ ,简述这种保护方法的原理:______ 。
(2)K与N连接时的电化学保护法称为______ ,钢铁桥墩为______ 极(填“正”、“负”、“阴”或“阳”)

(1)K与M连接时钢铁桥墩的电化学防护方法为
(2)K与N连接时的电化学保护法称为
您最近一年使用:0次
名校
7 . 研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。完成下列填空:
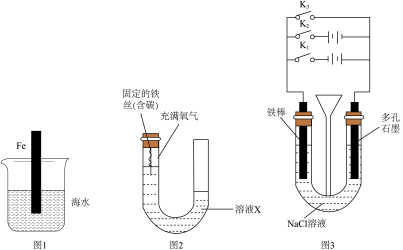
(1)①已知:海水的pH约为8.1,图1的腐蚀过程属于______ (选填“吸氧腐蚀”或“析氢腐蚀”。)图1插入海水中的铁棒(含碳量为10.8%)越靠近烧杯底部,发生电化学腐蚀就越______ (选填“轻微”、“严重”)。
②该实验说明______ 因素会影响铁的腐蚀速率。写出腐蚀时负极的电极反应式______ 。
(2)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化情况。该组实验的目的:研究电解质种类、酸碱性等因素会对铁的腐蚀过程产生影响。(已知:起始时两管内液面相平)选填(“A”“B”“C”)
A.左高右低B.左低右高C.相平
(3)用图3所示装置研究铁的防腐蚀过程:(填“K1”、“K2”或“K3”,下同);
①K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合______ 。
②为减缓铁的腐蚀,应只闭合______ ,该防护法称为______ 。
③只闭合K3,石墨电极附近的pH将______ (填“变大”、“变小”或“不变”)。

(1)①已知:海水的pH约为8.1,图1的腐蚀过程属于
②该实验说明
(2)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化情况。该组实验的目的:研究电解质种类、酸碱性等因素会对铁的腐蚀过程产生影响。(已知:起始时两管内液面相平)选填(“A”“B”“C”)
A.左高右低B.左低右高C.相平
| 溶液X | 浓硫酸 | 浓盐酸 | 极稀硫酸 |
| 液面情况 |
(3)用图3所示装置研究铁的防腐蚀过程:(填“K1”、“K2”或“K3”,下同);
①K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合
②为减缓铁的腐蚀,应只闭合
③只闭合K3,石墨电极附近的pH将
您最近一年使用:0次
名校
解题方法
8 . 用如图装置可以模拟铁的电化学防护,下列说法不正确的是


| A.若X为碳棒,开关K置于A处时,铁电极反应2H2O+2e-=H2+2OH- |
| B.若X为碳棒,开关K置于A处可以减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| D.若X为锌棒,开关K置于B处时,铁电极反应为2H++2e-=H2 |
您最近一年使用:0次
名校
解题方法
9 . 《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。

(1)查阅资料得知铜锈为 Cu2(OH)2CO3, 俗称铜绿,可溶于酸。请写出铜绿与盐酸反应的化学方程式___________
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)2Cl。考古学家将铜锈分为无害锈和有密锈,结构如图所示:
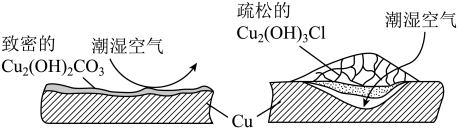
①Cu2(OH)2CO3可否作无害锈,请解释原因。___________
②如图为青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu2(OH) Cl的原理示意图:
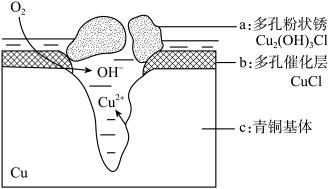
(3)若生成2.145 g Cu2(OH)3Cl (式量:214.5),计算理论上消耗标准状况氧气体积___________ L。
(4)文献显示有害锈的形成过程中会产生 CuCl(白色不溶于水的固体):
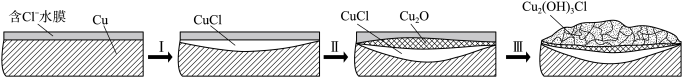
写出过程Ⅰ中负极的电极反应式___________ 。
(5)BTA保护法是青铜器的修复最常用的方法之一,原理如图所示:
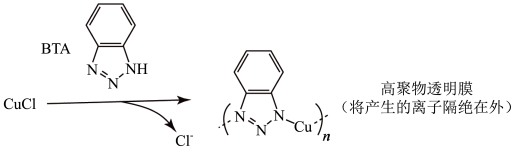
请分析BTA保护法可能的优点(请写出2点)___________ 。
(6)金属腐蚀会造成很严重的事故和损失。2020 年广东省虎门大桥出现桥面抖动现象,专家对桥墩的主体钢筋进行了全面检测,并确定了其安全性。以下说法正确的是___________

(1)查阅资料得知铜锈为 Cu2(OH)2CO3, 俗称铜绿,可溶于酸。请写出铜绿与盐酸反应的化学方程式
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)2Cl。考古学家将铜锈分为无害锈和有密锈,结构如图所示:

①Cu2(OH)2CO3可否作无害锈,请解释原因。
②如图为青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu2(OH) Cl的原理示意图:

(3)若生成2.145 g Cu2(OH)3Cl (式量:214.5),计算理论上消耗标准状况氧气体积
(4)文献显示有害锈的形成过程中会产生 CuCl(白色不溶于水的固体):

写出过程Ⅰ中负极的电极反应式
(5)BTA保护法是青铜器的修复最常用的方法之一,原理如图所示:

请分析BTA保护法可能的优点(请写出2点)
(6)金属腐蚀会造成很严重的事故和损失。2020 年广东省虎门大桥出现桥面抖动现象,专家对桥墩的主体钢筋进行了全面检测,并确定了其安全性。以下说法正确的是___________
| A.桥墩钢筋容易发生化学腐蚀 |
| B.在海面与空气交界处的钢铁,比海水中的钢铁更容易被腐蚀 |
| C.可以在桥墩钢铁上嵌附铜片,减慢其腐蚀速率 |
| D.将桥墩钢铁与外接电源负极相连的方法,称为牺牲阳极的阴极保护法 |
您最近一年使用:0次
名校
10 . 文物是人类宝贵的历史文化遗产,但保存完好的铁器比肯钢器少得多,研究铁质文物的保护意义重大。

已知:i.铁质文物在潮湿的土壤中主要发生吸氧腐蚀,表面生成疏松的FeOOH;
ii.铁质文物在干燥的土壤中表面会生成致密的Fe2O3,过程如下:

(1)写出 i 中铁器腐蚀生成FeOOH的总反应化学方程式:___________
(2)若ii中每一步反应转化的铁元素质量相等,则三步反应中电子转移数之比为___________
【资料1】 Cl⁻体积小、穿透能力强,可将氧化膜转化成易溶解的氯化物而促进铁质文物继续锈蚀。
【资料2】Cl⁻、Br⁻、I⁻促进铁器皿继续锈蚀的能力逐渐减弱。
(3)结合元素周期律解释“资料2”的原因是___________
(4)从潮湿土壤出土或海底打捞的铁质文物必须进行脱氯处理:用稀 NaOH 溶液反复浸泡使Cl⁻渗出后,取最后一次浸泡液加入试剂___________ ,填化学式)溶液检验脱氯处理是否达标。
(5)经脱氯、干燥处理后的铁质文物再“覆盖”一层透明的高分子膜可以有效防止其在空气中锈蚀。下图为其中一种高分子膜的片段:

该高分子的单体是:___________ 。

已知:i.铁质文物在潮湿的土壤中主要发生吸氧腐蚀,表面生成疏松的FeOOH;
ii.铁质文物在干燥的土壤中表面会生成致密的Fe2O3,过程如下:

(1)写出 i 中铁器腐蚀生成FeOOH的总反应化学方程式:
(2)若ii中每一步反应转化的铁元素质量相等,则三步反应中电子转移数之比为
【资料1】 Cl⁻体积小、穿透能力强,可将氧化膜转化成易溶解的氯化物而促进铁质文物继续锈蚀。
【资料2】Cl⁻、Br⁻、I⁻促进铁器皿继续锈蚀的能力逐渐减弱。
(3)结合元素周期律解释“资料2”的原因是
(4)从潮湿土壤出土或海底打捞的铁质文物必须进行脱氯处理:用稀 NaOH 溶液反复浸泡使Cl⁻渗出后,取最后一次浸泡液加入试剂
(5)经脱氯、干燥处理后的铁质文物再“覆盖”一层透明的高分子膜可以有效防止其在空气中锈蚀。下图为其中一种高分子膜的片段:

该高分子的单体是:
您最近一年使用:0次



