2023高三·全国·专题练习
名校
解题方法
1 . 将 溶液滴在一块光亮清洁的铁板表面上,一段时间后,发现液滴覆盖的圆周中心区(a)已被腐蚀变暗,在液滴外沿出现棕色铁锈环(b),如图所示。下列说法不正确的是
溶液滴在一块光亮清洁的铁板表面上,一段时间后,发现液滴覆盖的圆周中心区(a)已被腐蚀变暗,在液滴外沿出现棕色铁锈环(b),如图所示。下列说法不正确的是
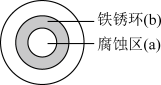
 溶液滴在一块光亮清洁的铁板表面上,一段时间后,发现液滴覆盖的圆周中心区(a)已被腐蚀变暗,在液滴外沿出现棕色铁锈环(b),如图所示。下列说法不正确的是
溶液滴在一块光亮清洁的铁板表面上,一段时间后,发现液滴覆盖的圆周中心区(a)已被腐蚀变暗,在液滴外沿出现棕色铁锈环(b),如图所示。下列说法不正确的是
A.铁锈环的主要成分是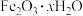 ,铁片腐蚀过程发生的总反应为 ,铁片腐蚀过程发生的总反应为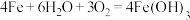 |
B.液滴之下氧气含量少,铁片作负极,发生的还原反应为 |
C.液滴边缘是正极区,发生的电极反应为 |
| D.铁片腐蚀最严重的区域不是生锈最多的区域 |
您最近一年使用:0次
2023-02-17更新
|
336次组卷
|
4卷引用:福建省福州市延安中学2023-2024学年高二上学期期中考试化学试题
福建省福州市延安中学2023-2024学年高二上学期期中考试化学试题(已下线)题型106 金属的腐蚀与防护(已下线)化学反应与电能——进阶学习【精品卷】4.3.1 金属的腐蚀-人教版2023-2024学年选择性必修1
名校
解题方法
2 . 关于下列各装置图的叙述错误的是
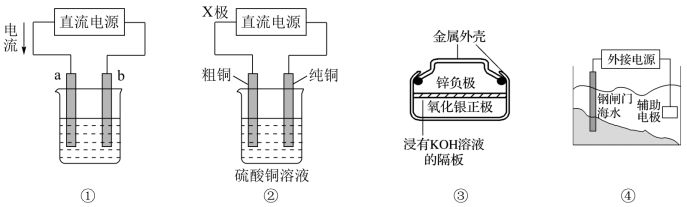
| A.图①装置用于实现铁上镀铜,a极为铜,b极为铁 |
| B.图②装置中的X极若为负极,则该装置可实现粗铜的精炼 |
C.图③装置中正极的电极反应式为: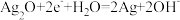 |
| D.图④装置中钢闸门应与外接电源的负极相连以实现外加电流的保护 |
您最近一年使用:0次
2021-07-09更新
|
1073次组卷
|
10卷引用:福建省连城县第一中学2022-2023学年高二上学期月考(一)化学试题
福建省连城县第一中学2022-2023学年高二上学期月考(一)化学试题四川省南充市2020-2021学年高二下学期期末考试化学试题(已下线)1.3.2 金属的电化学防护-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第4章 化学反应与电能(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)甘肃省永昌县第一高级中学2021-2022学年高二上学期期中考试化学(理)试题宁夏永宁县永宁中学2021-2022学年高二上学期期末考试化学试题内蒙古包头市第四中学2021-2022学年高二上学期期中考试化学试题河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题陕西省西安市蓝田县乡镇学校联考2023-2024学年高二上学期1月期末化学试题
3 . 港珠澳大桥的设计使用寿命高达120年,主要的防腐方法有:①钢梁上安装铝片;②使用高性能富锌(富含锌粉)底漆;③使用高附着性防腐涂料;④预留钢铁腐蚀量。下列分析不合理的是
| A.钢铁发生吸氧腐蚀时的负极反应式为:Fe-3e-=Fe3+ |
| B.防腐过程中铝和锌均作为牺牲阳极,失去电子 |
| C.防腐涂料可以防水、隔离O2,降低吸氧腐蚀速率 |
| D.方法①②③只能减缓钢铁腐蚀,未能完全消除 |
您最近一年使用:0次
2021-01-20更新
|
789次组卷
|
15卷引用:福建省福州第三中学2019-2020学年高二上学期期末考试化学试题
福建省福州第三中学2019-2020学年高二上学期期末考试化学试题福建省龙海市第二中学2020-2021学年高二上学期期中考试化学试题北京市朝阳区2019~2020学年高三上学期期中考试化学试题河南省商丘市虞城高中2020届高三11月月考化学试题江西省上饶市上饶中学2019-2020学年高二上学期第二次月考化学(理科培优班)试题宁夏育才中学2019-2020学年高二上学期期末考试化学试题辽宁省五校2021届高三上学期期末联考化学试题辽宁省实验中学2021届高三上学期期末考试化学试题甘肃省庆阳市第六中学2020-2021学年高二上学期期末考试化学试题山西省太原市2020-2021学年高二上学期期末化学(理)试题江西省宜春市奉新县冶城职业学校(奉新县第三中学)2020-2021学年高三上学期期末考试化学(普高)试题(已下线)【教材实验热点】17 金属的腐蚀与防护云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题(已下线)云南省昆明市官渡区第二中学2023-2024学年高二上学期开学考试化学试题云南省昆明市官渡区第二中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
4 . 点蚀又称为孔蚀,是一种集中于金属表面很小的范围并深入到金属内部的腐蚀形态。某铁合金钝化膜破损后的孔蚀如图,下列说法错误的是
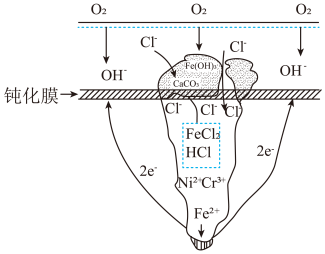

| A.孔隙中有可能发生析氢腐蚀 |
B.孔蚀中 水解导致电解质溶液酸性增强 水解导致电解质溶液酸性增强 |
| C.为防止孔蚀发生可以将外接电源负极与金属相连 |
D.蚀孔外每吸收2.24L  ,可氧化0.2mol Fe ,可氧化0.2mol Fe |
您最近一年使用:0次
2023-03-07更新
|
340次组卷
|
7卷引用:福建省龙岩市第一中学2022届高考考前模拟化学试题
福建省龙岩市第一中学2022届高考考前模拟化学试题福建省永春第一中学2023届高三下学期期初考试化学试题重庆市西南大学附属中学校2021- 2022学年高三下学期第六次月考化学试题(已下线)2022年辽宁省高考真题变式题(1-10)(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(1-10)辽宁省鞍山市普通高中2023届高三下学期第一次模拟联考化学试题(已下线)2022年辽宁高考真题化学试题变式题(选择题6-10)
真题
名校
5 . 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是()


| A.液滴中的Cl–由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH−形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-=Cu2+ |
您最近一年使用:0次
2019-01-30更新
|
1742次组卷
|
34卷引用:福建省永安市第三中学2020-2021学年高二10月月考化学(选考班)试题
福建省永安市第三中学2020-2021学年高二10月月考化学(选考班)试题2011年普通高等学校招生全国统一考试化学卷(浙江)(已下线)2011-2012学年浙江东阳中学、兰溪一中高二下学期期中考试化学卷(已下线)2011-2012学年吉林省扶余一中高一下学期期中考试化学试卷(已下线)2011-2012学年河南省信阳高中高一下学期期中考试化学试卷(已下线)2013届山西省山大附中高三1月月考化学试卷(已下线)2012-2013学年湖北省黄冈中学高二上学期期中考试化学试卷(已下线)2012届北京市清华附中高三考前适应性训练理综化学试卷2015-2016学年浙江省温州市瑞安市龙翔中学高二上第三次月考化学卷2015-2016学年北大附中河南分校高一下3月月考化学试卷浙江省温州中学2016-2017学年高一下学期期中考试化学试题河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题宁夏育才中学学益校区2017-2018学年高二12月月考化学试题山东省新汶中学2017-2018学年高二上学期第一次月考化学试题河南省郑州市第二中学2018-2019学年高二上学期第一次月考化学试题高二人教版选修4 第四章 第四节 金属的电化学腐蚀与防护(已下线)2018年12月15日 《每日一题》人教选修4-周末培优河南省鹤壁市高级中学2018-2019学年高一下学期第二次段考化学试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题16 金属的腐蚀与防护(已下线)上海市卢湾区2012届高三上学期期末考试化学试题甘肃省兰州市第一中学2019-2020学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第4节 金属的腐蚀与防护人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第三节 金属的腐蚀与防护 教材帮上海市上海中学2021届高三上学期期中考试化学试题河南省郑州励德双语学校2020-2021学年高二上学期期中考试化学试题(已下线)课时34 金属的腐蚀与防护-2022年高考化学一轮复习小题多维练(全国通用)新疆柯坪县柯坪湖州国庆中学2021-2022学年高三上学期第一次月考化学试题(已下线)专题08 电化学之电解池-【微专题·大素养】备战2022年高考化学讲透提分要点河南省信阳高级中学2021-2022学年高二下学期4月月考化学试题四川省遂宁市第二中学校2021-2022学年高二下学期半期考试化学试题内蒙古包头市2022-2023学年高二上学期期末考试化学试题山西大学附属中学校2022-2023学年高二上学期12月月考化学试题重庆市南开中学2023-2024学年高二上学期期末考试化学试题
6 . 化学与生活密切相关,下列有关说法错误的是
| A.新能源汽车的推广与使用,有助于减少光化学烟雾的产生 |
| B.服用铬含量超标的药用胶囊会对人体健康造成危害 |
| C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈 |
| D.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化 |
您最近一年使用:0次
2022-06-03更新
|
305次组卷
|
2卷引用:福建省福州第一中学2022届高三下学期模拟考试化学试题
名校
解题方法
7 . 2018年7月至9月,国家文物局在辽宁开展水下考古,搜寻、发现并确认了甲午海战北洋水师沉舰——经远舰。已知:正常海水呈弱碱性。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为_______ 。
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船进行了处理。

①下列说法不正确的是________ 。
A.锌块发生氧化反应:Zn-2e-=Zn2+
B.舰体有电子流入,可以有效减缓腐蚀
C.若通过外加电源保护舰体,应将舰体与电源正极相连
D.地下钢铁管道用导线连接锌块与该种舰体保护法原理相同
②采用“牺牲阳极的阴极保护法”后,舰体上正极的电极反应式为_________ 。
(3)船上有些器皿是铜制品,表面有铜锈。
①据了解铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。

下列说法正确的是________
A.疏松的Cu2(OH)3Cl属于有害锈
B.Cu2(OH)2CO3既能溶于盐酸也能溶于氢氧化钠溶液
C.青铜器表面涂一层食盐水可以做保护层
D.用HNO3溶液除锈可以保护青铜器的艺术价值,做到“修旧如旧”
②文献显示Cu2(OH)3Cl的形成过程中会产生CuCl(白色不溶于水的固体),将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,可以使CuCl转化为难溶的Cu2(OH)2CO3反应的离子方程式为______ 。
(4)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施保护文物。从电化学原理的角度分析“脱盐、干燥”的防腐原理:________ 。
(1)经远舰在海底“沉睡”124年后,钢铁制成的舰体腐蚀严重。舰体发生电化学腐蚀时,负极的电极反应式为
(2)为了保护文物,考古队员采用“牺牲阳极的阴极保护法”对舰船进行了处理。

①下列说法不正确的是
A.锌块发生氧化反应:Zn-2e-=Zn2+
B.舰体有电子流入,可以有效减缓腐蚀
C.若通过外加电源保护舰体,应将舰体与电源正极相连
D.地下钢铁管道用导线连接锌块与该种舰体保护法原理相同
②采用“牺牲阳极的阴极保护法”后,舰体上正极的电极反应式为
(3)船上有些器皿是铜制品,表面有铜锈。
①据了解铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。

下列说法正确的是
A.疏松的Cu2(OH)3Cl属于有害锈
B.Cu2(OH)2CO3既能溶于盐酸也能溶于氢氧化钠溶液
C.青铜器表面涂一层食盐水可以做保护层
D.用HNO3溶液除锈可以保护青铜器的艺术价值,做到“修旧如旧”
②文献显示Cu2(OH)3Cl的形成过程中会产生CuCl(白色不溶于水的固体),将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,可以使CuCl转化为难溶的Cu2(OH)2CO3反应的离子方程式为
(4)考古队员将舰船上的部分文物打捞出水后,采取脱盐、干燥等措施保护文物。从电化学原理的角度分析“脱盐、干燥”的防腐原理:
您最近一年使用:0次
2020-08-20更新
|
1057次组卷
|
11卷引用:福建省安溪一中、养正中学、惠安一中、泉州实验中学2022-2023学年高二上学期期中考联考化学试题
福建省安溪一中、养正中学、惠安一中、泉州实验中学2022-2023学年高二上学期期中考联考化学试题福建省泉州市 2022-2023学年高二上学期期中联考化学试题安徽省宣城市2019-2020学年高二上学期期末考试化学试题(已下线)第01章 化学反应与能量转化(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)(已下线)练习10 金属的腐蚀与防护-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)河北省保定市2020-2021学年高二上学期期末考试化学试题(已下线)1.3.2 金属的电化学防护-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第28讲 金属的腐蚀与防护(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)四川省成都市第七中学2022-2023学年高二下学期3月月考化学试题第四章 章末训练
名校
解题方法
8 . 电化学在科技、生产、社会和生活的各个发面都发挥着重要的作用。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母)。这种防止金属材料腐蚀的方法叫做_______。
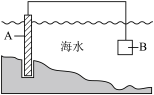
a.金块 b.锌板 c.铜板 d.钠块
氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)
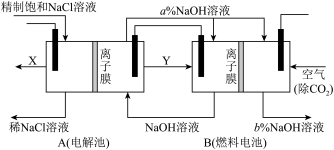
(2)写出A装置中发生反应的离子反应方程式:_______,分析比较图示中a%与b%的大小:a%_______b%(填“>”“<”或“=”)。
(3)写出燃料电池B中的负极的电极反应:_______。
通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:
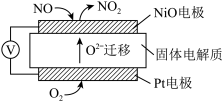
(4)NiO电极上发生的是反应_______(填“氧化”或“还原”)。Pt电极上的电极反应式为_______。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母)。这种防止金属材料腐蚀的方法叫做_______。

a.金块 b.锌板 c.铜板 d.钠块
氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)

(2)写出A装置中发生反应的离子反应方程式:_______,分析比较图示中a%与b%的大小:a%_______b%(填“>”“<”或“=”)。
(3)写出燃料电池B中的负极的电极反应:_______。
通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:

(4)NiO电极上发生的是反应_______(填“氧化”或“还原”)。Pt电极上的电极反应式为_______。
您最近一年使用:0次
2022-10-11更新
|
301次组卷
|
2卷引用:福建省泉州第一中学2022-2023学年高二上学期期中考试化学试题
9 . 关于下列各装置图的叙述不正确 的是
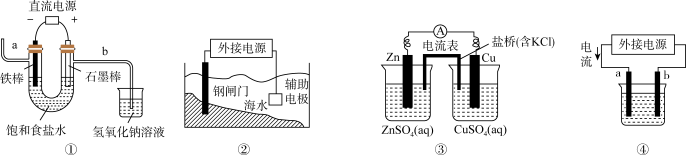

| A.图①装置中a导管释放出的气体具有可燃性 |
| B.图②装置中钢闸门应与外接电源的负极相连,称之为“牺牲阳极的阴极保护法” |
| C.图③装置盐桥中KCl的K+向右侧烧杯移动 |
| D.用图④装置精炼铜,b极为精铜,电解质溶液为CuSO4溶液 |
您最近一年使用:0次
2022-04-04更新
|
558次组卷
|
5卷引用:福建省福州第一中学2021-2022学年高二上学期期末考试化学试题
10 . 关于下列各装置图的叙述错误的是
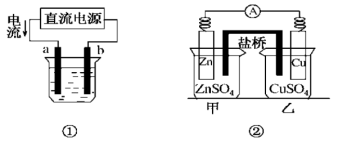
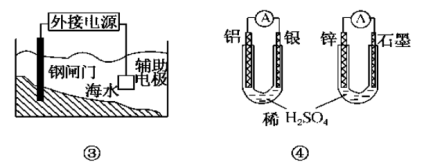


| A.用图①装置精炼铜,b极为精铜,电解质溶液为CuSO4 溶液 |
| B.图②装置盐桥中KCl的K+ 移向乙烧杯 |
| C.图③装置中钢闸门应与外接电源的负极相连,称之为“牺牲阳极的阴极保护法” |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 |
您最近一年使用:0次
2021-07-30更新
|
654次组卷
|
9卷引用:福建省泉州科技中学2021-2022学年高二上学期第一次月考化学试题
福建省泉州科技中学2021-2022学年高二上学期第一次月考化学试题四川省巴中市2021届高考“零诊”理科综合试题理综化学试题(已下线)1.3.2 金属的电化学防护-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)江苏省连云港市赣榆智贤中学2021-2022学年高二上学期第一次月考化学试题(已下线)4.3.1 金属的腐蚀(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)西藏林芝市第一中学2020-2021学年高三上学期第四次月考化学试题(已下线)2020年江苏卷化学高考真题变式题11-15(已下线)专题20 电解池 金属的电化学腐蚀与防护(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)不定项选择题



