名校
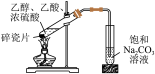
1 . 下列实验装置合理且能达到实验目的的是
|
|
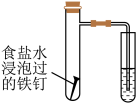
| A.制取乙酸乙酯 | B.验证铁的吸氧腐蚀 |
|
|
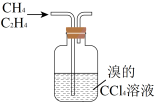
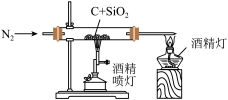
| C.除去甲烷中的乙烯气体 | D.比较碳、硅两元素非金属性的强弱 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列说法正确的是
| A.二氧化硅是一种半导体材料,应用于电子工业 |
| B.聚氯乙烯是一种重要的塑料,常用作食品保鲜膜 |
| C.马口铁(镀锡铁皮)镀层破坏后,镀层仍能起保护作用 |
| D.二氧化硫是一种抗氧化剂,可用作食品添加剂 |
您最近半年使用:0次
名校
解题方法
3 . 化学与人类生产、生活密切相关,下列说法中正确的是
| A.镀锌的铁板其镀层破损后,铁的腐蚀会比纯铁的腐蚀快 |
| B.牙膏中添加氟化物用于预防龋齿是利用了氧化还原反应的原理 |
| C.燃料电池的反应物不是储存在电池内部,而是由外部供给,两电极材料可以相同 |
| D.工业废水处理过程中,常以Na2S作沉淀剂除去废水中的Cu2+、Hg2+、Fe3+等 |
您最近半年使用:0次
4 . 钢铁是用量最大的合金,防止钢铁腐蚀有利用于节约资源。下列防止钢铁腐蚀的方法不正确 的是
| A.水里的铁闸与直流电源的正极相连 | B.家用铁锅用完及时将水擦干 |
| C.铁质栏杆外面涂刷一层油漆 | D.轮船表面焊接锌块 |
您最近半年使用:0次
名校
解题方法
5 . 由下列实验操作及现象能得出相应结论的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 常温下,用pH计测得0.1 mol/L弱酸盐NaA、NaB、NaC溶液pH值分别为a、b、c | 若c>b>a | 水解程度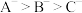 |
| B | 向BaCl2溶液中通入SO2和气体X | 产生白色沉淀 | 气体X一定为氧化剂 |
| C | 将稀硫酸酸化的H2O2加入 溶液中 溶液中 | 溶液出现黄色 | 说明H2O2的氧化性比Fe3+强 |
| D | 一块除去铁锈的铁片上滴一滴铁氰化钾溶液,静置2~3 min | 生成蓝色沉淀 | 铁片上可能发生了电化学腐蚀 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 下列说法错误的是
| A.手机上用的锂离子电池属于二次电池 |
B.工业上常用 溶液除锈,是利用了 溶液除锈,是利用了 水解使溶液显酸性 水解使溶液显酸性 |
C.工业电解精炼铜时,粗铜作阳极,纯铜作阴极, 溶液作电解质溶液,相同时间段内阴极和阳极的质量变化不相等 溶液作电解质溶液,相同时间段内阴极和阳极的质量变化不相等 |
| D.为减缓海水中钢闸门的腐蚀,常将钢闸门与直流电源的负极相连,该方法为牺牲阳极法 |
您最近半年使用:0次
名校
解题方法
7 . 化学与生活关系密切,下列说法正确的是
| A.合成氨工业采用金属镍催化,这样做是为了提高单位时间的转化率 |
| B.钢管表面镀锌可以防止钢管被腐蚀,镀层破损后,钢管反而会加速腐蚀 |
| C.打印机黑色的墨粉中含有铁的氧化物,这种氧化物是氧化铁 |
D.水垢中的 ,可先用 ,可先用 溶液处理,而后用酸除去 溶液处理,而后用酸除去 |
您最近半年使用:0次
2023-11-27更新
|
172次组卷
|
2卷引用:浙江省宁波市鄞州中学2023-2024学年高二上学期期中考试化学试卷
名校
8 . 下列装置或操作不能达到目的的是
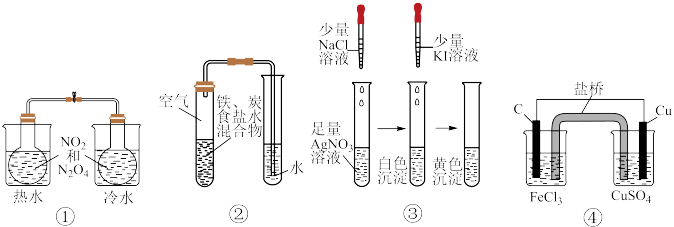

A.操作①观察颜色:浸泡在热水中的烧瓶内红棕色加深,冷水中烧瓶内红棕色变浅,判断反应2NO2(g,红棕色) N2O4(g,无色)的ΔH<0 N2O4(g,无色)的ΔH<0 |
| B.操作②观察右侧导管中出现水柱,判断铁发生吸氧腐蚀 |
| C.操作③判断Ksp(AgCl)>Ksp(AgI) |
| D.装置④实现反应Cu+2Fe3+=Cu2++2Fe2+的化学能转变为电能 |
您最近半年使用:0次
2023-11-12更新
|
202次组卷
|
2卷引用:浙江省浙南名校联盟2023-2024学年高二上学期11月期中考试化学试题
9 . 下列措施或事实能用勒夏特列原理解释的是
| A.在合成氨(正反应放热)的反应中,升温有利于氨的合成 |
B. 、 、 、 、 三者的平衡混合气加压(缩小体积)后颜色变深 三者的平衡混合气加压(缩小体积)后颜色变深 |
| C.钢铁在潮湿的空气中更容易生锈 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
您最近半年使用:0次
10 . 下列说法正确的是
| A.在铁上镀铜时,金属铜作阴极 |
| B.工业上常用电解熔融的氧化镁冶炼金属镁 |
| C.牺牲阳极法通常是在被保护的钢铁设备上安装若干镁合金或锌块 |
D.用石墨电极电解 的 的 溶液,当阳极产生标准状况下 溶液,当阳极产生标准状况下 气体时,停止电解,向剩余溶液中加入适量 气体时,停止电解,向剩余溶液中加入适量 可使电解质溶液恢复至原状态 可使电解质溶液恢复至原状态 |
您最近半年使用:0次