13-14高二·全国·单元测试
名校
解题方法
1 . (1)装置如图,打开K2,闭合K1。A极可观察到的现象是___ ;B极的电极反应为___ ,打开K1,闭合K2,A极可观察到的现象是_____ ;B极的电极反应为______ 。

(2)将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应为_____ ,电解反应的离子方程式为_____ , 实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积_____ L。


(2)将较纯净的CuSO4溶液放入如图所示的装置中进行电解,石墨电极上的电极反应为

您最近一年使用:0次
2020-10-22更新
|
71次组卷
|
7卷引用:陕西省渭南市临渭区尚德中学2020-2021学年高二上学期第一次月考化学试题
2 . 一种高性能的碱性硼化钒(VB2)—空气电池如下图所示,其中在VB2电极发生反应: 该电池工作时,下列说法错误的是
该电池工作时,下列说法错误的是
 该电池工作时,下列说法错误的是
该电池工作时,下列说法错误的是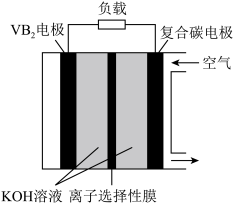
| A.负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应 |
| B.正极区溶液的pH降低、负极区溶液的pH升高 |
C.电池总反应为 |
| D.电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极 |
您最近一年使用:0次
2020-07-09更新
|
21074次组卷
|
77卷引用:陕西省咸林中学2021-2022学年高二上学期第一次月考化学试题
陕西省咸林中学2021-2022学年高二上学期第一次月考化学试题2020年全国统一考试化学试题(新课标Ⅲ)(已下线)专题08 电化学及其应用-2020年高考真题和模拟题化学分项汇编(已下线)专题讲座(六)新型电源及电极反应式的书写(精讲)——2021年高考化学一轮复习讲练测(已下线)第20讲 原电池 化学电源(精讲)——2021年高考化学一轮复习讲练测吉林省长春汽车经济技术开发区第六中学2020-2021学年高二上学期月考化学试题江西省南昌市第二中学2021届高三上学期第四次考试理综化学试题(已下线)专题4.2 化学电源-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)湖南省长沙县第九中学2020-2021学年高二上学期第三次月考化学试题(已下线)小题必刷25 原电池及化学电源——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷26 电解池原理及其应用——2021年高考化学一轮复习小题必刷(通用版本)江西省南昌市南昌县莲塘第一中学2021届高三上学期12月质量检测化学试题山西省太原市2021届高三上学期期末考试化学试题(已下线)4.2 化学电源(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)江西省新余市第四中学2021届高三化学上学期第四次考试试题安徽省滁州市明光中学2020-2021学年高二下学期开学考试化学试题浙江省之江教育评价2021届高三下学期返校联考化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练山西省晋城市2021届高三上学期期末考试化学试题山西省长治市2021届高三上学期期末考试化学试题(已下线)小题16 新型原电池装置——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第11题 电化学基础-备战2021年高考化学临考题号押题(课标全国卷)江苏省苏州市姑苏区苏州中学2020-2021学年高二下学期期中考试化学试题江西省九江市第三中学2020-2021学年高一下学期期中考试化学试题河南省原阳县第三高级中学2020-2021学年高一下学期第三次月考化学试题四川省广安友谊中学高2020-2021学年高一下学期6月月考化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 C 高考挑战区吉林省长春外国语学校2020-2021学年高二下学期第二次月考化学试题河南省信阳高级中学2020-2021学年高一6月月考化学试题选择性必修1(SJ)专题1专题培优专练(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)选择性必修1 专题1 素养检测(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第16讲 原电池 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(四)新型电源及电极反应式的书写 (讲) — 2022年高考化学一轮复习讲练测(新教材新高考)江西省靖安中学2021届高三上学期第四次月考化学试题黑龙江省青冈县第一中学校2022届高三上学期第一次模拟考试化学试题(已下线)第六单元 化学反应与能量(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)黑龙江省大庆市东风中学2021-2022学年高二上学期期中考试化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)2020年全国卷Ⅲ化学真题变式题(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习山东省烟台第二中学2021-2022学年高一3月月月考化学试题(已下线)押全国卷理综第11题 电化学基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点03 电化学-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题08电化学及其应用-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题08电化学及其应用-五年(2018~2022)高考真题汇编(全国卷)(已下线)第08练 以新型化学电源及电极反应式的书写突破原电池原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)第四章 综合拔高练四川省内江市第六中学2022---2023学年高二上学期入学考试化学试题 (已下线)第16讲 原电池 新型电源 (练)-2023年高考化学一轮复习讲练测(新教材新高考)云南省罗平县第五中学2021-2022学年高二下学期6月月考化学试题福建省福州市第一中学2022-2023学年高二上学期10月月考化学试题河南省濮阳市第一高级中学2022-2023学年高三上学期第三次质量检测考试化学试题(已下线)化学(北京A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)专题十一 化学能与电能-实战高考·二轮复习核心突破(已下线)第一部分 二轮专题突破 专题11 新型电池和电解原理的应用贵州省铜仁市第二中学2022-2023学年高三上学期第二次月考化学试题(已下线)题型16 金属-空气电池的应用(已下线)第六章 化学反应与能量 第36练 新型化学电源(已下线)专题卷14 新型化学电源装置-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)四川省乐山市沫若中学2021-2022学年高二下学期第二次月考化学试题(已下线)专题12 电化学的综合应用四川省绵阳南山中学2022-2023学年高一下学期6月月考化学试题 (已下线)第3讲 原电池 化学电源福建省厦门市松柏中学2023-2024学年高二上学期10月月考化学试题四川省眉山市彭山区第一中学2023-2024学年高二上学期12月月考化学试题河南省焦作市第十一中学2023-2024学年高二上学期12月份月考 化学试卷云南省大理州实验中学2021-2022学年高二上学期化学期中考试题天津市南开中学2024届高三下学期第五次月检测化学试卷2024届四川省雅安市神州天立学校高三下学期高考冲刺考试理科综合试题-高中化学
3 . 科学家近年发明了一种新型Zn−CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
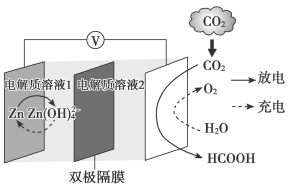
A.放电时,负极反应为 |
| B.放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol |
C.充电时,电池总反应为 |
| D.充电时,阳极室溶液中OH−浓度升高 |
您最近一年使用:0次
2020-07-08更新
|
27379次组卷
|
102卷引用:陕西省渭南中学2023届高三上学期第二次质量调研化学试题
陕西省渭南中学2023届高三上学期第二次质量调研化学试题2020年全国统一考试化学试题(新课标Ⅰ)(已下线)专题08 电化学及其应用-2020年高考真题和模拟题化学分项汇编广州市天河中学2019—2020学年高二下学期期末测试化学试卷(已下线)第04章 电化学基础(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)黑龙江省哈尔滨师范大学附属中学2020-2021学年高二上学期开学考试化学试题新疆哈密市第十五中学2021届高三上学期第一次质量检测化学试题吉林省辽源市第五中学2019-2020学年高一下学期期末考试化学试题(已下线)专题讲座(六)新型电源及电极反应式的书写(精讲)——2021年高考化学一轮复习讲练测(已下线)第20讲 原电池 化学电源(精讲)——2021年高考化学一轮复习讲练测山东省莱州市第一中学2020-2021学年高二上学期10月月考化学试题山东省章丘市第一中学2020-2021学年高二上学期9月月考化学试题(已下线)第四章 化学反应与电能(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)北京首都师范大学附属中学2020-2021学年高二上学期期中考试化学试题山东省枣庄市2021届高三上学期第三次质量检测化学试题江苏省镇江市镇江中学2021届高三上学期期中教学质量检测化学试题黑龙江省哈尔滨市南岗区哈尔滨师范大学附属中学2021届高三上学期期中考试化学试题吉林省白城市洮南市第一中学2020-2021学年高二上学期第三次月考化学试题(已下线)小题必刷25 原电池及化学电源——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷26 电解池原理及其应用——2021年高考化学一轮复习小题必刷(通用版本)河北省石家庄市第二十四中学2021届高三上学期月考化学试卷黑龙江省鸡西市第一中学2020-2021学年度高二上学期期末化学试题广东省中山市2020-2021学年高二上学期期末考试化学试题人教版2019必修第二册 第六章 第一节综合拔高练(已下线)热点6 电化学及其应用-2021年高考化学专练【热点·重点·难点】(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记重庆市第七中学校2020-2021学年高二上学期12月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)小题18 可充电电池装置 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)押全国卷理综第11题 电化学基础-备战2021年高考化学临考题号押题(课标全国卷)(已下线)押山东卷第10题 原电池选择题-备战2021年高考化学临考题号押题(山东卷)江苏省苏州市姑苏区苏州中学2020-2021学年高二下学期3月月考化学试题(已下线)【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00117】(已下线)第18讲 原电池 化学电源(精讲)-2022年一轮复习讲练测选择性必修1(SJ)专题1专题培优专练(已下线)课时32 可充电电池装置-2022年高考化学一轮复习小题多维练(全国通用)选择性必修1 专题1 素养检测(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点21 原电池 化学电源-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第16讲 原电池 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)江苏省如皋中学2021-2022学年高三上学期期初测试化学试题(已下线)专题讲座(四)新型电源及电极反应式的书写 (讲) — 2022年高考化学一轮复习讲练测(新教材新高考)河北正定中学2020-2021学年高二上学期开学考试化学试题江苏省苏州八校联盟2021-2022学年高三上学期第一次适应性检化学试题山东省滕州市第五中学2021-2022学年高二上学期第一次单元测试化学试题山东省济南德润高级中学2021-2022学年高二上学期10月月考化学试题山东省菏泽市郓城实验中学2021-2022学年高二上学期10月月考化学试题(已下线)专题08 电化学之电解池-【微专题·大素养】备战2022年高考化学讲透提分要点(已下线)第六单元 化学反应与能量(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省山河联盟2021-2022学年高二上学期12月考试化学试题2020年全国卷Ⅰ理综化学高考真题变式题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习福建省福州华侨中学2021-2022学年高二上学期期中考试化学试题(已下线)押全国卷理综第11题 电化学基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点03 电化学-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)四川省绵阳市盐亭中学2021-2022学年高二下学期第三次月考化学试题湖南省常德市鼎城区第一中学2021-2022学年高三下学期期中考试化学试题(已下线)专题08电化学及其应用-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题08电化学及其应用-五年(2018~2022)高考真题汇编(全国卷)浙江省浙江大学附属中学2021-2022学年高三下学期5月份仿真模拟化学试题 江西省赣州市定南中学2021-2022学年高二下学期5月月考化学试题内蒙古赤峰二中2021-2022学年高二下学期第二次月考化学试题(已下线)第09练 以隔膜在电化学中的功能突破电解原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)浙江省绍兴市柯桥区2021-2022 学年高三下学期选考科目6月适应性考试化学试题(已下线)【教材实验热点】09 化学能与电能广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第三次月考化学试题(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)宁夏石嘴山市第三中学2021-2022学年高三上学期期末考试化学试题福建省福州市五校联考2021-2022学年高二上学期期中考试化学试题第四章 综合拔高练(已下线)第16讲 原电池 新型电源 (练)-2023年高考化学一轮复习讲练测(新教材新高考)西藏自治区拉萨中学2022届高三第六次月考理综化学试题四川省成都市西北中学2021-2022学年高二下学期3月月考化学试题浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题福建省福州第十五中学2022-2023学年高二上学期10月月考化学试题福建省厦门市国祺中学2021-2022学年高三上学期期中考试化学试题重庆市西南大学附属中学校2022-2023学年高二上学期开学定时训练化学试题(广延班)(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题11 新型电池和电解原理的应用(已下线)第六章 化学反应与能量 第35讲 原电池 化学电源(已下线)题型104 二次电池(已下线)专题七 电化学中“离子交换膜”的应用(练习)四川省广安市第二中学校2022-2023学年高二下学期第一次月考化学试题(已下线)专题卷14 新型化学电源装置-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)四川省广元中学2022-2023学年高二下学期4月月考化学试题(已下线)题型21 四室膜和双极膜电解装置及其应用(已下线)专题12 电化学的综合应用安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题(已下线)第3讲 原电池 化学电源福建省三明第一中学2022-2023学年高三上学期期中考试化学试题天津市第八中学2022-2023学年高三上学期期中检测化学试题江苏省南京航空航天大学苏州附属中学2023-2024学年高二上学期10月月考化学试题江苏省南航苏州附中2023-2024学年高二上学期10月月考化学试题河北省沧州市2023-2024学年高二上学期12月月考化学试题黑龙江省大庆市肇州县第二中学2023-2024学年高三上学期12月月考化学试题河南省焦作市第十一中学2023-2024学年高二上学期12月份月考 化学试卷北京市第一五六中学2021-2022学年高三上学期期中考试化学试题江西省宜春市宜丰中学2023-2024学年高二下学期4月期中考试化学试题辽宁省沈阳市东北育才学校科学高中部2024届高三下学期最后一模化学试题
名校
解题方法
4 . 将两极质量相同的铜棒和锌棒,用导线相连接后插入CuSO4溶液中,经过一段时间后,取出洗净后干燥并称重,两棒质量相差6.45 g,导线中通过的电子的物质的量为 ( )
| A.0.1 mol | B.0.2 mol | C.0.3 mol | D.0.4 mol |
您最近一年使用:0次
2020-05-12更新
|
132次组卷
|
3卷引用:陕西省渭南市华州区咸林中学2022-2023学年高一下学期期中考试化学试题
解题方法
5 . (1)选择适宜的材料和试剂设计一个原电池,完成下列反应:Zn+CuSO4=ZnSO4+Cu。
①画出装置图:___ 。
②电极材料和电解质溶液各是什么___ 。?
③写出电极反应式:负极:___ ;正极:___ 。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25克,铜表面析出了氢气___ L(标准状况下)。导线中通过___ mol电子。
①画出装置图:
②电极材料和电解质溶液各是什么
③写出电极反应式:负极:
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25克,铜表面析出了氢气
您最近一年使用:0次
2020-05-08更新
|
70次组卷
|
2卷引用:陕西省渭南市三贤中学2020年高一下学期期中考试化学试题
解题方法
6 . 用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)
图1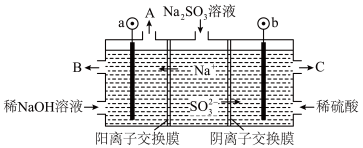 图2
图2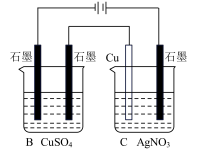
(1)图1中a极要连接电源的__________ (填“正”或“负”)极,SO32-放电的电极反应__________
(2)在图2所示的装置中,若通入直流电5 min时,铜电极质量增加2.16g,试回答:
①溶液pH变化:B__________ ,C__________ (填“增大”“减小”或“不变”)。
②通电5 min时,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为__________ (设电解前后溶液体积无变化)。
图1
 图2
图2
(1)图1中a极要连接电源的
(2)在图2所示的装置中,若通入直流电5 min时,铜电极质量增加2.16g,试回答:
①溶液pH变化:B
②通电5 min时,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为
您最近一年使用:0次
名校
解题方法
7 . 氢氧燃料电池是的介色化学理的新型发电装置,下图为电池示意图,该电池电极表面镀一层细细的铂粉,吸附气体的能力强,性质稳定,请回答
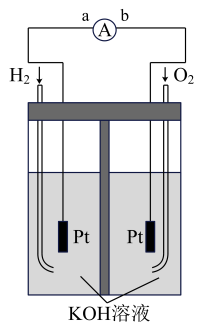
(1)氢氧燃料电量的转化形式是____ ,在导线中电子的流动方向为______ (用a,b表示)
(2)负极反应式为___________
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,因此大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2↑
①反应I中的还原剂是______ ,反应II中的氧化剂是______
②由LiH与H2O作用,放出224L(标准状况)H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为____ mol;将产生的电能用来电解饱和食盐水,产生的氢气体积(标准状况)为_____ L

(1)氢氧燃料电量的转化形式是
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,因此大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2↑
①反应I中的还原剂是
②由LiH与H2O作用,放出224L(标准状况)H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
您最近一年使用:0次
名校
解题方法
8 . 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。该电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )| A.放电时正极反应为:FeO42-+3e-+4H2O=Fe(OH)3↓+5OH- |
| B.充电时阴极反应为:Zn(OH)2+2e-=Zn+2OH- |
| C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 |
| D.标有“+”的接线柱充电时作阳极,放电时作正极 |
您最近一年使用:0次
2020-03-19更新
|
171次组卷
|
5卷引用:陕西省渭南市尚德中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
9 . 某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:
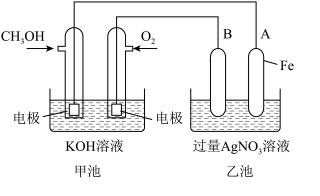
(1)充电时,原电池的负极与电源___ 极相连。乙池中阳极的电极反应为___ 。
(2)放电时:负极的电极反应式为___ 。
(3)在此过程中若完全反应,乙池中A极的质量增加648 g,则甲池中理论上消耗O2___ L(标准状况下)。
(4)若在常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,表示甲醇燃烧热的热化学方程式为___ 。

(1)充电时,原电池的负极与电源
(2)放电时:负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质量增加648 g,则甲池中理论上消耗O2
(4)若在常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
2019-12-13更新
|
282次组卷
|
5卷引用:陕西省渭南韩城市2019-2020学年高二上学期竞赛考试化学试题
名校
10 . 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

请回答:(1)B极是电源的___ 极,电极C的电极反应式为:___ 。
(2)若C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为___ 。
(3)现用丙装置给铜件镀银,则H电极材料是___ (填“铜”或“银”),电镀液是___ 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为___ 。
(4)一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明__ 在电场作用下向Y极移动。

请回答:(1)B极是电源的
(2)若C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H电极材料是
(4)一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明
您最近一年使用:0次
2019-12-06更新
|
171次组卷
|
2卷引用:陕西省渭南市临渭区尚德中学2019-2020学年高二上学期期中考试化学试题



