名校
解题方法
1 . 氯碱工业是以电解饱和食盐水为核心工艺的化学工业。完成下列填空:
I.
(1)写出电解饱和食盐水的离子方程式:_______ 。
II.如图是实验室模拟电解饱和食盐水的装置,连通电源后,b电极附近的溶液首先变红。

(2)b极使溶液显红色的主要微粒是_______ 。
(3)a是该电解装置的_______ 极,表面发生的反应类型属于_______ 反应(填“氧化”或“还原”)。检验a极产物的化学方法是:_______ 。
(4)若采用粗盐(含 、
、 、
、 等杂质)配制的溶液进行电解,
等杂质)配制的溶液进行电解,_______ 极还可能出现白色浑浊的现象,原因是:_______ (用离子方程式表示)。
(5)当转移0.2 电子时,标准状况下生成的氢气体积为
电子时,标准状况下生成的氢气体积为_______ 。
(6) 在溶液中的移动方向是:a
在溶液中的移动方向是:a_______ b(填“→”或“←”)。工业上电解熔融的NaCl制得金属Na,解释电解饱和食盐水得不到金属Na的主要原因: _______ 。
I.
(1)写出电解饱和食盐水的离子方程式:
II.如图是实验室模拟电解饱和食盐水的装置,连通电源后,b电极附近的溶液首先变红。

(2)b极使溶液显红色的主要微粒是
(3)a是该电解装置的
(4)若采用粗盐(含
 、
、 、
、 等杂质)配制的溶液进行电解,
等杂质)配制的溶液进行电解,(5)当转移0.2
 电子时,标准状况下生成的氢气体积为
电子时,标准状况下生成的氢气体积为(6)
 在溶液中的移动方向是:a
在溶液中的移动方向是:a
您最近一年使用:0次
2 . 食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量K+、Ca2+、Mg2+、SO 等杂质离子,实验室提纯NaCl的流程如图:
等杂质离子,实验室提纯NaCl的流程如图:
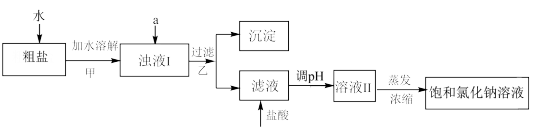
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。
(1)欲除去粗盐溶解后形成溶液中的Ca2+、Mg2+、SO 离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:
离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:____ 、____ 、____ (只填化学式)。为检测SO 离子是否沉淀完全,请你写出检验方法:
离子是否沉淀完全,请你写出检验方法:____ 。
(2)上述流程中,甲、乙两个过程均要用到玻璃棒,玻璃棒的作用分别是甲____ ,乙____ 。
(3)饱和食盐水通过____ 可以得到的NaCl晶体。
(4)食盐是无机化工生产之母,电解饱和食盐水的装置如图所示。

写出电解饱和食盐水的化学方程式____ ;若在U形管中滴加酚酞溶液,电解一段时间后,U形管_____ (填电极“X”或“Y”)边的溶液变红。检验电解食盐水X电极产物的方法是____ ;若电解时消耗了117克氯化钠,则理论上得到氯气的最大体积为____ (标准状况)。
 等杂质离子,实验室提纯NaCl的流程如图:
等杂质离子,实验室提纯NaCl的流程如图:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。
(1)欲除去粗盐溶解后形成溶液中的Ca2+、Mg2+、SO
 离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:
离子,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为: 离子是否沉淀完全,请你写出检验方法:
离子是否沉淀完全,请你写出检验方法:(2)上述流程中,甲、乙两个过程均要用到玻璃棒,玻璃棒的作用分别是甲
(3)饱和食盐水通过
(4)食盐是无机化工生产之母,电解饱和食盐水的装置如图所示。

写出电解饱和食盐水的化学方程式
您最近一年使用:0次
2022-08-27更新
|
412次组卷
|
3卷引用:上海市静安区七一中学分部2021-2022学年高一上学期期中考试化学试题
上海市静安区七一中学分部2021-2022学年高一上学期期中考试化学试题(已下线)2.1.1 粗盐的提纯和氯碱工业-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)上海市陆行中学2022-2023学年高一上学期期中考试化学试题
3 . 碳酸锂是生产锂离子电池的重要原料。
(1)碳酸锂制取锂的反应原理为:
① ;
;
②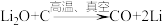 。
。
锂原子的电子排布式为___ ;CO2的结构式为____ ;反应②中物质涉及的化学键类型有____ 。
(2)碳原子核外电子有_ 种不同能量的电子,其中有两个电子的能量最高且能量相等,这两个电子所处的轨道分别是__ 。
(3)氢化锂(LiH)是离子化合物,写出其阴离子的电子式___ ,氢负离子(H-)与锂离子具有相同电子层结构,试比较两者微粒半径的大小,并用原子结构理论加以解释:___ 。
(4)用 、氨水和液溴制备
、氨水和液溴制备 。除生成
。除生成 外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:
外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式: ,
,_____ 。
(5)磷酸亚铁锂电池总反应为: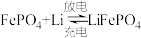 ,放电时,负极为
,放电时,负极为___ (填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有 气体(标准状况)产生时,该电池消耗锂的质量为
气体(标准状况)产生时,该电池消耗锂的质量为___ 。
(1)碳酸锂制取锂的反应原理为:
①
 ;
;②
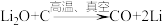 。
。锂原子的电子排布式为
(2)碳原子核外电子有
(3)氢化锂(LiH)是离子化合物,写出其阴离子的电子式
(4)用
 、氨水和液溴制备
、氨水和液溴制备 。除生成
。除生成 外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:
外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式: ,
,(5)磷酸亚铁锂电池总反应为:
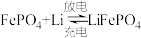 ,放电时,负极为
,放电时,负极为 气体(标准状况)产生时,该电池消耗锂的质量为
气体(标准状况)产生时,该电池消耗锂的质量为
您最近一年使用:0次
4 . 近来, 科学家研制了一种新型的乙醇电池(DEFC), 它用磺酸类质子作溶剂, 在200℃左右时供电, 乙醇电池比甲醇电池效率高出32倍且更加安全。电池总反应式为: C2H5OH+3O2 2CO2+3H2O。下列说法不正确的是
2CO2+3H2O。下列说法不正确的是
 2CO2+3H2O。下列说法不正确的是
2CO2+3H2O。下列说法不正确的是| A.C2H5OH在电池的负极上参加反应 | B.1 mol乙醇被氧化转移6 mol电子 |
| C.在外电路中电子由负极沿导线流向正极 | D.电池正极得电子的物质是O2 |
您最近一年使用:0次
2016-07-04更新
|
430次组卷
|
11卷引用:上海市青浦区朱家角中学2021-2022学年高一上学期10月月考化学试题
上海市青浦区朱家角中学2021-2022学年高一上学期10月月考化学试题湖南省长沙市第一中学2020-2021学年高二下学期开学考化学试题云南省曲靖市第二中学2021-2022学年高二上学期开学收心检测化学试题2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷2015-2016学年河北省冀州市中学高一下期末化学试卷2015-2016学年河北省冀州市中学高一下期末理科化学A卷2015-2016学年山西省阳高一中高一下学期期末化学试卷2016-2017学年宁夏吴忠中学高二上学期开学考试化学试卷四川省成都市成华区2016-2017学年高一下学期期末考试化学试题黑龙江省哈尔滨师范大学附属中学2019-2020学年高一下学期期末考试化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第二节 化学反应与能量转化



