1 . 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的 在5.0~6.0之间,通过电解生成
在5.0~6.0之间,通过电解生成 沉淀。
沉淀。 有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
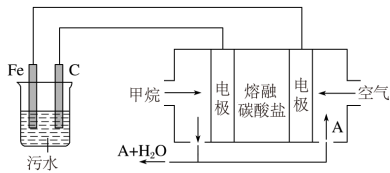
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的___________ (填字母)。
a. b.
b. c.
c. d.
d.
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应分别是___________ ;___________ 。
(3)该熔融盐燃料电池是以熔融碳酸盐为电解质,以 为燃料,空气为氧化剂,稀土金属材料为电极。
为燃料,空气为氧化剂,稀土金属材料为电极。
①正极的电极反应为___________ 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环,A物质的化学式是___________ 。
(4)实验过程中,若在阴极产生了67.2L(标准状况)气体,则熔融盐燃料电池消耗 (标准状况)
(标准状况)___________ L。
 在5.0~6.0之间,通过电解生成
在5.0~6.0之间,通过电解生成 沉淀。
沉淀。 有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的
a.
 b.
b. c.
c. d.
d.
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应分别是
(3)该熔融盐燃料电池是以熔融碳酸盐为电解质,以
 为燃料,空气为氧化剂,稀土金属材料为电极。
为燃料,空气为氧化剂,稀土金属材料为电极。①正极的电极反应为
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环,A物质的化学式是
(4)实验过程中,若在阴极产生了67.2L(标准状况)气体,则熔融盐燃料电池消耗
 (标准状况)
(标准状况)
您最近一年使用:0次
解题方法
2 . 化学电源分为一次电池、二次电池和燃料电池,它们在生产生活中具有广泛的应用及发展前景。
(1)一种可充电的“锂—空气电池”的工作原理如图1所示。

①电池放电过程中,金属锂发生______ (填“氧化”或“还原”)反应。
②电池正极的反应式为_______ 。
(2)镍镉电池是二次电池,其工作原理如图2所示(L为小灯泡,K1、K2为开关,a、b为直流电源的两极)。
①断开K2、闭合K1,此时镍镉电池的能量转化形式为______ 。
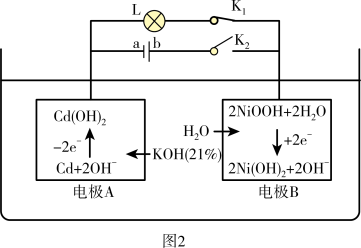
②电极B发生氧化反应过程中,溶液中KOH浓度______ (填“增大”、“减小”或“不变”)。
(3)研究HCOOH燃料电池性能的装置如图3所示,两电极之间用允许K+、H+通过的半透膜隔开。
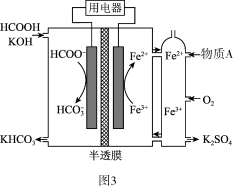
①电池负极的电极反应式为______ ;放电过程中需补充的物质A为______ (填化学式)。
②电池工作时每消耗标准状况下22.4LO2,电路中转移电子的数目为______ NA。
(1)一种可充电的“锂—空气电池”的工作原理如图1所示。

①电池放电过程中,金属锂发生
②电池正极的反应式为
(2)镍镉电池是二次电池,其工作原理如图2所示(L为小灯泡,K1、K2为开关,a、b为直流电源的两极)。
①断开K2、闭合K1,此时镍镉电池的能量转化形式为

②电极B发生氧化反应过程中,溶液中KOH浓度
(3)研究HCOOH燃料电池性能的装置如图3所示,两电极之间用允许K+、H+通过的半透膜隔开。

①电池负极的电极反应式为
②电池工作时每消耗标准状况下22.4LO2,电路中转移电子的数目为
您最近一年使用:0次
名校
解题方法
3 . 如图1所示,某同学设计燃料电池并探究氯碱工业原理的相美问题,其中乙装置中X为阳离子交换膜。
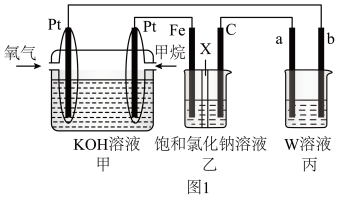
(1)石墨电极(C)作_________ 极,甲中甲烷燃料电池的负极反应式为_________ 。
(2)若在标准状况下,有 氧气参加反应,则乙装置中C电极上生成气体的物质的量为
氧气参加反应,则乙装置中C电极上生成气体的物质的量为_________  。
。
(3)若W为 溶液,欲用丙装置给铜镀银,b电极应是
溶液,欲用丙装置给铜镀银,b电极应是_________ (填化学式)。
(4)若丙中以 溶液为电解质溶液进行粗铜(含
溶液为电解质溶液进行粗铜(含 、
、 、
、 、
、 、
、 等杂质)的电解精炼,下列说法正确的是_________(填字母)。
等杂质)的电解精炼,下列说法正确的是_________(填字母)。
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解 的原理如图2所示。
的原理如图2所示。

① 电极上的电极反应式为
电极上的电极反应式为_________ 。
②若电解过程中转移了 电子,则膜两侧电解液的质量变化差
电子,则膜两侧电解液的质量变化差 为
为_________ 。

(1)石墨电极(C)作
(2)若在标准状况下,有
 氧气参加反应,则乙装置中C电极上生成气体的物质的量为
氧气参加反应,则乙装置中C电极上生成气体的物质的量为 。
。(3)若W为
 溶液,欲用丙装置给铜镀银,b电极应是
溶液,欲用丙装置给铜镀银,b电极应是(4)若丙中以
 溶液为电解质溶液进行粗铜(含
溶液为电解质溶液进行粗铜(含 、
、 、
、 、
、 、
、 等杂质)的电解精炼,下列说法正确的是_________(填字母)。
等杂质)的电解精炼,下列说法正确的是_________(填字母)。| A.a电极为纯铜 | B.粗铜接电源正极,发生还原反应 |
C.溶液中 的浓度保持不变 的浓度保持不变 | D.利用阳极泥可回收 、 、 、 、 等金属 等金属 |
 的原理如图2所示。
的原理如图2所示。
①
 电极上的电极反应式为
电极上的电极反应式为②若电解过程中转移了
 电子,则膜两侧电解液的质量变化差
电子,则膜两侧电解液的质量变化差 为
为
您最近一年使用:0次
解题方法
4 . 碱性电池具有容量大.放电电流大的特点,因而得到广泛应用。碱性锌锰电池以氢氧化钾溶液为电解液,电池反应方程式为:
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
| A.电池工作时,电子由正极通过外电路流向负极 |
| B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,锌失去电子 |
| D.外电路中每通过0.2 mol电子,锌的质量减少6.5 g |
您最近一年使用:0次
解题方法
5 . 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图(a、b为石墨电极)所示,下列说法正确的是
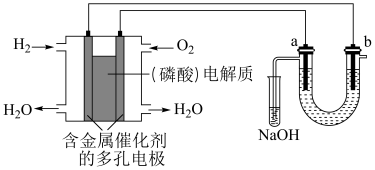

| A.电池工作时,正极反应式为O2+2H2O +4e-=4OH- |
| B.电解时,电子流动路径:负极→外电路→阴极→溶液→阳极→正极 |
| C.试管中NaOH溶液可以用饱和食盐水替代 |
| D.忽略能量损耗,当电池中消耗2.245L(标准状况)H2时,b极会产生0.1mol气体 |
您最近一年使用:0次
2022-09-22更新
|
174次组卷
|
2卷引用:陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题
解题方法
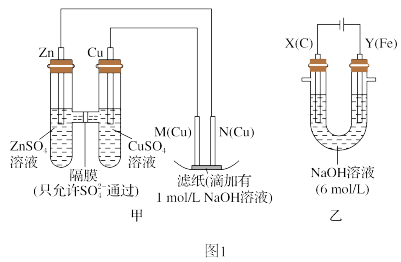
6 . 为探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示装置进行实验。
Ⅰ.用图1甲装置进行第一组实验:
(1)实验过程中,
_______ (填“从左向右”、“从右向左”或“不”)移动。
(2)电极M处滤纸上可观察到的现象是_______ 。
(3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。
)在溶液中呈紫红色。
①电解过程中,Y极发生的电极反应为 和
和_______ 。
②电解一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气体体积为_______ mL(气体均为标准状况下的体积)。
Ⅱ.某同学设计如图2所示燃料电池探究氯碱工业原理和粗铜的精炼原理:
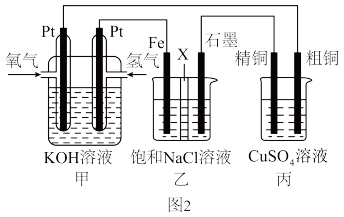
(4)下列说法正确的是_______(填字母)。
(5)如果粗铜中含有锌,银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将_______ (填“增大”、“减小”或“不变”)。若在标准状况下,有224mL氧气参加反应,则丙装置中阴极析出铜的质量为_______ g。
Ⅲ.以铬酸钾( )为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
)为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
 ):
):
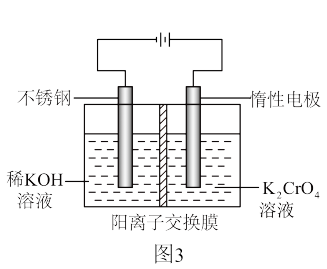
(6)分析阳极区能得到重铬酸钾溶液的原因_______ 。
(7)电解一段时间后,测得阳极区溶液中 物质的量由a mol变为b mol,则此时铬酸钾的转化率为
物质的量由a mol变为b mol,则此时铬酸钾的转化率为_______ 。
Ⅰ.用图1甲装置进行第一组实验:

(1)实验过程中,

(2)电极M处滤纸上可观察到的现象是
(3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。①电解过程中,Y极发生的电极反应为
 和
和②电解一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气体体积为
Ⅱ.某同学设计如图2所示燃料电池探究氯碱工业原理和粗铜的精炼原理:

(4)下列说法正确的是_______(填字母)。
| A.装置甲中通入氢气的电极为正极,装置乙中石墨电极为阳极 |
B.装置甲中负极的电极反应式为 |
| C.反应一段时间后,在乙装置中滴入酚酞溶液,铁极区的溶液先变红 |
| D.若用隔膜法电解饱和食盐水生成NaClO,则X应为阳离子交换膜 |
Ⅲ.以铬酸钾(
 )为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
)为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
 ):
):
(6)分析阳极区能得到重铬酸钾溶液的原因
(7)电解一段时间后,测得阳极区溶液中
 物质的量由a mol变为b mol,则此时铬酸钾的转化率为
物质的量由a mol变为b mol,则此时铬酸钾的转化率为
您最近一年使用:0次
名校
7 . 回答下列问题:
(1)根据氧化还原反应: 设计原电池如图所示,其中盐桥中盛有琼脂-饱和
设计原电池如图所示,其中盐桥中盛有琼脂-饱和 溶液。
溶液。
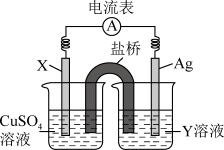
①Y是_______ (填化学式)。
②若开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为_______ g。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
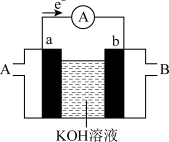
①假设使用的“燃料”是氢气 ,则a极的电极反应式为
,则a极的电极反应式为_______ 。若电池中氢气 通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为
通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为_______ C(已知一个电子所带电量为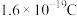 ,
, 约为
约为 )。
)。
②假设使用的“燃料”是甲醇 ,则a极的电极反应式为
,则a极的电极反应式为_______ 。如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为_______ (用 表示)。
表示)。
(3)一种高性能的碱性硼化钒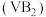 -空气电池如下图所示,电池总反应为
-空气电池如下图所示,电池总反应为 。
。

①正极区溶液的pH_______ (选填“升高”或“降低”)。
② 电极发生的电极反应为
电极发生的电极反应为_______ 。
(1)根据氧化还原反应:
 设计原电池如图所示,其中盐桥中盛有琼脂-饱和
设计原电池如图所示,其中盐桥中盛有琼脂-饱和 溶液。
溶液。
①Y是
②若开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气
 ,则a极的电极反应式为
,则a极的电极反应式为 通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为
通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为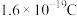 ,
, 约为
约为 )。
)。②假设使用的“燃料”是甲醇
 ,则a极的电极反应式为
,则a极的电极反应式为 表示)。
表示)。(3)一种高性能的碱性硼化钒
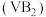 -空气电池如下图所示,电池总反应为
-空气电池如下图所示,电池总反应为 。
。
①正极区溶液的pH
②
 电极发生的电极反应为
电极发生的电极反应为
您最近一年使用:0次
名校
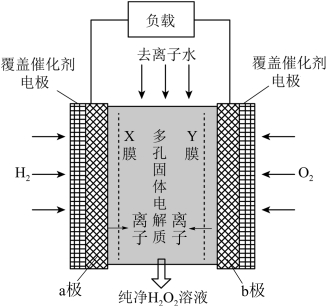
8 . 2019年11月《Science》杂志报道了王浩天教授团队发明的制取H2O2的绿色方法,原理如图所示(已知:H2O2 H++
H++ ,Ka=2.4×10﹣12)。下列说法错误的是
,Ka=2.4×10﹣12)。下列说法错误的是
 H++
H++ ,Ka=2.4×10﹣12)。下列说法错误的是
,Ka=2.4×10﹣12)。下列说法错误的是
| A.X膜为阳离子交换膜 |
| B.每生成1molH2O2,外电路通过4mole- |
| C.催化剂可加快单位时间内反应中电子的转移数目 |
D.b极上的电极反应为:O2+H2O+2e- ═ +OH− +OH− |
您最近一年使用:0次
2022-02-28更新
|
390次组卷
|
15卷引用:陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题
陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题浙江省丽水市高中发展共同体2020-2021学年高二下学期期中联合测试化学试题安徽省合肥市六校2020-2021学年高二下学期期末联考化学试题江苏省常熟市2021-2022学年高三上学期阶段性抽测一化学试题山东省聊城第三中学2021-2022学年高二上学期第三次质量检测化学试题2019年江苏省南京、盐城高三第一次模拟考试化学试题山东省济宁市2020届高三下学期线上自我检测化学试题重庆市第一中学2020届高三3月月考理科综合化学试题江苏省宿迁市沭阳县2019-2020学年高二下学期期中调研测试化学试题江苏省连云港市老六所四星高中(海州高中 、赣榆高中 、海头中学 、东海高中 新海高中 、灌云高中)2020届高三模拟考试化学试题宁夏中卫市2020届高三第二次模拟考试理综化学试题天津市河西区2020芦台一中高三模拟测试江苏省泰州中学2019-2020学年高二下学期第二次月考化学试题山东省烟台第二中学2021-2022学年高一3月月月考化学试题宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题
解题方法
9 . 羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为CO2,H2O的原电池–电解池组合装置(如图),该装置能实现发电、环保二位一体。下列说法正确的是
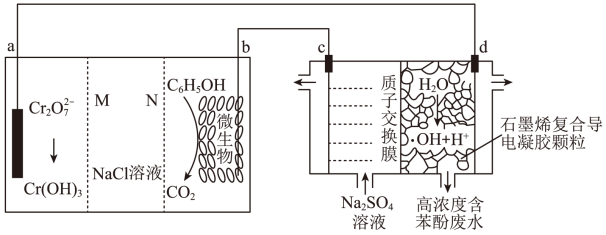

| A.电池工作时,b电极附近pH增加 |
| B.d极区苯酚被氧化的化学方程式为C6H5OH +28·OH=6CO2↑+17H2O |
C.a极每有1 mol Cr2O 参与反应,通过质子交换膜的H+数目理论上有8 NA个 参与反应,通过质子交换膜的H+数目理论上有8 NA个 |
| D.右侧装置中,每转移0.7 mol电子,c、d 两极共产生气体3.36L(标准状况) |
您最近一年使用:0次
名校
解题方法
10 . 利用如图所示装置可以将温室气体CO2转化为燃料气体CO,下列说法不正确的是
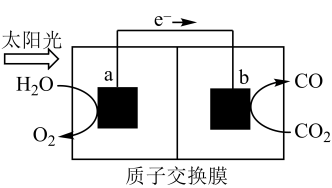

| A.电池工作时a极区溶液的pH降低 |
| B.电极b表面发生反应CO2+2e-+2H+=CO+H2O |
| C.该装置工作时,H+从a极区向b极区移动 |
| D.标准状况下,电极a生成1.12LO2时,两极电解质溶液质量相差3.2g |
您最近一年使用:0次
2021-12-19更新
|
913次组卷
|
7卷引用:陕西省汉中市2021-2022学年高三上学期教学质量第一次检测考试化学试题
陕西省汉中市2021-2022学年高三上学期教学质量第一次检测考试化学试题山东省滨州市2021-2022学年高三上学期第一次检测化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)一轮巩固卷5-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)第34练 原电池-2023年高考化学一轮复习小题多维练(全国通用)新疆石河子第一中学2021-2022学年高一下学期4月月考化学试题山东省潍坊高密市第三中学2022-2023学年高三上学期9月月考化学试题



