解题方法
1 . 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图(a、b为石墨电极)所示,下列说法正确的是
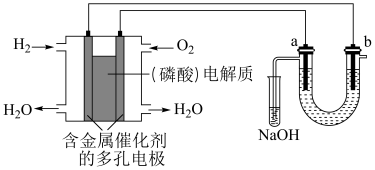

| A.电池工作时,正极反应式为O2+2H2O +4e-=4OH- |
| B.电解时,电子流动路径:负极→外电路→阴极→溶液→阳极→正极 |
| C.试管中NaOH溶液可以用饱和食盐水替代 |
| D.忽略能量损耗,当电池中消耗2.245L(标准状况)H2时,b极会产生0.1mol气体 |
您最近一年使用:0次
2022-09-22更新
|
174次组卷
|
2卷引用:陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题
名校
2 . 回答下列问题:
(1)根据氧化还原反应: 设计原电池如图所示,其中盐桥中盛有琼脂-饱和
设计原电池如图所示,其中盐桥中盛有琼脂-饱和 溶液。
溶液。
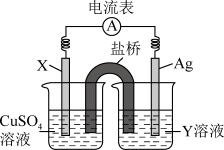
①Y是_______ (填化学式)。
②若开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为_______ g。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
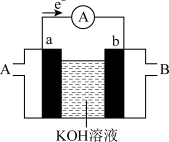
①假设使用的“燃料”是氢气 ,则a极的电极反应式为
,则a极的电极反应式为_______ 。若电池中氢气 通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为
通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为_______ C(已知一个电子所带电量为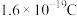 ,
, 约为
约为 )。
)。
②假设使用的“燃料”是甲醇 ,则a极的电极反应式为
,则a极的电极反应式为_______ 。如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为_______ (用 表示)。
表示)。
(3)一种高性能的碱性硼化钒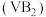 -空气电池如下图所示,电池总反应为
-空气电池如下图所示,电池总反应为 。
。

①正极区溶液的pH_______ (选填“升高”或“降低”)。
② 电极发生的电极反应为
电极发生的电极反应为_______ 。
(1)根据氧化还原反应:
 设计原电池如图所示,其中盐桥中盛有琼脂-饱和
设计原电池如图所示,其中盐桥中盛有琼脂-饱和 溶液。
溶液。
①Y是
②若开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气
 ,则a极的电极反应式为
,则a极的电极反应式为 通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为
通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为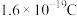 ,
, 约为
约为 )。
)。②假设使用的“燃料”是甲醇
 ,则a极的电极反应式为
,则a极的电极反应式为 表示)。
表示)。(3)一种高性能的碱性硼化钒
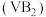 -空气电池如下图所示,电池总反应为
-空气电池如下图所示,电池总反应为 。
。
①正极区溶液的pH
②
 电极发生的电极反应为
电极发生的电极反应为
您最近一年使用:0次
名校
解题方法
3 . 利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是
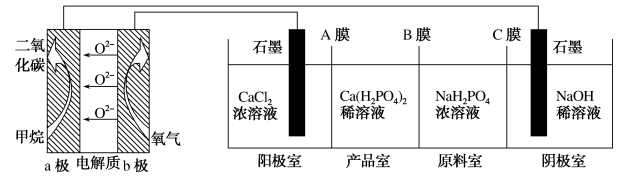
| A.a极的电极反应式为CH4-8e-+4O2-=CO2+2H2O |
| B.A膜和C膜均为阴离子交换膜 |
| C.可用铁电极替换阴极的石墨电极 |
| D.a极上通入2.24L(标准状况下)甲烷,阳极室Ca2+减少0.4mol |
您最近一年使用:0次
2021-10-30更新
|
1076次组卷
|
7卷引用:陕西省西安中学2021届高三第八次模拟考试化学试题
陕西省西安中学2021届高三第八次模拟考试化学试题陕西省西安中学2020届高三第八次模拟考试化学试题河北省河北衡水中学2021届高三下学期第二次调研考试化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】01(已下线)备战2022年高考化学精准检测卷【全国卷】09河南省信阳高级中学2022-2023学年高一下学期7月期末考试化学试题(已下线)重难点03 原电池原理的应用与化学电源-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
名校
4 . 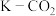 电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的
电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的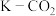 电池。电池总反应为
电池。电池总反应为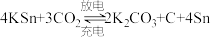 。
。

下列说法错误的是
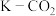 电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的
电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的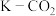 电池。电池总反应为
电池。电池总反应为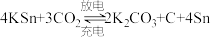 。
。
下列说法错误的是
A.活泼的钾负极替换成 合金是为了改善负极侧的枝晶问题 合金是为了改善负极侧的枝晶问题 |
B.电池的正极反应式为 |
| C.在碳纳米管正极表面引入羧酸根离子,可以使放电产物更易于可逆分解,降低充电过电位 |
D.充电时,每生成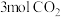 。阴极质量减少 。阴极质量减少 |
您最近一年使用:0次
2021-09-09更新
|
1017次组卷
|
5卷引用:陕西省西安市长安区第一中学2022届高三第一次模拟考试化学试题
陕西省西安市长安区第一中学2022届高三第一次模拟考试化学试题全国2022届高三上学期第一次学业质量联合检测化学试题(已下线)科技热点之几种新型电池重庆市第七中学校2022届高三第二次月考化学试题(已下线)提升卷05-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)
解题方法
5 . 镉可用于制造体积小和电容量大的电池,可利用铜镉渣(主要成分为镉,还含有少量锌、铜、铁、钴(Co)等杂质)来制备,工艺流程如下:

已知:镉(Cd)的金属活动性介于锌、铁之间。
回答下列问题:
(1)“浸出”中,镉的浸出率结果如图所示。由图可知,当镉的浸出率为80%时,所采用的实验条件为___________ ,“浸渣1”是___________ (填名称)。

(2)“除钴”过程中,含Co2+的浸出液中需要加入Zn、Sb2O3产生合金CoSb,写出“除钴”过程的离子方程式___________ 。
(3)“除铁”时先加入适量的KMnO4溶液,其目的是___________ ;再加入ZnO,调节溶液的pH的范围是___________ ,“滤渣3”的主要成分是___________ (填化学式)和MnO2。
室温下相关金属离子[c0(Mn+)=0.1mol·L—1]形成氢氧化物沉淀的pH范围如下:
(4)“电解”步骤中,若阴极生成11.2g金属Cd,阳极生成的气体在标准状况下的体积为___________ L
(5)根据室温下Ksp[Cd(OH)2]= 2.0×10-16,若采用生石灰处理含镉电解废液,当测得室温下溶液的pH为10时,溶液中的Cd2+是否已沉淀完全?___________ (填“是或否”),列式计算___________ 。(已知离子浓度小于1.0×10-5mol·L-1时,即可认为该离子已沉淀完全)。

已知:镉(Cd)的金属活动性介于锌、铁之间。
回答下列问题:
(1)“浸出”中,镉的浸出率结果如图所示。由图可知,当镉的浸出率为80%时,所采用的实验条件为

(2)“除钴”过程中,含Co2+的浸出液中需要加入Zn、Sb2O3产生合金CoSb,写出“除钴”过程的离子方程式
(3)“除铁”时先加入适量的KMnO4溶液,其目的是
室温下相关金属离子[c0(Mn+)=0.1mol·L—1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Cd2+ |
| 开始沉淀的pH | 1.9 | 6.3 | 7.2 |
| 沉淀完全的pH | 3.2 | 8.3 | 9.5 |
(5)根据室温下Ksp[Cd(OH)2]= 2.0×10-16,若采用生石灰处理含镉电解废液,当测得室温下溶液的pH为10时,溶液中的Cd2+是否已沉淀完全?
您最近一年使用:0次
解题方法
6 . 某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。
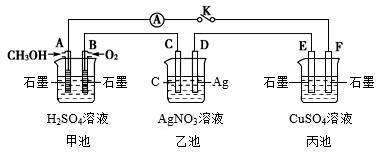
请回答下列问题:
(1)甲池为__ (填“原电池”“电解池”或“电镀池”),通入O2电极的电极反应式为__ 。
(2)乙池中C(石墨)电极的名称为___ (填“正极”“负极”或“阴极”“阳极”),总反应的化学方程式为____ 。
(3)当乙池中D极质量增加5.4g时,甲池中理论上消耗O2的体积为___ mL(标准状况),转移的电子数为__ 。
(4)丙池中__ (填“E”或“F”)极析出铜。
(5)若丙中电极不变,将其溶液换成NaCl溶液,开关闭合一段时间后,丙中溶液的pH将__ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池中C(石墨)电极的名称为
(3)当乙池中D极质量增加5.4g时,甲池中理论上消耗O2的体积为
(4)丙池中
(5)若丙中电极不变,将其溶液换成NaCl溶液,开关闭合一段时间后,丙中溶液的pH将
您最近一年使用:0次
2011·安徽合肥·一模
名校
解题方法
7 . 图甲和图乙是双液原电池装置。由图可判断下列说法中错误的是


A.图甲电池反应的离子方程式为 |
B.反应 能够发生 能够发生 |
| C.盐桥的作用是形成闭合回路,并使两边溶液保持电中性 |
D.当图乙中有 电子通过外电路时,正极有 电子通过外电路时,正极有 析出 析出 |
您最近一年使用:0次
2020-09-12更新
|
764次组卷
|
16卷引用:陕西省西安市铁一中 学2021-2022学年高一下学期期中考试化学试题
陕西省西安市铁一中 学2021-2022学年高一下学期期中考试化学试题2014-2015陕西省西安市庆安高级中学高二上学期期末化学试卷2014-2015陕西省西安市七十中高二上学期期末考试化学试卷选择性必修1专题1第二单元 课时1 原电池的工作原理吉林省长春北师大附属学校2021-2022学年高二上学期期中考试化学试题(已下线)2011届安徽省合肥市高三第一次教学质检化学试卷2016-2017学年吉林省长春实验中学高二上9月月考化学卷(已下线)同步君 选修4 第4章 第1节 原电池高中化学人教版 选修四 第四章 电化学基础 第一节 原电池 原电池黑龙江省哈尔滨师范大学青冈实验中学校2020-2021学年高二上学期开学考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 化学能转化为电能——电池 课时1 原电池的工作原理高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 课时1 原电池的工作原理第一节 原电池 第1课时 原电池的工作原理1.2.1原电池的工作原理 课后作业(四) 原电池的工作原理第四章 第一节 原电池 第1课时 原电池的工作原理
8 . 以铅蓄电池为电源,石墨为电极电解CuSO4溶液(足量),装置如下图。若一段时间后Y电极上有6.4 g红色物质析出,停止电解。下列说法正确的是( )


| A.a为铅蓄电池的负极 |
| B.电解过程中SO42-向右侧移动 |
| C.电解结束时,左侧溶液质量增重8 g |
| D.铅蓄电池工作时正极电极反应式为:PbSO4+2e-===Pb+SO42- |
您最近一年使用:0次
2019-11-23更新
|
380次组卷
|
10卷引用:陕西省西安市蓝田县2021-2022学年高二上学期期末考试化学试题
陕西省西安市蓝田县2021-2022学年高二上学期期末考试化学试题吉林省白城市第一中学2020-2021学年高二下学期3月月考化学试题广东省惠阳高级中学2018届高三上学期12月月考理科综合化学试题(已下线)2019年9月16日 《每日一题》2020年高考一轮复习-电解原理及其应用福建省莆田市第二中学2019-2020学年高二第一学期期中考试化学试题河北省沧州市肃宁县第一中学2019-2020学年高二上学期第四次月考化学试题2017届江西省新余市第四中学、宜春中学高三下学期开学联考理科综合化学试卷云南省玉溪市峨山一中2021—2022学年高二下学期3月月考化学试题上海交通大学附属中学2022-2023学年高二上学期开学摸底考试化学试题宁夏石嘴山市第三中学2022-2023学年高二下学期第一次月考化学(理)试题



