名校
解题方法
1 . 少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢,为了加快此反应速率而不改变H2的量,可以使用如下方法中的
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol·L-1盐酸
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol·L-1盐酸
| A.⑤⑦⑧ | B.③⑤⑧ | C.①⑥⑦ | D.③⑦⑧ |
您最近一年使用:0次
2021-07-14更新
|
417次组卷
|
10卷引用:黑龙江省哈尔滨市第六中学2020-2021学年高一下学期期末考试化学试题
黑龙江省哈尔滨市第六中学2020-2021学年高一下学期期末考试化学试题黑龙江省大庆市东风中学2021-2022学年高一下学期期中考试化学试题新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二上学期第一次月考化学试题河北省石家庄外国语学校2019-2020学年高二上学期期末考试化学试题四川省简阳市阳安中学2020-2021学年高二上学期9月月考化学试题陕西省渭南市澄城县城关中学2020-2021学年高二上学期第一次月考化学试题宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题新疆乌鲁木齐市第八中学2020-2021学年高二上学期第一阶段考试化学试题四川省凉山宁南中学2021-2022学年高二上学期第一次月考化学试题江苏省无锡市太湖高级中学2022-2023学年高二下学期期中考试化学试题
9-10高一下·山东济宁·期中
名校
2 . A、B、C都是金属,当B中混有C时,只有C能被盐酸溶解,A、B与稀硫酸组成原电池时,A为电池的正极,A、B、C三种金属的活动性顺序为
A. | B.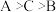 |
C.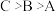 | D.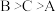 |
您最近一年使用:0次
2021-07-11更新
|
574次组卷
|
26卷引用:黑龙江省牡丹江市第十五中学2020-2021学年高一下学期期中考试化学(文)试题
黑龙江省牡丹江市第十五中学2020-2021学年高一下学期期中考试化学(文)试题(已下线)2010年山东省济宁市第二中学高一下学期期中考试化学试题(已下线)2010—2011学年四川省雅安中学高一下学期期中考试化学试卷(已下线)2011-2012学年江西省九江一中高一下学期期中考试理科化学试卷(已下线)2011-2012学年吉林省四校高一下学期期中联考化学试卷(已下线)2014届云南省昆明滇池中学高一下学期期中考试化学试卷2015-2016学年云南省开远四中高一下学期期中化学试卷山西省新绛县2016-2017学年高一下学期期中考试化学试题湖南省张家界市2015-2016学年高一下学期期末联考(B)化学试题【校级联考】湖北省宜昌市部分示范高中教学协作体2018-2019学年高一第二学期期中联考化学试题甘肃省靖远县第四中学2018-2019学年高一下学期期中考试化学试题山东省青岛市城阳区第三高级中学2018-2019学年高一下学期期中考试化学试题陕西省咸阳市乾县第二中学2019-2020学年高一下学期期中测试化学试题四川省绵阳南山中学实验学校2019-2020学年高一下学期开学考试化学试题北京市平谷区第五中学2019-2020学年高一下学期期中考试化学试题甘肃省张掖市山丹县第一中学2019-2020学年高一下学期期中考试化学试题河南省焦作市沁阳市第一中学2019-2020学年高一下学期第一次月考化学试题(已下线)6.1.2 化学反应与电能(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)广西靖西市第二中学2020-2021学年高一下学期期中水平考试化学试题湖南省长沙市长郡中学2020-2021学年高一下学期期末考试化学试题陕西省宝鸡市陈仓区2020-2021学年高一下学期期中考试化学试题课后-6.1.2 化学反应与电能-人教2019必修第二册吉林省长春汽车经济技术开发区第三中学 2021-2022学年 高一下学期线上月考化学试题甘肃省永昌县第一高级中学2021-2022学年高一下学期期中合格性考试化学试题新疆和田地区皮山县高级中学2021-2022学年高一下学期期中考试化学试题云南省广南县二中2021-2022年学年高二下学期开学考试化学试题
名校
解题方法
3 . 在盛有稀硫酸的烧杯中放入用导线连接的铁片和铜片,下列说法正确的是
| A.铁片上有气泡逸出 | B.电子通过导线由铜流向铁 |
| C.溶液中H+向铜片移动 | D.铁片上发生氧化反应:Fe-3e-=Fe3+ |
您最近一年使用:0次
2021-07-09更新
|
755次组卷
|
4卷引用:黑龙江省哈尔滨市宾县第二中学2021-2022学年高一下学期期末考试化学试题
黑龙江省哈尔滨市宾县第二中学2021-2022学年高一下学期期末考试化学试题河北省唐山市2020-2021学年高一年级下学期期末联考化学试题河北省唐县第一中学2021-2022学年高一下学期期中考试化学试题(已下线)第34练 原电池-2023年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
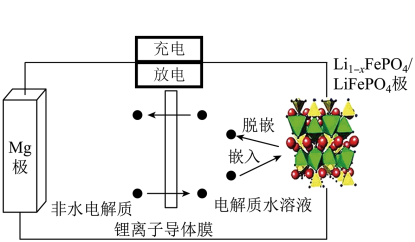
4 . Mg/LiFePO4电池的总反应为xMg2++2LiFePO4 xMg+2Li1-xFePO4+2xLi+,该电池的装置示意图如图所示。下列说法正确的是
xMg+2Li1-xFePO4+2xLi+,该电池的装置示意图如图所示。下列说法正确的是
 xMg+2Li1-xFePO4+2xLi+,该电池的装置示意图如图所示。下列说法正确的是
xMg+2Li1-xFePO4+2xLi+,该电池的装置示意图如图所示。下列说法正确的是
| A.放电时,Li+通过锂离子导体膜向Mg极移动 |
| B.充电时,阴极上的电极反应式为Mg2++2e-=Mg |
| C.可以用磷酸溶液代替非水电解质以提高电解质的导电效率 |
| D.若负极减少12g,则有NA个电子经电解质由负极流向正极 |
您最近一年使用:0次
2021-06-23更新
|
113次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题
解题方法
5 . 有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如下图所示:

(1)写出甲池中负极的电极反应式:_______ 。
(2)写出乙池中负极的电极材料和总反应的离子方程式:负极材料(化学式)_______ ;总反应的离子方程式_______ 。
(3)由此实验,可得到如下哪些正确结论_______ (填字母)。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析
(4)丙同学依据甲、乙同学的思路,设计如下实验:
将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池,在这两个原电池中,负极分别为_______ (填字母)。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片

(1)写出甲池中负极的电极反应式:
(2)写出乙池中负极的电极材料和总反应的离子方程式:负极材料(化学式)
(3)由此实验,可得到如下哪些正确结论
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析
(4)丙同学依据甲、乙同学的思路,设计如下实验:
将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
您最近一年使用:0次
6 . 下列叙述的方法不正确的是
| A.金属的电化学腐蚀比化学腐蚀更普遍 | B.用铝质铆钉焊接铁板,铁板易被腐蚀 |
| C.钢铁在干燥空气中不易被腐蚀 | D.在粗铜的电解精炼中纯铜做阴极 |
您最近一年使用:0次
2021-06-17更新
|
265次组卷
|
3卷引用:黑龙江省鹤岗市第一中学2020-2021学年高一6月月考化学试题
名校
解题方法
7 . 微生物燃料电池(MFC)以厌氧微生物催化氧化有机物(如葡萄糖),同时处理含Cu2+废水,装置如图所示,下列说法正确的是
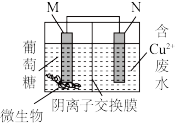

| A.N极发生氧化反应 |
| B.温度越高,反应速率越快,电池工作效率越高 |
| C.原电池中电子的移动方向是:M→导线→N→电解质溶液→M,阴离子移向M极 |
| D.N极的电极反应式:Cu2++2e-=Cu |
您最近一年使用:0次
2021-06-15更新
|
224次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高一6月月考化学试题
8 . 观察图示,回答问题:
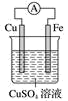
(1)负极是_______ ,电极反应式为_______ 。
(2)正极是_______ ,电极反应式为_______ 。
(3)电池总反应的离子方程式为_______ 。

(1)负极是
(2)正极是
(3)电池总反应的离子方程式为
您最近一年使用:0次
名校
9 . 一种“全氢电池”的工作原理如图所示。下列说法正确的是
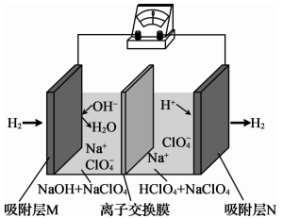

| A.电流方向是从吸附层M通过导线到吸附层N |
B.放电时,吸附层M发生的电极反应: |
C. 从右边穿过离子交换膜向左边移动 从右边穿过离子交换膜向左边移动 |
D.“全氢电池”放电时的总反应式为: |
您最近一年使用:0次
2021-05-30更新
|
1095次组卷
|
11卷引用:黑龙江省哈尔滨市第一中学校 2021-2022学年高三上学期期末考试理综化学试题
黑龙江省哈尔滨市第一中学校 2021-2022学年高三上学期期末考试理综化学试题 黑龙江省哈尔滨市德强学校2022-2023学年高三上学期10月月考化学试题天津市部分区2021届高三质量调查(二模)化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期期末考试化学试题(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省长沙市雅礼中学2021-2022学年高三上学期第四次月考化学试题 (已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习山东省德州市第一中学2021-2022学年高二12月月考化学试题内蒙古莫力达瓦旗尼尔基第一中学2021-2022学年高三上学期期末考试化学试题湖北省2022-2023学年高三上学期期末考试化学试题天津市静海区第一中学2020-2021学年高三下学期第三次模拟考试化学试题
名校
10 . 某化学兴趣小组的几位同学探究原电池原理的应用时,做了如图的实验:
I.原电池原理判断金属的活泼性
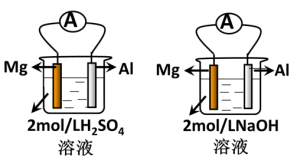
(1)实验前,甲同学认为“构成原电池的负极总是较活泼的金属材料”,若根据他的判断,两个装置中的Al都是___ 极;实际实验时发现两个装置中的电流表偏转方向不同,则以下的有关中判断正确的是___ 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件影响较大,故应具体问题具体分析
(2)乙同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是___ 。
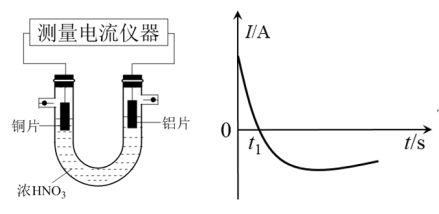
II.铜与浓硝酸反应探究
(3)乙同学又将铜片直接放入浓硝酸中:
①实验现象为___ ,溶液显绿色。
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是___ (用离子方程式表示)。
(4)电化学降解NO 的原理如题图所示。
的原理如题图所示。
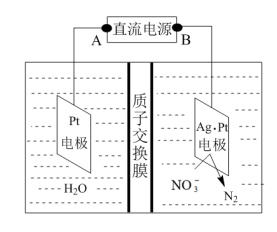
电源正极为___ (填“A”或“B”),阳极的电极反应式为___ 。
I.原电池原理判断金属的活泼性

(1)实验前,甲同学认为“构成原电池的负极总是较活泼的金属材料”,若根据他的判断,两个装置中的Al都是
A.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件影响较大,故应具体问题具体分析
(2)乙同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是

II.铜与浓硝酸反应探究
(3)乙同学又将铜片直接放入浓硝酸中:
①实验现象为
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是
(4)电化学降解NO
 的原理如题图所示。
的原理如题图所示。
电源正极为
您最近一年使用:0次
2021-05-27更新
|
276次组卷
|
2卷引用:黑龙江省大庆市铁人中学2020-2021学年高一下学期期中考试化学试题



