名校
解题方法
1 . 一种新型微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,下列说法正确的是。
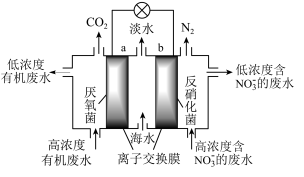
| A.该电池能在高温下工作 |
| B.a极为电池的正极 |
| C.有机废水处理后pH降低 |
D.处理 的电极反应为 的电极反应为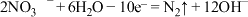 |
您最近半年使用:0次
名校
解题方法
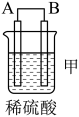
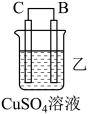
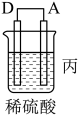
2 . 化学能还可以转化为电能,由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)外电路中电流由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)外电路中电流由
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近半年使用:0次
名校
解题方法
3 . 下列说法正确的是
A.过量的 使紫色石蕊试液先变红后褪色,说明 使紫色石蕊试液先变红后褪色,说明 具有酸性和漂白性 具有酸性和漂白性 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸具有不稳定性 |
| C.向金属铜与浓硫酸反应后混合液中直接加入蒸馏水,变蓝色证明混合液中含有铜离子 |
| D.纯锌与稀硫酸反应制氢气比粗锌慢,因为粗锌中含有比锌稳定的金属杂质使锌作正极 |
您最近半年使用:0次
4 . 离子液体是指在室温或接近室温下呈现液态的、完全由阴阳离子所组成的盐,也称为低温熔融盐。一种以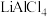 离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是
离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是
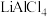 离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是
离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是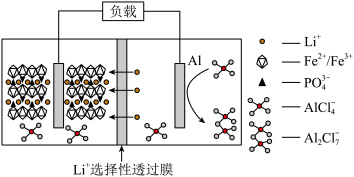
A.充电时,阳极的电极反应式为 |
| B.放电时,磷酸铁锂电极中锂元素被氧化 |
C.放电时,铝为负极,其电极反应式为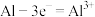 |
| D.充电时,电子由Al电极经离子液体流向磷酸铁锂电极 |
您最近半年使用:0次
5 . 某化学小组为了探究铝电极在原电池中的作用,进行了下列实验,实验结果记录如表。下列说法正确的是
编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
① | Mg、Al | 稀盐酸 | 偏向Al |
② | Al、Cu | 稀盐酸 | 偏向Cu |
③ | Al、石墨 | 稀盐酸 | 偏向________ |
④ | Mg、Al | NaOH溶液 | 偏向Mg |
| A.实验①和②中,Al电极的作用相同 |
| B.实验③中,电流表指针偏向A1 |
C.实验④中,Mg为负极,电极反应式为: |
| D.以上实验说明,铝在原电池中的作用,与另一个电极材料和电解质溶液有关 |
您最近半年使用:0次
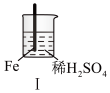
6 . Fe和Mg与硫酸反应的实验如下,下列说法正确的是
| 实验 |
|
|
|
|
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
| A.I中产生气体的原因是:2Fe+6H+=2Fe3++3H2 |
| B.取出Ⅱ中的铁棒插入硫酸铜溶液中立即析出红色金属 |
| C.实验Ⅲ中产生的气体主要是氢气 |
| D.实验Ⅳ能证明Mg的金属性强于Fe |
您最近半年使用:0次
7 . 某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粒(假设溶液体积不变),用排水集气法收集反应放出的氢气,实验记录如下(累计值):
下列说法错误的是
时间t/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL(标准状况) | 105 | 217 | 334 | 410 | 476 |
A.1~2min内,用盐酸的浓度变化表示的平均反应速率为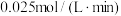 |
B.化学反应速率最大时间段为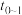 |
| C.根据以上实验数据可以判定该反应为放热反应 |
D.反应开始时,向盐酸中滴加少量的 溶液,相同时间内产生氢气的体积比未加 溶液,相同时间内产生氢气的体积比未加 溶液时大 溶液时大 |
您最近半年使用:0次
8 . 某化学小组探究 浓硝酸原电池中硝酸浓度对“电极反转”的影响,将规格完全相同的Cu片和Fe片插入9.4
浓硝酸原电池中硝酸浓度对“电极反转”的影响,将规格完全相同的Cu片和Fe片插入9.4 、13.3
、13.3 、13.4
、13.4 、13.7
、13.7 、15.0
、15.0 的硝酸溶液中,组成原电池测试电流变化如图所示。已知:
的硝酸溶液中,组成原电池测试电流变化如图所示。已知: 氧化层比
氧化层比 更致密。
更致密。
 浓硝酸原电池中硝酸浓度对“电极反转”的影响,将规格完全相同的Cu片和Fe片插入9.4
浓硝酸原电池中硝酸浓度对“电极反转”的影响,将规格完全相同的Cu片和Fe片插入9.4 、13.3
、13.3 、13.4
、13.4 、13.7
、13.7 、15.0
、15.0 的硝酸溶液中,组成原电池测试电流变化如图所示。已知:
的硝酸溶液中,组成原电池测试电流变化如图所示。已知: 氧化层比
氧化层比 更致密。
更致密。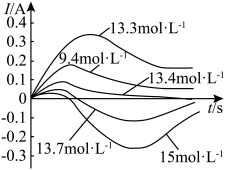
| A.初始阶段,铁做负极 |
B.15 的硝酸溶液中,一段时间后,发生“电极反转” 的硝酸溶液中,一段时间后,发生“电极反转” |
C.硝酸浓度小于13.3 时,硝酸浓度越小,电流强度越大 时,硝酸浓度越小,电流强度越大 |
D.将Fe换为Al后,测得“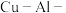 硝酸”原电池电极反转的硝酸溶液浓度的临界值为9.1 硝酸”原电池电极反转的硝酸溶液浓度的临界值为9.1 ,工业上用铝罐储存硝酸更合适 ,工业上用铝罐储存硝酸更合适 |
您最近半年使用:0次
9 . 航母山东舰采用模块制造再焊接组装而成。实验室模拟海水和淡水对焊接金属材料的影响,结果如图所示。下列分析正确的是
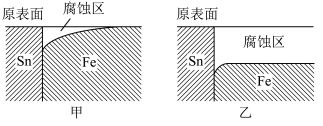
| A.舰艇腐蚀是因为形成了电解池 | B.图甲是海水环境下的腐蚀情况 |
C.腐蚀时负极反应为: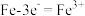 | D.焊点附近可用锌块打“补丁”延缓腐蚀 |
您最近半年使用:0次
名校
解题方法
10 . LiH是制备有机合成的重要还原剂LiAlH4的反应物,氢化锂遇水蒸气剧烈反应。某小组设计如图所示装置制备LiH:
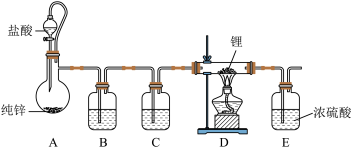
| A.装置B中盛装浓硫酸 |
| B.装置A中加入少量硫酸铜,可加快反应速率 |
| C.装置E用于吸收尾气,避免污染环境 |
| D.实验中,先点燃酒精灯,再通入H2 |
您最近半年使用:0次