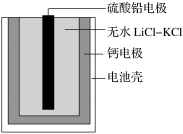
1 . 热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是

| A.正极反应式:Ca+2Cl--2e-=CaCl2 |
| B.放电过程中,Li+向正极移动 |
| C.每转移0.1mol电子,理论上生成20.7gPb |
| D.常温时,在正、负极间接上电流表或检流计,指针不偏转 |
您最近一年使用:0次
名校
2 . 某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+8H2O+5Fe2(SO4)3+K2SO4设计如下原电池,盐桥中装有饱和K2SO4琼脂溶液,其阴、阳离子可向甲、乙做定向移动,从而把甲、乙连接以形成闭合回路,形成原电池。下列说法正确的是


A.a电极上发生的反应为: +8H++5e﹣═Mn2++4H2O +8H++5e﹣═Mn2++4H2O |
| B.外电路电子的流向是从a到b |
C.电池工作时,盐桥中的 移向甲烧杯 移向甲烧杯 |
| D.b电极上发生氧化反应 |
您最近一年使用:0次
解题方法
3 . 化学家正在研究尿素燃料电池,尿素燃料电池结构如图所示,用这种电池直接去除城市废水中的尿素,下列有关描述正确的是


| A.甲电极为电池的正极 |
B.乙电极的电极反应式为: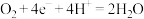 |
| C.电池工作时氢离子向甲电极移动 |
D.D.电池工作时,理论上净化1mol 消耗标准状况下33.6L 消耗标准状况下33.6L 浓度的废水 浓度的废水 |
您最近一年使用:0次
名校
解题方法
4 . 常温下对于任一电池反应 ,其电动势
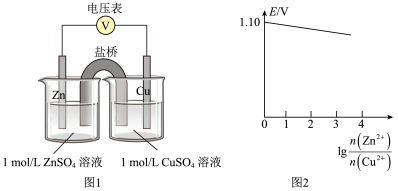
,其电动势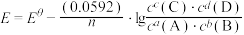 ,n为电池反应中转移的电子数。某同学设计装置(如图1),以Zn―Cu原电池探究离子浓度的改变对电极电势的影响。测得初始时
,n为电池反应中转移的电子数。某同学设计装置(如图1),以Zn―Cu原电池探究离子浓度的改变对电极电势的影响。测得初始时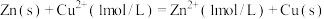 ,
,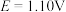 (该反应
(该反应 ),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
 ,其电动势
,其电动势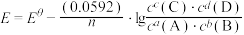 ,n为电池反应中转移的电子数。某同学设计装置(如图1),以Zn―Cu原电池探究离子浓度的改变对电极电势的影响。测得初始时
,n为电池反应中转移的电子数。某同学设计装置(如图1),以Zn―Cu原电池探究离子浓度的改变对电极电势的影响。测得初始时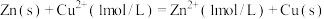 ,
,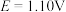 (该反应
(该反应 ),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
| A.盐桥中通常装有含KCl饱和溶液的琼脂,离子可在其中自由移动 |
B.推测图2中直线与x轴的交点坐标大约为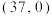 |
C.向盛有2mL 1mol/L 溶液的试管中滴加5滴1mol/L 溶液的试管中滴加5滴1mol/L 溶液,有白色沉淀产生,再向其中滴加5滴1mol/L 溶液,有白色沉淀产生,再向其中滴加5滴1mol/L 溶液产生黑色沉淀,则可知: 溶液产生黑色沉淀,则可知: |
| D.某同学用铜丝代替图1中的盐桥,也能检测到电流,推测一段时间后铜丝质量不变 |
您最近一年使用:0次
解题方法
5 . 下列有关四个常用电化学装置的叙述中,正确的是
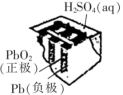 | 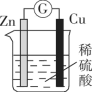 | 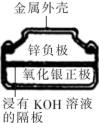 | 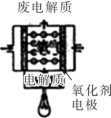 |
| ①铅蓄电池 | ②铜锌原电池 | ③银锌纽扣电池 | ④氢氧燃料电池 |
| A.图①所示电池放电过程中,负极的质量不断增大 |
| B.图②所示电池放电过程中,电解质溶液的质量不断减小 |
C.图③所示电池工作过程中,电子由 极流向 极流向 极 极 |
D.图④所示电池的正极反应式一定是 |
您最近一年使用:0次
6 . 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是
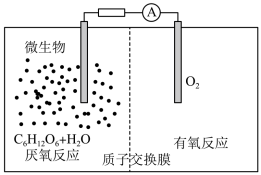

| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从正极区移向负极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
您最近一年使用:0次
解题方法
7 . 镁H2O2酸性电池采用海水作电解质溶液(加入一定量的酸),下列说法正确的是
| A.电池总反应的离子方程式为Mg+H2O2+2H+=Mg2++2H2O |
| B.负极的电极反应为H2O2+2H++2e-=2H2O |
| C.工作时,正极周围海水的pH增大 |
| D.电池工作时,溶液中的H+向负极移动 |
您最近一年使用:0次
名校
解题方法
8 . 某反应中反应物与生成物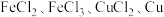 ,将上述反应设计成的原电池如图甲所示、设计成电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,下列判断正确的是
,将上述反应设计成的原电池如图甲所示、设计成电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,下列判断正确的是
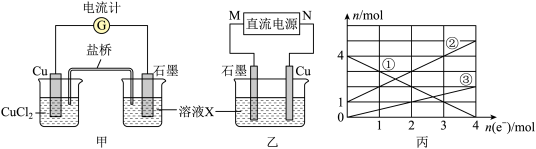
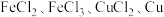 ,将上述反应设计成的原电池如图甲所示、设计成电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,下列判断正确的是
,将上述反应设计成的原电池如图甲所示、设计成电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,下列判断正确的是
A.图中X溶液是 |
B.原电池工作时,盐桥中的 不断进入X溶液中 不断进入X溶液中 |
C.图丙中的③线是 的变化 的变化 |
D.甲乙两装置中的 电极上均发生氧化反应 电极上均发生氧化反应 |
您最近一年使用:0次
名校
解题方法
9 . 一个由锌片和石墨棒作为电极的原电池,电极反应如下,下列说法错误的是
锌片: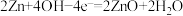 ,石墨:
,石墨: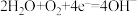
锌片:
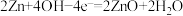 ,石墨:
,石墨: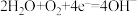
| A.电子从石墨经外电路流向锌片 |
B.该原电池工作一段时间后正极区附近溶液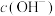 增大 增大 |
C.电极总反应为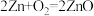 |
| D.原电池放电时,负极上发生反应的物质是Zn,发生还原反应 |
您最近一年使用:0次
2022-10-19更新
|
160次组卷
|
2卷引用:河北省石家庄实验中学2022-2023学年高二上学期10月月考化学试题
名校
10 . 下列有关说法中错误的是
| A.实现在铜的表面镀上一层银,与电源负极相连的应为银电极 |
| B.原电池中电子从负极出发,经外电路流向正极,再从正极经电解液回到负极 |
C.常温下用镁和铝作电极, 溶液作电解质溶液的原电池中铝为负极 溶液作电解质溶液的原电池中铝为负极 |
D.甲烷燃料电池用 作电解质,负极的电极反应式为 作电解质,负极的电极反应式为 |
您最近一年使用:0次



