2023高三·全国·专题练习
名校
解题方法
1 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
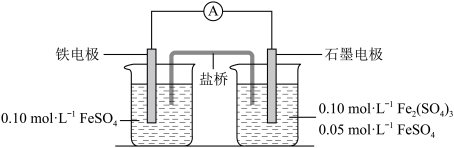
回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为___________________ ,铁电极的电极反应式为_______________________________ 。因此,验证了Fe2+氧化性小于________ 、还原性小于________ 。

回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次
名校
解题方法
2 . 某实验小组同学进行如下实验:
(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是__ (填序号)。

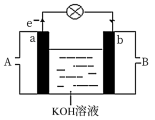
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中__ (填A或B)处电极入口通甲烷,该原电池的正极电极反应式为___ 。当消耗标况下甲烷33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量__ mol。
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
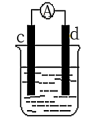
①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸,写出该原电池正极的电极反应式为___ 。
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为__ ;该原电池的负极反应式为___ 。
(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中

(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸,写出该原电池正极的电极反应式为
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为
您最近一年使用:0次
3 . 已知 的氧化性大于
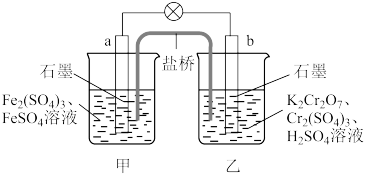
的氧化性大于 。根据如图所示装置可构成原电池(盐桥中装有含琼脂的饱和
。根据如图所示装置可构成原电池(盐桥中装有含琼脂的饱和 溶液),下列叙述错误的是
溶液),下列叙述错误的是
 的氧化性大于
的氧化性大于 。根据如图所示装置可构成原电池(盐桥中装有含琼脂的饱和
。根据如图所示装置可构成原电池(盐桥中装有含琼脂的饱和 溶液),下列叙述错误的是
溶液),下列叙述错误的是
| A.a为原电池的负极,b为原电池的正极 |
B.电池工作时,盐桥中的 移向甲烧杯 移向甲烧杯 |
C.a极的电极反应式为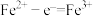 |
D.工作一段时间后,乙烧杯中溶液的 减小(忽略溶液体积变化) 减小(忽略溶液体积变化) |
您最近一年使用:0次
2022-10-27更新
|
360次组卷
|
2卷引用:海南省2022-2023学年高三上学期高考全真模拟卷(二)化学试题



