解题方法
1 . Ⅰ中和热的测定:测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
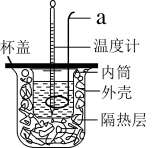
(1)仪器a的名称为_______ ,实验中还需要用到的玻璃仪器是_______ 。
(2)用相同浓度和体积的氨水代替 溶液进行上述实验,测得的中和热数值会偏小,原因为
溶液进行上述实验,测得的中和热数值会偏小,原因为_______ 。
Ⅱ.在试管中进行溶液间反应时,同学们无法观察到 转化为
转化为 ,于是又设计了如下实验(电压表读数:
,于是又设计了如下实验(电压表读数: )。
)。
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
(3)步骤ⅰ中,B中石墨上的电极反应式是_______ 。
(4)结合信息,解释实验步骤ⅳ中 的原因
的原因_______ 。
(5)能说明 转化为
转化为 的实验现象是
的实验现象是_______ 。

(1)仪器a的名称为
(2)用相同浓度和体积的氨水代替
 溶液进行上述实验,测得的中和热数值会偏小,原因为
溶液进行上述实验,测得的中和热数值会偏小,原因为Ⅱ.在试管中进行溶液间反应时,同学们无法观察到
 转化为
转化为 ,于是又设计了如下实验(电压表读数:
,于是又设计了如下实验(电压表读数: )。
)。| 装置 | 步骤 | 电压表读数 |
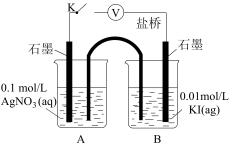 | ⅰ.如图连接装置并加入试剂,闭合K | a |
ⅱ.向B中滴入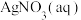 ,至沉淀完全 ,至沉淀完全 | b | |
ⅲ.再向B中投入一定量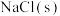 | c | |
ⅳ.重复ⅰ,再向B中加入与ⅲ等量 | a |
(3)步骤ⅰ中,B中石墨上的电极反应式是
(4)结合信息,解释实验步骤ⅳ中
 的原因
的原因(5)能说明
 转化为
转化为 的实验现象是
的实验现象是
您最近半年使用:0次
解题方法
2 . ORP传感器(如下图)测定物质的氧化性的原理:将Pt电极插入待测溶液中,Pt电极、Ag/AgCl电极与待测溶液组成原电池,测得的电压越高,溶液的氧化性越强。向NaIO3溶液、FeCl3溶液中分别滴加2滴H2SO4溶液,测得前者的电压增大,后者的几乎不变。
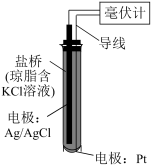
下列说法不正确 的是

下列说法
| A.盐桥中的Cl-移向Ag/AgCl电极 |
| B.Ag/AgCl电极反应是Ag-e-+Cl-=AgCl |
C.酸性越强, 的氧化性越强 的氧化性越强 |
| D.向FeCl3溶液中滴加浓NaOH溶液至碱性,测得电压几乎不变 |
您最近半年使用:0次
名校
解题方法
3 . 含氮化合物种类多,用途广。回答下列问题。
(1)NH3的电子式为__________ ,NH3与NaClO在一定条件下可生成N2H4,化学方程式为__________ 。
(2) 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为__________ 。
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是__________ 。
③从分子结构角度分析,N2H4不如氨气稳定的原因是__________ 。
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则 =
=__________ (常温下NH3·H2O的电离平衡常数为 )。
)。
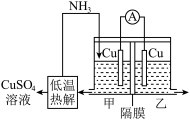
(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体__________ 。
(1)NH3的电子式为
(2)
 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是
 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是③从分子结构角度分析,N2H4不如氨气稳定的原因是
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则
 =
= )。
)。(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。

| A.甲室Cu电极为负极 |
| B.Cu2+通过隔膜进入乙室 |
| C.电池总反应为:Cu2++4NH3=[Cu(NH3)4]2+ |
| D.NH3扩散到乙室不会对电池电压产生影响 |
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体
您最近半年使用:0次
2023高三·全国·专题练习
名校
解题方法
4 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
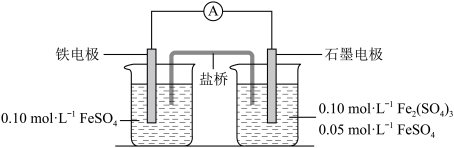
回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为___________________ ,铁电极的电极反应式为_______________________________ 。因此,验证了Fe2+氧化性小于________ 、还原性小于________ 。

回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为
您最近半年使用:0次
名校
解题方法
5 . 现有M、N、P、E四种金属,已知:①氧化性强弱顺序为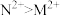 ;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为
;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为 ,
, 。则这四种金属的还原性由强到弱的顺序是
。则这四种金属的还原性由强到弱的顺序是
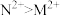 ;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为
;②E、P用导线连接放入稀硫酸中,P表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为 ,
, 。则这四种金属的还原性由强到弱的顺序是
。则这四种金属的还原性由强到弱的顺序是A.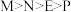 | B. |
C. | D.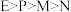 |
您最近半年使用:0次
2022-09-11更新
|
173次组卷
|
2卷引用:甘肃省白银市会宁县2021-2022学年高二上学期期末质量检测化学试题
名校
解题方法
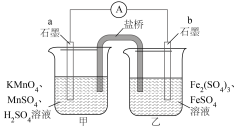
6 . 已知氧化性 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
| A.a为电池的负极,b为电池的正极 |
| B.电流从a经过外电路流向b |
C.电池工作时,盐桥中的 移向乙烧杯 移向乙烧杯 |
D.A电极上发生的反应为: +8H++5e- = Mn2++4H2O +8H++5e- = Mn2++4H2O |
您最近半年使用:0次
名校
解题方法
7 . 羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是
的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是

 )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是
的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是
A.a极每 参与反应,有 参与反应,有 移向氯化钠溶液 移向氯化钠溶液 |
| B.相同条件下,电极b与c产生气体的体积比为7:3 |
| C.电极c为阴极,发生还原反应 |
D.d极区苯酚被氧化的化学方程式为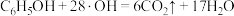 |
您最近半年使用:0次
名校
解题方法
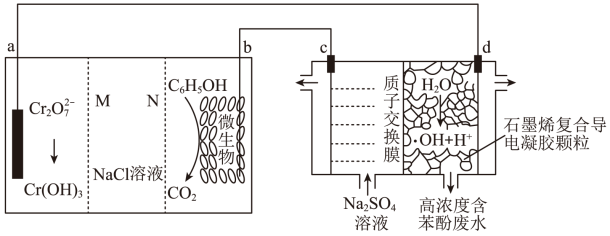
8 . 我国科学家设计了一种利用废水中的 将苯酚氧化为
将苯酚氧化为 和
和 的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基(
的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基( )的氧化性仅次于氟气。下列说法正确的是
)的氧化性仅次于氟气。下列说法正确的是
 将苯酚氧化为
将苯酚氧化为 和
和 的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基(
的原电池—电解池组合装置(如图),实现了发电、环保二位一体。已知:羟基自由基( )的氧化性仅次于氟气。下列说法正确的是
)的氧化性仅次于氟气。下列说法正确的是
| A.电子转移方向:c电极→导线→b电极 |
B.d电极的电极反应为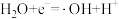 |
C.右侧装置中,c、d两电极产生气体的体积比(相同条件下)为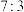 |
D.若a电极上有 参与反应,理论上 参与反应,理论上 溶液中有 溶液中有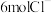 通过阴离子膜进入a电极区溶液 通过阴离子膜进入a电极区溶液 |
您最近半年使用:0次
2023-05-04更新
|
299次组卷
|
2卷引用:河北省石家庄部分重点高中2022-2023学年高三下学期3月月考化学试题
名校
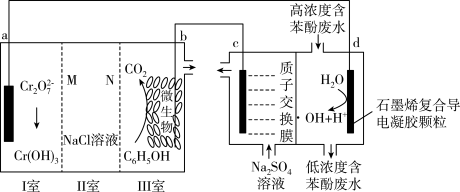
9 . 羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
 )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
| A.a极为正极,c极为阴极 |
B.a极区每产生1mol ,c极区溶液质量减轻3g ,c极区溶液质量减轻3g |
C.d极的电极反应式为 |
D.工作时,如果II室中 、 、 数目都减小,则N为阴离子交换膜 数目都减小,则N为阴离子交换膜 |
您最近半年使用:0次
2022-12-24更新
|
695次组卷
|
4卷引用:广东省部分学校2022-2023学年高三上学期12月大联考化学试题
广东省部分学校2022-2023学年高三上学期12月大联考化学试题河北省衡水市2022-2023学年高三上学期12月份大联考化学试卷辽宁省沈阳市第二中学2022-2023学年高三上学期期末考试化学试题 (已下线)专题一 原电池的工作原理及其应用(练习)
名校
解题方法
10 . Ⅰ.回答下列问题
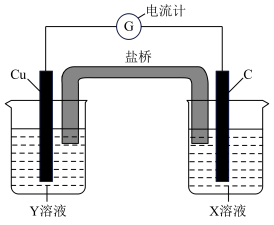
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:
①写出电极反应式。正极:_______ ;负极:_______ 。
②图中X溶液的溶质是_______ (填化学式,下同),Y溶液的溶质是_______ 。
③原电池工作时,盐桥中的_______ (填“阳”或“阴”)离子向X溶液方向移动。
(2)控制合适的条件将反应2Fe3++2I-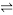 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:

①反应开始时,乙中石墨电极上发生_______ (填“氧化”或“还原”,下同)反应,电极反应式为_______ 。甲中石墨电极上发生_______ 反应,电极反应式为_______ 。
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作_______ (填“正”或“负”)极,该电极的电极反应式为_______ 。
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_______ 。
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式_______ 。实验结果未见到蓝色。
(5)乙同学认为甲同学的实验方案有问题,理由是_______ 。请设计原电池证明Ag+也能氧化 Iˉ,画出装置图,并标明电极材料及电解质溶液。______
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:

①写出电极反应式。正极:
②图中X溶液的溶质是
③原电池工作时,盐桥中的
(2)控制合适的条件将反应2Fe3++2I-
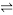 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:
①反应开始时,乙中石墨电极上发生
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式
(5)乙同学认为甲同学的实验方案有问题,理由是
您最近半年使用:0次



