名校
解题方法
1 . CH3OH、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
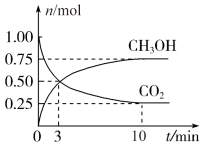
①从反应开始到平衡,CO2的平均反应速率v(CO2)=____ 。
②达到平衡时,H2的浓度为____ mol/L。
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是____ 。
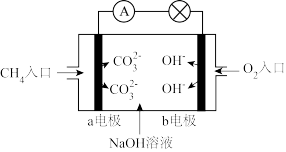
(3)某种甲烷燃料电池的工作原理如图所示氧气通入的一极为电源的____ 极,a电极反应式:____ ,b电极反应式:____ 。
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)____ L。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是| A.反应中CO与CH3OH的物质的量之比为1:1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)

您最近半年使用:0次
2022-05-12更新
|
429次组卷
|
3卷引用:河南省南阳市2021-2022学年高一下学期期中质量评估化学试题
名校
解题方法
2 . 某课题研究小组设计如图所示装置(电极材料均为Pt),该装置可将工业废水中的乙胺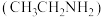 转化为无毒无害物质。下列分析错误的是
转化为无毒无害物质。下列分析错误的是
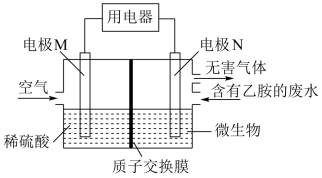
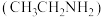 转化为无毒无害物质。下列分析错误的是
转化为无毒无害物质。下列分析错误的是 
| A.电极N为电池的负极 |
B.电池工作时, 由M极区通过交换膜移动到N极区 由M极区通过交换膜移动到N极区 |
C.电极N的电极反应式为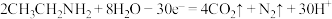 |
| D.当空气(含氧气20%)的进入量为7.5mol时,可以处理含乙胺(质量分数为9%)的废水0.2kg |
您最近半年使用:0次
解题方法
3 . 如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(1)通入氧气的电极为_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
(2)铁电极为_______ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减小”或“不变”)
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为_______ (用 为阿伏加德罗常数的值表示)。
为阿伏加德罗常数的值表示)。
(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
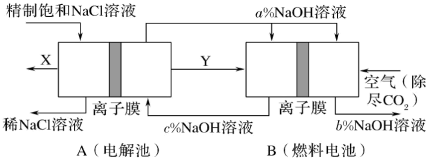
分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
 为阿伏加德罗常数的值表示)。
为阿伏加德罗常数的值表示)。(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

分析图可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近半年使用:0次
解题方法
4 . 如图是一套电化学实验装置,图中C、D均为铂电极,G是灵敏电流计,其指针总是偏向电源正极。回答下列问题:
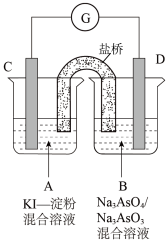
(1)向烧杯B中加入适量较浓的硫酸,发现G的指针向右偏移。则电极C是原电池的_______ (填“正极”或“负极”),电极C上的电极反应式为_______ ,烧杯A中的主要实验现象是_______ 。
(2)一段时间后,再向烧杯B中加入适量质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总反应的离子方程式为 ,此时电极D为
,此时电极D为_______ (填“正极”或“负极”),其电极反应方程式为_______ 。
(3)再过一段时间后,实验装置中的化学反应已经达到化学平衡状态,则此时G的指针指向_______ (填“右边”“左边”或“0刻度”),理由是_______ 。

(1)向烧杯B中加入适量较浓的硫酸,发现G的指针向右偏移。则电极C是原电池的
(2)一段时间后,再向烧杯B中加入适量质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总反应的离子方程式为
 ,此时电极D为
,此时电极D为(3)再过一段时间后,实验装置中的化学反应已经达到化学平衡状态,则此时G的指针指向
您最近半年使用:0次
名校
解题方法
5 . SO2可形成酸雨,是大气污染物。利用如图装置既可以吸收工厂排放的SO2又可以制得硫酸溶液。下列说法正确的是


| A.a极为负极,发生还原反应 |
B.b极的电极反应式为 |
| C.电子的流动方向:a极→电解质溶液→b极 |
| D.从左下口流出的硫酸溶液的质量分数一定大于50% |
您最近半年使用:0次
2023-07-11更新
|
298次组卷
|
5卷引用:广东省清远市2022-2023学年高一下学期期末质量检测化学试题
名校
6 . 水体中氨氮含量过高会造成水体富营养化。利用微生物燃料电池可以对废水中氨氮进行处理的装置如图,两极材料均为石墨棒,下列说法正确的是
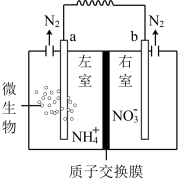

| A.a极表面发生还原反应 |
B.工作时 通过质子交换膜移向左室 通过质子交换膜移向左室 |
C.标准状况下,每转移 电子,负极生成 电子,负极生成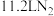 ,且左室 ,且左室 降低 降低 |
D.正极电极反应式为: |
您最近半年使用:0次
解题方法
7 . 某甲烷燃料电池的构造如图所示,a、b为电极,C、D为选择性离子交换膜,只允许一种离子通过。下列说法正确的是
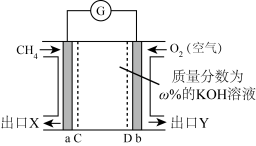

| A.b是电池负极 |
| B.电流由b沿导线流向a,再由a通过电解质溶液流回b |
| C.出口Y中KOH的质量分数小于ω% |
| D.a电极的电极反应式为:CH4−8e-+8OH-=CO2+6H2O |
您最近半年使用:0次
解题方法
8 . 钇稳定氧化锆浓差电池可用于测定待测环境中氧气的含量,在冶金、能源等领域应用广泛。其原理是利用空气与待测环境中氧气的浓度差对电压的影响,某工作状态如图所示。该电池工作时,下列说法不正确的是
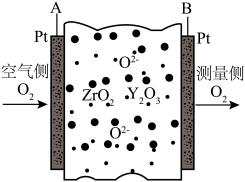

| A.电极A为正极 | B.O2-由电极A向电极B迁移 |
C.电极B发生的反应为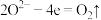 | D.理论上,电解质中O2-的总物质的量会增加 |
您最近半年使用:0次
解题方法
9 . 一种基于原电池原理的氧气传感器可用于测定样气中氧气的含量,其装置如图所示。下列说法正确的是
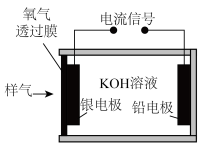
| A.铅电极为正极 |
B.银电极上发生的反应为 |
| C.电子由铅电极经过KOH溶液流向银电极 |
| D.工作过程中,传感器的质量不变 |
您最近半年使用:0次
名校
解题方法
10 . 任何化学反应都伴随着能量的变化,通过化学反应,化学能可以与热能、电能等不同形式的能量相互转化,用于生产、生活和科研。请回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋利用_____ (填“放热”或“吸热”)的化学变化或物理变化的原理。
(2)世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最。光伏电池能将_____ 直接转变为电能(填:“化学能”“太阳能”“热能”等)
(3)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过氨热分解法制氢气。相关化学键的键能数据
一定温度下,利用催化剂将 分解为
分解为 和3 mol
和3 mol  ,吸收90.8 kJ热量,则
,吸收90.8 kJ热量,则
_____ 。
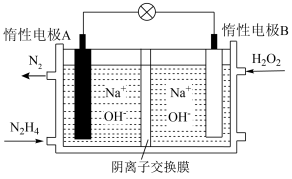
(4)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“ ”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液
”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液_____ 。______ (填“正”或“负”)极,其电极反应式为_____ 。
②电池工作过程中,若A极区产生14 g ,则转移的电子数目为
,则转移的电子数目为______ 。
③有人提出可用甲烷去替代肼,此时惰性电极A发生的电极反应式为______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋利用
(2)世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最。光伏电池能将
(3)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过氨热分解法制氢气。相关化学键的键能数据
| 化学键 |  |  |  |
键能E/(kJ·mol ) ) | 946.0 | a | 390.8 |
 分解为
分解为 和3 mol
和3 mol  ,吸收90.8 kJ热量,则
,吸收90.8 kJ热量,则
(4)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“
 ”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液
”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液
②电池工作过程中,若A极区产生14 g
 ,则转移的电子数目为
,则转移的电子数目为③有人提出可用甲烷去替代肼,此时惰性电极A发生的电极反应式为
您最近半年使用:0次
2024-05-04更新
|
487次组卷
|
2卷引用:广东省深圳市翠园中学、龙城高级中学2023-2024学年高一下学期第一次月考化学试题



