名校
1 . 羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
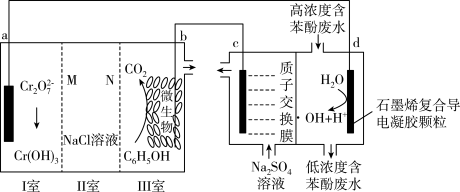
和 的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
 )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
的原电池-电解池组合装置(如图所示),该装置能实现发电、环保二位一体。下列说法错误的是
| A.a极为正极,c极为阴极 |
B.a极区每产生1mol ,c极区溶液质量减轻3g ,c极区溶液质量减轻3g |
C.d极的电极反应式为 |
D.工作时,如果II室中 、 、 数目都减小,则N为阴离子交换膜 数目都减小,则N为阴离子交换膜 |
您最近一年使用:0次
2022-12-24更新
|
698次组卷
|
4卷引用:广东省部分学校2022-2023学年高三上学期12月大联考化学试题
广东省部分学校2022-2023学年高三上学期12月大联考化学试题河北省衡水市2022-2023学年高三上学期12月份大联考化学试卷辽宁省沈阳市第二中学2022-2023学年高三上学期期末考试化学试题 (已下线)专题一 原电池的工作原理及其应用(练习)
名校
2 . 电池的应用给我们的生活带来了很多便利,请根据原电池工作原理回答下列问题:
(1)现有如下两个反应:①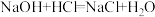 ②
② 。根据两反应本质,判断能设计成原电池的反应是
。根据两反应本质,判断能设计成原电池的反应是_______ (填序号)。该电池的正极材料是_______ 。
(2)锌锰干电池是最早使用的化学电池,其基本构造如图1所示:电路中每通过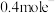 ,负极质量减少
,负极质量减少_______ g;工作时 在正极放电产生两种气体,其中一种气体分子是
在正极放电产生两种气体,其中一种气体分子是 的微粒,正极的电极反应式是
的微粒,正极的电极反应式是_______ 。
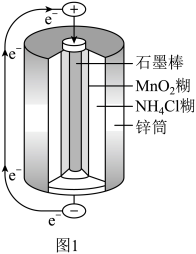
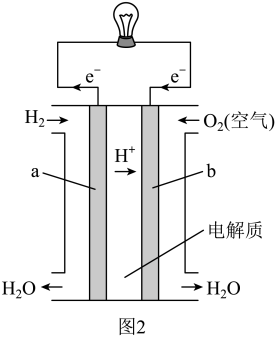
(3)图2为氢氧燃料电池原理示意图。该燃料电池正极的电极反应式_______ 。若导线中通过 个电子,负极消耗气体的体积为
个电子,负极消耗气体的体积为_______ (标况下)。
(4)直接乙醇燃料电池( )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。
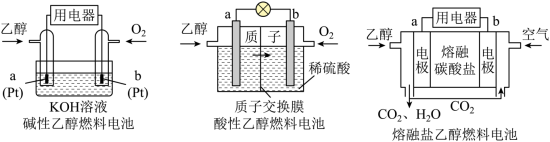
①碱性乙醇燃料电池中,电极a上发生的电极反应式为_______ 。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为_______ 。
③熔融碳酸盐乙醇燃料电池中,电极a上发生的电极反应式为_______ 。
(1)现有如下两个反应:①
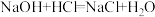 ②
② 。根据两反应本质,判断能设计成原电池的反应是
。根据两反应本质,判断能设计成原电池的反应是(2)锌锰干电池是最早使用的化学电池,其基本构造如图1所示:电路中每通过
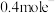 ,负极质量减少
,负极质量减少 在正极放电产生两种气体,其中一种气体分子是
在正极放电产生两种气体,其中一种气体分子是 的微粒,正极的电极反应式是
的微粒,正极的电极反应式是
(3)图2为氢氧燃料电池原理示意图。该燃料电池正极的电极反应式
 个电子,负极消耗气体的体积为
个电子,负极消耗气体的体积为
(4)直接乙醇燃料电池(
 )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。
①碱性乙醇燃料电池中,电极a上发生的电极反应式为
②酸性乙醇燃料电池中,电极a上发生的电极反应式为
③熔融碳酸盐乙醇燃料电池中,电极a上发生的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 某实验小组同学进行如下实验:
(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是__ (填序号)。

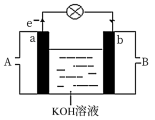
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中__ (填A或B)处电极入口通甲烷,该原电池的正极电极反应式为___ 。当消耗标况下甲烷33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量__ mol。
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
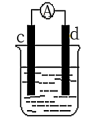
①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸,写出该原电池正极的电极反应式为___ 。
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为__ ;该原电池的负极反应式为___ 。
(1)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中

(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸,写出该原电池正极的电极反应式为
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为
您最近一年使用:0次
22-23高一下·广东深圳·期中
名校
4 . 电池是人类生产和生活中的重要能量来源。人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。
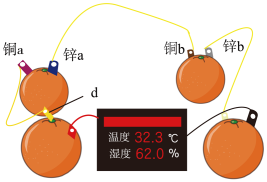
(1)知识源于实践。学习原电池知识后,某学习小组以 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是_______(填字母)。
(3)将 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
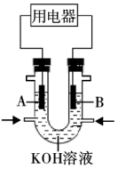
实验测得电子定向移向 电极,则
电极,则_______ (填“ ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为_______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: ,请回答下列问题:
,请回答下列问题:
①放电时,正极反应式为_______ 。
②放电时,负极附近溶液的碱性_______ 。(填“增强”或“减弱”)
(5) 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
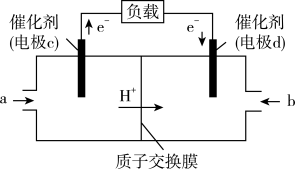
电池总反应为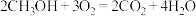 ,则
,则 电极反应式为
电极反应式为_______ ,若线路中转移 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为_______  。
。
(1)知识源于实践。学习原电池知识后,某学习小组以
 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
A.每个水果果汁中的 移向正极 移向正极 |
B.锌 、 、 发生的电极反应式为 发生的电极反应式为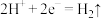 |
C.四个水果电池串联,则电极 为铜片 为铜片 |
D.铜 为电池正极,发生氧化反应 为电池正极,发生氧化反应 |
| A.锌锰电池工作一段时间后碳棒会变细 |
| B.氢氧燃料电池具有高效的特点,能量转化率可达100% |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
D.铅蓄电池负极是 ,正极是 ,正极是 |
 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
实验测得电子定向移向
 电极,则
电极,则 ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
 ,请回答下列问题:
,请回答下列问题:①放电时,正极反应式为
②放电时,负极附近溶液的碱性
(5)
 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
电池总反应为
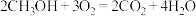 ,则
,则 电极反应式为
电极反应式为 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为 。
。
您最近一年使用:0次
解题方法
5 . 工业上常采用碱性氯化法来处理高浓度氰化物污水,发生的主要反应为CN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)。下列关于该反应的说法错误的是
| A.Cl2是氧化剂,CO2和N2是氧化产物 |
| B.若有1 mol CN-发生反应,则有5 mol电子发生转移 |
| C.若将反应设计成原电池,则CN-在负极上发生反应 |
| D.还原剂和氧化剂的化学计量数之比5:2 |
您最近一年使用:0次
6 . 氢氧燃料电池的能量转化率较高,且产物是H2O,无污染,是一种具有应用前景的绿色电源。下列有关氢氧燃料电池的说法不正确的是
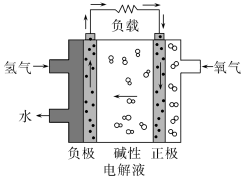

| A.通入氢气的电极发生氧化反应 |
| B.正极的电极反应式为O2+2H2O+4e-=4OH- |
| C.放电过程中碱性电解液的pH不变 |
| D.碱性电解液中阳离子向通入氧气的方向移动 |
您最近一年使用:0次
2023-03-31更新
|
837次组卷
|
2卷引用:江苏省徐州市树恩高级中学2022-2023学年高一下学期第一次月考化学试题
2023高三上·全国·专题练习
7 . 书写不同的环境下甲烷燃料电池的电极反应式。
(1)酸性条件
正极反应式:_______ ;
负极反应式:_______ 。
(2)碱性条件
正极反应式:_______ ;
负极反应式:_______ 。
(3)固体电解质(高温下能传导O2-)
正极反应式:_______ ;
负极反应式:_______ 。
(4)熔融碳酸盐(如熔融K2CO3)环境下
正极反应式:_______ ;
负极反应式:_______ 。
(1)酸性条件
正极反应式:
负极反应式:
(2)碱性条件
正极反应式:
负极反应式:
(3)固体电解质(高温下能传导O2-)
正极反应式:
负极反应式:
(4)熔融碳酸盐(如熔融K2CO3)环境下
正极反应式:
负极反应式:
您最近一年使用:0次
8 . 硅作为地壳中第二丰富的元素,将其用于制作电池有很大的应用前景。某硅−酸电池,其电极材料分别为碳包覆硅和铜的CuSi@C以及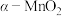 ,电解质溶液为酸性硫酸钠溶液,工作原理如图所示,下列说法错误的是
,电解质溶液为酸性硫酸钠溶液,工作原理如图所示,下列说法错误的是

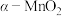 ,电解质溶液为酸性硫酸钠溶液,工作原理如图所示,下列说法错误的是
,电解质溶液为酸性硫酸钠溶液,工作原理如图所示,下列说法错误的是
| A.硅−酸电池比碱性硅−空气电池更能实现持续放电 |
| B.放电时,当电路中转移4mol电子时,负极区电解质溶液质量减少36g |
C.放电时,负极电极反应式为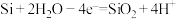 |
D.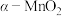 电极电极反应式仅为 电极电极反应式仅为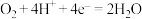 |
您最近一年使用:0次
名校
解题方法
9 . 在第十三届阿布扎比国际防务展上,采用先进的氢氧燃料电池系统的无人机,创造了该级别270分钟续航的新世界记录。下列有关氢氧燃料电池的说法正确的是
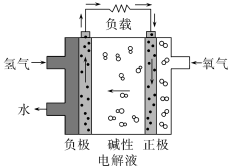

| A.通入氧气的电极发生氧化反应 |
| B.碱性电解液中阳离子向通入氢气的方向移动 |
C.正极的电极反应式为: |
D.该电池工作时,每消耗22.4L 转移4mol电子 转移4mol电子 |
您最近一年使用:0次
2021-07-31更新
|
475次组卷
|
3卷引用:重庆市清华中学2020-2021学年高一下学期第一次月考化学试题
10 . 能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
(2)下图为原电池装置示意图:
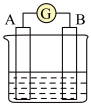
①若A为 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:_____ ,反应过程中溶液的酸性_____ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出2.24L(标准状况)气体时,电路中有_____ 个电子通过了导线(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为 溶液,则铝片为
溶液,则铝片为_____ (填“正极”或“负极”);写出该电极的电极反应式:_____ 。
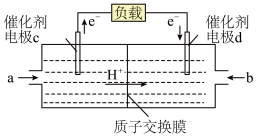
(3)燃料电池是一种具有应用前景的绿色电源, 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_____ (填“正极”或“负极”),则该燃料电池如下:
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
A. |
B.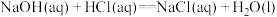 |
C.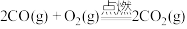 |
D.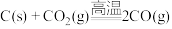 |

①若A为
 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式: 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②若A为镁片,B为铝片,电解质为
 溶液,则铝片为
溶液,则铝片为(3)燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



