解题方法
1 . 某学习小组的同学查阅相关资料知氧化性: ,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和
,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和 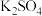 溶液。下列叙述中正确的是
溶液。下列叙述中正确的是

 ,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和
,设计了盐桥式原电池,如图。盐桥中装有琼脂与饱和 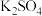 溶液。下列叙述中正确的是
溶液。下列叙述中正确的是
| A.甲烧杯的溶液中发生还原反应 |
B.电池工作时,盐桥中的 移向乙烧杯 移向乙烧杯 |
C.外电路的电流方向是从 到 到  |
D.乙烧杯中发生的电极反应为: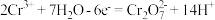 |
您最近半年使用:0次
解题方法
2 . 原电池是直接把化学能转化为电能的装置。
(1)某研究性学习小组的同学对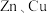 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和 溶液,起到连通电路的作用)。
溶液,起到连通电路的作用)。
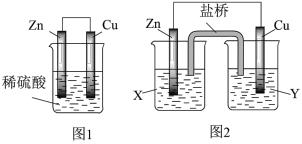
①实验表明,图1中锌电极为_____ 极(填写“正”或“负”),电极反应为:_____ 。
②图2中实验过程中只有 极上产生气泡,则X是
极上产生气泡,则X是_____ 溶液,正极的电极反应式为_____ 。
(2)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: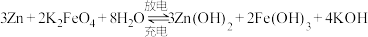
①放电时,正极反应为_____ 。
②放电时,_____ (填“正”或“负”)极附近溶液的碱性增强。
(3)新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子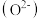 在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:
在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:_____ 。

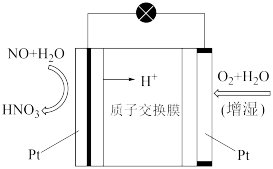
(4)一氧化氮—空气质子交换膜燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中负极的电极反应式:_____ ,若过程中产生 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为_____ L。
(1)某研究性学习小组的同学对
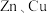 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和 溶液,起到连通电路的作用)。
溶液,起到连通电路的作用)。
①实验表明,图1中锌电极为
②图2中实验过程中只有
 极上产生气泡,则X是
极上产生气泡,则X是(2)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
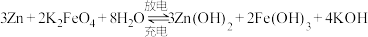
①放电时,正极反应为
②放电时,
(3)新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子
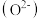 在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:
在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:
(4)一氧化氮—空气质子交换膜燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中负极的电极反应式:
 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为
您最近半年使用:0次
名校
3 . 某小组设计不同实验方案比较 、
、 的氧化性。
的氧化性。
查阅资料: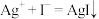
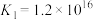 ;
;
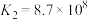
(1)方案1:通过置换反应比较
向酸化的 溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性
溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性 。反应的化学方程式是
。反应的化学方程式是___________ 。
(2)方案2:通过 、
、 分别与同一物质反应进行比较
分别与同一物质反应进行比较
①经检验,I中溶液不含 ,黄色沉淀是
,黄色沉淀是___________ 。
②经检验,II中溶液含 。推测
。推测 做氧化剂,白色沉淀A是CuI.确认A的实验如下:
做氧化剂,白色沉淀A是CuI.确认A的实验如下:

a.检验滤液无 。溶液呈蓝色说明溶液含有
。溶液呈蓝色说明溶液含有___________ (填离子符号)。
b.白色沉淀A与 溶液反应的离子方程式是
溶液反应的离子方程式是___________ ,说明氧化性 。
。
(3)分析方案2中 未能氧化
未能氧化 ,但
,但 氧化了
氧化了 的原因,设计实验如下:
的原因,设计实验如下:
(电极均为石墨,溶液浓度均为1mol/L,b,d中溶液 )
)
①a中溶液呈棕黄色的原因是___________ (用电极反应式表示)。
②“实验3”不能说明 氧化了
氧化了 。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是
。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是___________ 。
③方案2中, 能氧化
能氧化 ,而
,而 未能氧化
未能氧化 。其原因一是从K值分析:
。其原因一是从K值分析: ,故
,故 更易与
更易与 发生复分解反应,生成AgI;二是从
发生复分解反应,生成AgI;二是从 的反应特点分析:
的反应特点分析:___________ 。
 、
、 的氧化性。
的氧化性。查阅资料:
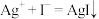
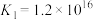 ;
;
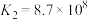
(1)方案1:通过置换反应比较
向酸化的
 溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性
溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性 。反应的化学方程式是
。反应的化学方程式是(2)方案2:通过
 、
、 分别与同一物质反应进行比较
分别与同一物质反应进行比较| 实验 | 试剂 | 编号及现象 | |
| 试管 | 滴管 | ||
 | 1.0mol/LKI溶液 | 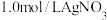 溶液 溶液 | I.产生黄色沉淀,溶液无色 |
 溶液 溶液 | II.产生白色沉淀A,溶液变黄 | ||
 ,黄色沉淀是
,黄色沉淀是②经检验,II中溶液含
 。推测
。推测 做氧化剂,白色沉淀A是CuI.确认A的实验如下:
做氧化剂,白色沉淀A是CuI.确认A的实验如下:
a.检验滤液无
 。溶液呈蓝色说明溶液含有
。溶液呈蓝色说明溶液含有b.白色沉淀A与
 溶液反应的离子方程式是
溶液反应的离子方程式是 。
。(3)分析方案2中
 未能氧化
未能氧化 ,但
,但 氧化了
氧化了 的原因,设计实验如下:
的原因,设计实验如下:| 编号 | 实验1 | 实验2 | 实验3 |
| 实验 |  | 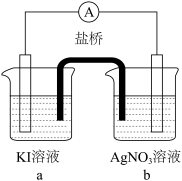 | 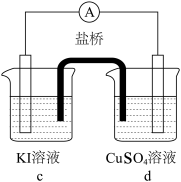 |
| 现象 | 无明显变化 | a中溶液较快变棕黄色,b中电极上析出银;电流计指针偏转 | c中溶液较慢变浅黄色;电流计指针偏转 |
 )
)①a中溶液呈棕黄色的原因是
②“实验3”不能说明
 氧化了
氧化了 。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是
。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是③方案2中,
 能氧化
能氧化 ,而
,而 未能氧化
未能氧化 。其原因一是从K值分析:
。其原因一是从K值分析: ,故
,故 更易与
更易与 发生复分解反应,生成AgI;二是从
发生复分解反应,生成AgI;二是从 的反应特点分析:
的反应特点分析:
您最近半年使用:0次
解题方法
4 . Ⅰ中和热的测定:测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
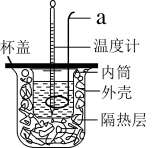
(1)仪器a的名称为_______ ,实验中还需要用到的玻璃仪器是_______ 。
(2)用相同浓度和体积的氨水代替 溶液进行上述实验,测得的中和热数值会偏小,原因为
溶液进行上述实验,测得的中和热数值会偏小,原因为_______ 。
Ⅱ.在试管中进行溶液间反应时,同学们无法观察到 转化为
转化为 ,于是又设计了如下实验(电压表读数:
,于是又设计了如下实验(电压表读数: )。
)。
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
(3)步骤ⅰ中,B中石墨上的电极反应式是_______ 。
(4)结合信息,解释实验步骤ⅳ中 的原因
的原因_______ 。
(5)能说明 转化为
转化为 的实验现象是
的实验现象是_______ 。

(1)仪器a的名称为
(2)用相同浓度和体积的氨水代替
 溶液进行上述实验,测得的中和热数值会偏小,原因为
溶液进行上述实验,测得的中和热数值会偏小,原因为Ⅱ.在试管中进行溶液间反应时,同学们无法观察到
 转化为
转化为 ,于是又设计了如下实验(电压表读数:
,于是又设计了如下实验(电压表读数: )。
)。| 装置 | 步骤 | 电压表读数 |
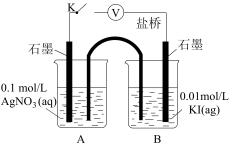 | ⅰ.如图连接装置并加入试剂,闭合K | a |
ⅱ.向B中滴入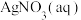 ,至沉淀完全 ,至沉淀完全 | b | |
ⅲ.再向B中投入一定量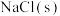 | c | |
ⅳ.重复ⅰ,再向B中加入与ⅲ等量 | a |
(3)步骤ⅰ中,B中石墨上的电极反应式是
(4)结合信息,解释实验步骤ⅳ中
 的原因
的原因(5)能说明
 转化为
转化为 的实验现象是
的实验现象是
您最近半年使用:0次
名校
解题方法
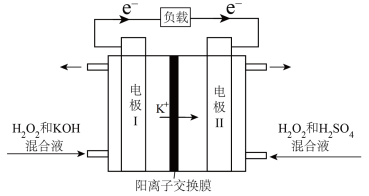
5 . 直接 燃料电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法
燃料电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法不正确 的是
 燃料电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法
燃料电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法
| A.电极Ⅰ为负极 |
B.电极Ⅱ的反应式为: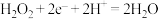 |
C.电池总反应为: |
D.该电池的设计利用了 在酸碱性不同条件下氧化性、还原性的差异 在酸碱性不同条件下氧化性、还原性的差异 |
您最近半年使用:0次
2023-01-03更新
|
1128次组卷
|
9卷引用:北京市海淀区2023届高三上学期期末考试化学试卷
北京市海淀区2023届高三上学期期末考试化学试卷(已下线)北京市海淀区2022-2023学年高三上学期期末考试化学试卷(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(8-14)黑龙江省齐齐哈尔三立高中2022-2023学年高一下学期期初考试化学试题(已下线)专题02 化学变化中的能量变化(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)北京一零一中学2023-2024学年高三上学期11月统练五化学试题北京市第一七一中学2023-2024学年高三上学期11月期中考试化学试题北京市育才学校2023-2024学年高三上学期11月期中考试化学试题北京实验学校2023-2024学年高三上学期12月化学学科竞赛试题
解题方法
6 . ORP传感器(如下图)测定物质的氧化性的原理:将Pt电极插入待测溶液中,Pt电极、Ag/AgCl电极与待测溶液组成原电池,测得的电压越高,溶液的氧化性越强。向NaIO3溶液、FeCl3溶液中分别滴加2滴H2SO4溶液,测得前者的电压增大,后者的几乎不变。
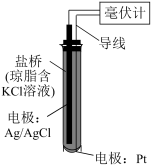
下列说法不正确 的是

下列说法
| A.盐桥中的Cl-移向Ag/AgCl电极 |
| B.Ag/AgCl电极反应是Ag-e-+Cl-=AgCl |
C.酸性越强, 的氧化性越强 的氧化性越强 |
| D.向FeCl3溶液中滴加浓NaOH溶液至碱性,测得电压几乎不变 |
您最近半年使用:0次
7 . 高锰酸钾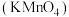 和双氧水
和双氧水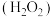 都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
(1)H2O2是一种二元弱酸,与 反应的化学方程式为
反应的化学方程式为 ,写出H2O2的电离方程式
,写出H2O2的电离方程式_______ (只写第一步)。在酸性条件下H2O2的分解速度变大,利用平衡移动的原理进行解释:_______ 。
(2)新型甲醇 和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
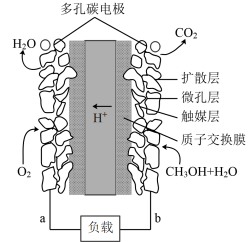
①a处的多孔碳电极是_______ (填“正极”或“负极”),发生的电极反应是_____ 。
②b处的多孔碳电极上发生的电极反应____ 。有1mol甲醇发生反应转移的质子数是_____  。
。
(3)现有 燃料电池,装置如下图所示:
燃料电池,装置如下图所示:
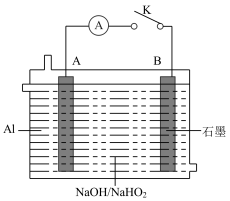
①关闭电键K,电流表指针发生偏转。A电极是Al,写出A电极的电极反应式_______ ,反应后B电极区溶液的pH_______ (填“增大”“减小”或“不变”)。
②电子从_______ 电极流向_______ 电极(填“A”或“B”)。
(4)某化学兴趣小组为了探究KMnO4与H2O2氧化性强弱,设计了如下实验装置:
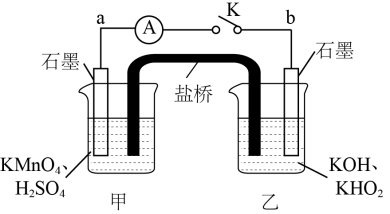
①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生_______ 反应(填“氧化”或“还原”),石墨电极b上发生的电极反应为_______ 。
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻转,最后向右偏转,说明KMnO4与H2O2氧化性与_______ 有关。
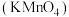 和双氧水
和双氧水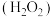 都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:(1)H2O2是一种二元弱酸,与
 反应的化学方程式为
反应的化学方程式为 ,写出H2O2的电离方程式
,写出H2O2的电离方程式(2)新型甲醇
 和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
①a处的多孔碳电极是
②b处的多孔碳电极上发生的电极反应
 。
。(3)现有
 燃料电池,装置如下图所示:
燃料电池,装置如下图所示:
①关闭电键K,电流表指针发生偏转。A电极是Al,写出A电极的电极反应式
②电子从
(4)某化学兴趣小组为了探究KMnO4与H2O2氧化性强弱,设计了如下实验装置:

①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻转,最后向右偏转,说明KMnO4与H2O2氧化性与
您最近半年使用:0次
名校
解题方法
8 . 含氮化合物种类多,用途广。回答下列问题。
(1)NH3的电子式为__________ ,NH3与NaClO在一定条件下可生成N2H4,化学方程式为__________ 。
(2) 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为__________ 。
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是__________ 。
③从分子结构角度分析,N2H4不如氨气稳定的原因是__________ 。
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则 =
=__________ (常温下NH3·H2O的电离平衡常数为 )。
)。
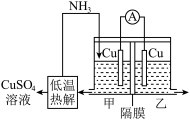
(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体__________ 。
(1)NH3的电子式为
(2)
 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是
 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是③从分子结构角度分析,N2H4不如氨气稳定的原因是
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则
 =
= )。
)。(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。

| A.甲室Cu电极为负极 |
| B.Cu2+通过隔膜进入乙室 |
| C.电池总反应为:Cu2++4NH3=[Cu(NH3)4]2+ |
| D.NH3扩散到乙室不会对电池电压产生影响 |
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体
您最近半年使用:0次
9 . 实验室探究NaHSO3溶液与Cu2+的反应。
I.如图所示制备(经检验装置气密性良好)。
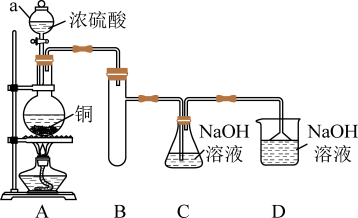
(1)仪器a的名称是___________ ,装置D的作用为___________ 。
(2)写出C中制备NaHSO3的离子方程式___________ 。
Ⅱ.探究NaHSO3溶液与Cu2+的反应,过程如图所示:
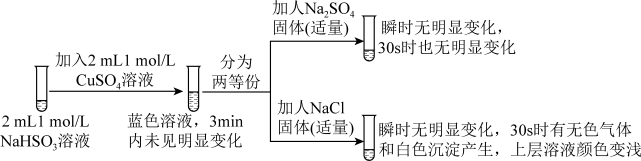
已知:硫酸亚铜易溶于水。回答下列问题:
(3)加入NaCl固体后产生的无色气体和白色沉淀经检验分别是SO2和CuCl,说明发生了氧化还原反应。加入NaCl固体发生反应的原因:
a.Cl-改变了 的还原性 b.Cl-改变了Cu2+的氧化性
的还原性 b.Cl-改变了Cu2+的氧化性
用原电池原理进行试验,探究上述现象可能的原因。
①由实验1、2可知原因a不合理,依据是___________ 。
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。
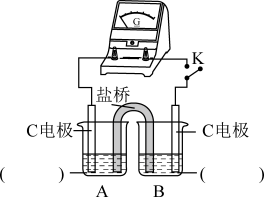
i.补全电化学装置示意图A________________ 、B_____________________ 。
ii.写出B中的电极反应方程式___________ 。
iii.请从反应原理的角度解释原因:Cl-与Cu2+的还原产物Cu+形成沉淀,___________ ,使 与Cu2+的反应能够反应完全。
与Cu2+的反应能够反应完全。
I.如图所示制备(经检验装置气密性良好)。

(1)仪器a的名称是
(2)写出C中制备NaHSO3的离子方程式
Ⅱ.探究NaHSO3溶液与Cu2+的反应,过程如图所示:

已知:硫酸亚铜易溶于水。回答下列问题:
(3)加入NaCl固体后产生的无色气体和白色沉淀经检验分别是SO2和CuCl,说明发生了氧化还原反应。加入NaCl固体发生反应的原因:
a.Cl-改变了
 的还原性 b.Cl-改变了Cu2+的氧化性
的还原性 b.Cl-改变了Cu2+的氧化性用原电池原理进行试验,探究上述现象可能的原因。
| 编号 | 实验1 | 实验2 |
| 实验 | 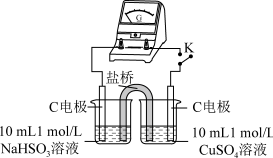 |  |
| 现象 | 闭合开关K,电流计指针发生微小偏 转,烧杯中未见明显现象 | 闭合开关K,电流计指针发生微小偏 转,烧杯中未见明显现象 |
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。

i.补全电化学装置示意图A
ii.写出B中的电极反应方程式
iii.请从反应原理的角度解释原因:Cl-与Cu2+的还原产物Cu+形成沉淀,
 与Cu2+的反应能够反应完全。
与Cu2+的反应能够反应完全。
您最近半年使用:0次
2023高三·全国·专题练习
名校
解题方法
10 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
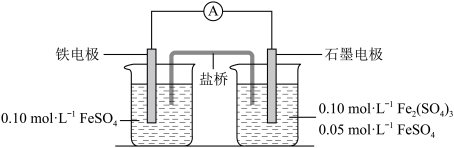
回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为___________________ ,铁电极的电极反应式为_______________________________ 。因此,验证了Fe2+氧化性小于________ 、还原性小于________ 。

回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为
您最近半年使用:0次



