名校
1 . 某小组设计不同实验方案比较 、
、 的氧化性。
的氧化性。
查阅资料: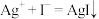
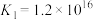 ;
;
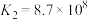
(1)方案1:通过置换反应比较
向酸化的 溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性
溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性 。反应的化学方程式是
。反应的化学方程式是___________ 。
(2)方案2:通过 、
、 分别与同一物质反应进行比较
分别与同一物质反应进行比较
①经检验,I中溶液不含 ,黄色沉淀是
,黄色沉淀是___________ 。
②经检验,II中溶液含 。推测
。推测 做氧化剂,白色沉淀A是CuI.确认A的实验如下:
做氧化剂,白色沉淀A是CuI.确认A的实验如下:

a.检验滤液无 。溶液呈蓝色说明溶液含有
。溶液呈蓝色说明溶液含有___________ (填离子符号)。
b.白色沉淀A与 溶液反应的离子方程式是
溶液反应的离子方程式是___________ ,说明氧化性 。
。
(3)分析方案2中 未能氧化
未能氧化 ,但
,但 氧化了
氧化了 的原因,设计实验如下:
的原因,设计实验如下:
(电极均为石墨,溶液浓度均为1mol/L,b,d中溶液 )
)
①a中溶液呈棕黄色的原因是___________ (用电极反应式表示)。
②“实验3”不能说明 氧化了
氧化了 。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是
。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是___________ 。
③方案2中, 能氧化
能氧化 ,而
,而 未能氧化
未能氧化 。其原因一是从K值分析:
。其原因一是从K值分析: ,故
,故 更易与
更易与 发生复分解反应,生成AgI;二是从
发生复分解反应,生成AgI;二是从 的反应特点分析:
的反应特点分析:___________ 。
 、
、 的氧化性。
的氧化性。查阅资料:
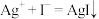
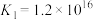 ;
;
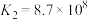
(1)方案1:通过置换反应比较
向酸化的
 溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性
溶液插入铜丝,析出黑色固体,溶液变蓝,说明氧化性 。反应的化学方程式是
。反应的化学方程式是(2)方案2:通过
 、
、 分别与同一物质反应进行比较
分别与同一物质反应进行比较| 实验 | 试剂 | 编号及现象 | |
| 试管 | 滴管 | ||
 | 1.0mol/LKI溶液 | 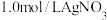 溶液 溶液 | I.产生黄色沉淀,溶液无色 |
 溶液 溶液 | II.产生白色沉淀A,溶液变黄 | ||
 ,黄色沉淀是
,黄色沉淀是②经检验,II中溶液含
 。推测
。推测 做氧化剂,白色沉淀A是CuI.确认A的实验如下:
做氧化剂,白色沉淀A是CuI.确认A的实验如下:
a.检验滤液无
 。溶液呈蓝色说明溶液含有
。溶液呈蓝色说明溶液含有b.白色沉淀A与
 溶液反应的离子方程式是
溶液反应的离子方程式是 。
。(3)分析方案2中
 未能氧化
未能氧化 ,但
,但 氧化了
氧化了 的原因,设计实验如下:
的原因,设计实验如下:| 编号 | 实验1 | 实验2 | 实验3 |
| 实验 |  | 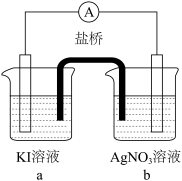 | 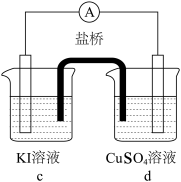 |
| 现象 | 无明显变化 | a中溶液较快变棕黄色,b中电极上析出银;电流计指针偏转 | c中溶液较慢变浅黄色;电流计指针偏转 |
 )
)①a中溶液呈棕黄色的原因是
②“实验3”不能说明
 氧化了
氧化了 。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是
。依据是空气中的氧气也有氧化作用,设计实验证实该依据,实验方案及现象是③方案2中,
 能氧化
能氧化 ,而
,而 未能氧化
未能氧化 。其原因一是从K值分析:
。其原因一是从K值分析: ,故
,故 更易与
更易与 发生复分解反应,生成AgI;二是从
发生复分解反应,生成AgI;二是从 的反应特点分析:
的反应特点分析:
您最近一年使用:0次
解题方法
2 . Ⅰ中和热的测定:测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
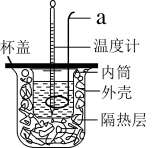
(1)仪器a的名称为_______ ,实验中还需要用到的玻璃仪器是_______ 。
(2)用相同浓度和体积的氨水代替 溶液进行上述实验,测得的中和热数值会偏小,原因为
溶液进行上述实验,测得的中和热数值会偏小,原因为_______ 。
Ⅱ.在试管中进行溶液间反应时,同学们无法观察到 转化为
转化为 ,于是又设计了如下实验(电压表读数:
,于是又设计了如下实验(电压表读数: )。
)。
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
(3)步骤ⅰ中,B中石墨上的电极反应式是_______ 。
(4)结合信息,解释实验步骤ⅳ中 的原因
的原因_______ 。
(5)能说明 转化为
转化为 的实验现象是
的实验现象是_______ 。

(1)仪器a的名称为
(2)用相同浓度和体积的氨水代替
 溶液进行上述实验,测得的中和热数值会偏小,原因为
溶液进行上述实验,测得的中和热数值会偏小,原因为Ⅱ.在试管中进行溶液间反应时,同学们无法观察到
 转化为
转化为 ,于是又设计了如下实验(电压表读数:
,于是又设计了如下实验(电压表读数: )。
)。| 装置 | 步骤 | 电压表读数 |
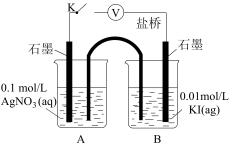 | ⅰ.如图连接装置并加入试剂,闭合K | a |
ⅱ.向B中滴入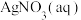 ,至沉淀完全 ,至沉淀完全 | b | |
ⅲ.再向B中投入一定量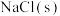 | c | |
ⅳ.重复ⅰ,再向B中加入与ⅲ等量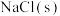 | a |
(3)步骤ⅰ中,B中石墨上的电极反应式是
(4)结合信息,解释实验步骤ⅳ中
 的原因
的原因(5)能说明
 转化为
转化为 的实验现象是
的实验现象是
您最近一年使用:0次
名校
解题方法
3 . 含氮化合物种类多,用途广。回答下列问题。
(1)NH3的电子式为__________ ,NH3与NaClO在一定条件下可生成N2H4,化学方程式为__________ 。
(2) 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为__________ 。
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是__________ 。
③从分子结构角度分析,N2H4不如氨气稳定的原因是__________ 。
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则 =
=__________ (常温下NH3·H2O的电离平衡常数为 )。
)。
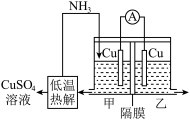
(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体__________ 。
(1)NH3的电子式为
(2)
 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是
 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是③从分子结构角度分析,N2H4不如氨气稳定的原因是
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则
 =
= )。
)。(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。

| A.甲室Cu电极为负极 |
| B.Cu2+通过隔膜进入乙室 |
| C.电池总反应为:Cu2++4NH3=[Cu(NH3)4]2+ |
| D.NH3扩散到乙室不会对电池电压产生影响 |
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体
您最近一年使用:0次
4 . 实验室探究NaHSO3溶液与Cu2+的反应。
I.如图所示制备(经检验装置气密性良好)。
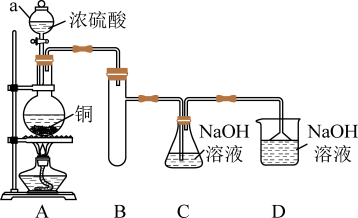
(1)仪器a的名称是___________ ,装置D的作用为___________ 。
(2)写出C中制备NaHSO3的离子方程式___________ 。
Ⅱ.探究NaHSO3溶液与Cu2+的反应,过程如图所示:
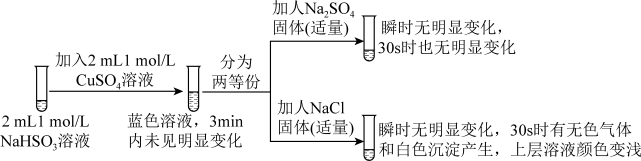
已知:硫酸亚铜易溶于水。回答下列问题:
(3)加入NaCl固体后产生的无色气体和白色沉淀经检验分别是SO2和CuCl,说明发生了氧化还原反应。加入NaCl固体发生反应的原因:
a.Cl-改变了 的还原性 b.Cl-改变了Cu2+的氧化性
的还原性 b.Cl-改变了Cu2+的氧化性
用原电池原理进行试验,探究上述现象可能的原因。
①由实验1、2可知原因a不合理,依据是___________ 。
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。
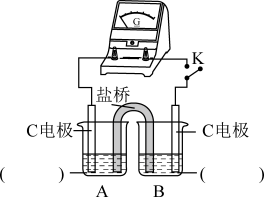
i.补全电化学装置示意图A________________ 、B_____________________ 。
ii.写出B中的电极反应方程式___________ 。
iii.请从反应原理的角度解释原因:Cl-与Cu2+的还原产物Cu+形成沉淀,___________ ,使 与Cu2+的反应能够反应完全。
与Cu2+的反应能够反应完全。
I.如图所示制备(经检验装置气密性良好)。

(1)仪器a的名称是
(2)写出C中制备NaHSO3的离子方程式
Ⅱ.探究NaHSO3溶液与Cu2+的反应,过程如图所示:

已知:硫酸亚铜易溶于水。回答下列问题:
(3)加入NaCl固体后产生的无色气体和白色沉淀经检验分别是SO2和CuCl,说明发生了氧化还原反应。加入NaCl固体发生反应的原因:
a.Cl-改变了
 的还原性 b.Cl-改变了Cu2+的氧化性
的还原性 b.Cl-改变了Cu2+的氧化性用原电池原理进行试验,探究上述现象可能的原因。
| 编号 | 实验1 | 实验2 |
| 实验 | 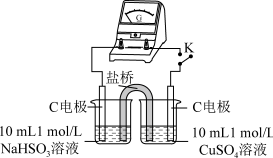 |  |
| 现象 | 闭合开关K,电流计指针发生微小偏 转,烧杯中未见明显现象 | 闭合开关K,电流计指针发生微小偏 转,烧杯中未见明显现象 |
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。

i.补全电化学装置示意图A
ii.写出B中的电极反应方程式
iii.请从反应原理的角度解释原因:Cl-与Cu2+的还原产物Cu+形成沉淀,
 与Cu2+的反应能够反应完全。
与Cu2+的反应能够反应完全。
您最近一年使用:0次
2023高三·全国·专题练习
5 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
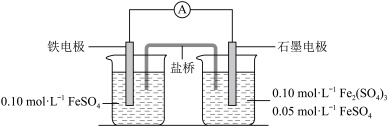
回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据表中数据,盐桥中应选择_____ 作为电解质。
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入______ 电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol•L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=______ 。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为_____ ,铁电极的电极反应式为______ 。因此,验证了Fe2+氧化性小于______ 、还原性小于______ 。

回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据表中数据,盐桥中应选择
| 阳离子 | u∞×108/(m2•s-1•V-1) | 阴离子 | u∞×108/(m2•s-1•V-1) |
| Li+ | 4.07 | HCO | 4.61 |
| Na+ | 5.19 | NO | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 | SO | 8.27 |
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol•L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次
名校
6 . 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol/L的H2SO4溶液中,乙同学将电极放入6mol/L的NaOH溶液中,如图所示。 移向
移向___________ (填“铝片”或“镁片”),写出甲中正极的电极反应式___________ 。
(2)乙中负极为___________ (填“铝片”或“镁片”),写出正极的电极反应式式:___________ 。
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为___________ 。
(4)如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。___________ 口通入(填“A”或“B”)。电流由___________ 流向___________ (填“a”或“b”)。其总反应方程式为___________ ,在碱性条件下,负极反应式为___________ 。
(5)直接乙醇燃料电池( )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。___________ 。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为___________ 。
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为___________ 。
(6)某同学设计如图的原电池,负极实验现象为___________ ,则正极的电极反应式为:___________ ,当导线中有3.01×1023个电子流过,溶液质量变化为___________ g。

 移向
移向(2)乙中负极为
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为
(4)如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
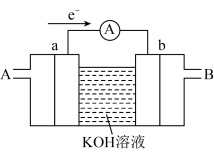
(5)直接乙醇燃料电池(
 )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为
(6)某同学设计如图的原电池,负极实验现象为

您最近一年使用:0次
2024-04-24更新
|
299次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高一下学期半期模拟考试化学试题
名校
解题方法
7 . 化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,而许多能量的利用与化学反应中的能量变化密切相关。
I.完成下列问题
(1)H2(g) +Cl2(g)=2HCl(g)的反应过程如图所示:
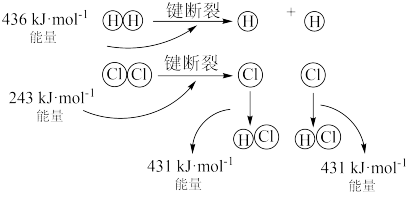
该反应为_______ (填“放热”或“吸热”)反应,其吸收或放出的热量为_______ 。
(2)下列变化中属于吸热反应的是_______ (填序号)。
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④生石灰与水反应生成熟石灰
⑤CO2 +C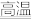 2CO
2CO
⑥Ba(OH)2·8H2O与固体NH4Cl混合
⑦C+ H2O(g)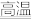 CO+ H2
CO+ H2
⑧Al与盐酸反应
(3)某化学反应中,设反应物的总能量为E1,生成物的总能量为E2。
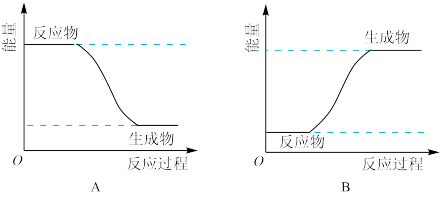
若E1>E2,则该反应可用图_______ (填“A”或“B")表示。
Ⅱ.回答下列问题
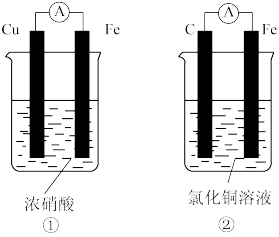
(4)为了验证Fe2+与Cu2+的氧化性强弱,如图装置能达到实验目的的是_______ (填装置序号),其正极的电极反应式为_______ ;若构建该原电池时两个电极的质量相等,当导线中通过0.4mol电子时,两个电极的质量差为_______ g。
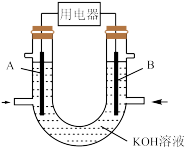
将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则_______ (填“A”或“B”)处电极入口通CH4,其电极反应式为_______ 。
I.完成下列问题
(1)H2(g) +Cl2(g)=2HCl(g)的反应过程如图所示:

该反应为
(2)下列变化中属于吸热反应的是
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④生石灰与水反应生成熟石灰
⑤CO2 +C
 2CO
2CO⑥Ba(OH)2·8H2O与固体NH4Cl混合
⑦C+ H2O(g)
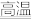 CO+ H2
CO+ H2⑧Al与盐酸反应
(3)某化学反应中,设反应物的总能量为E1,生成物的总能量为E2。

若E1>E2,则该反应可用图
Ⅱ.回答下列问题
(4)为了验证Fe2+与Cu2+的氧化性强弱,如图装置能达到实验目的的是

将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则

您最近一年使用:0次
8 . 小组探究Mg与 溶液能快速反应产生
溶液能快速反应产生 的原因。
的原因。
【查阅资料】与致密的 相比
相比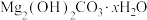 是质地疏松的难溶物。
是质地疏松的难溶物。
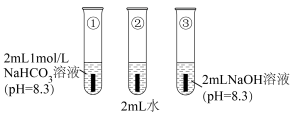
【实验过程】
如图所示,将打磨后的镁条分别加入试管①~③中,观察到:①中镁表面持续产生大量气泡,溶液显浑浊(经检验该浑浊物为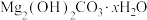 ),气体中检测到
),气体中检测到 ;②中镁表面有极微量气泡附着,滴加酚酞试液后,镁条附近至红色;③中镁表面无明显气泡。
;②中镁表面有极微量气泡附着,滴加酚酞试液后,镁条附近至红色;③中镁表面无明显气泡。
(1)镁和水反应的化学方程式为___________ 。
(2)设计实验③的目的是___________ 。
(3)将②中镁条取出,加入到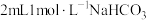 溶液中,观察到很快镁条表面开始产生大量气泡。综合上述实验,结合化学用语从化学反应平衡与速率的角度解释:Mg能与
溶液中,观察到很快镁条表面开始产生大量气泡。综合上述实验,结合化学用语从化学反应平衡与速率的角度解释:Mg能与 溶液能快速产生
溶液能快速产生 的原因是
的原因是___________ 。
(4)综合上述实验可知,在水溶液中,镁表面产生 的快慢取决于
的快慢取决于___________ 。
(5)某同学根据上述结论,设计了如图左下原电池,得到了电压表数值随时间的变化(电压数值为正值时,镁片为负极)。

①50s后,铝片表面的电极反应式为___________ 。
②50s前,原电池的负极为___________ 片(填“镁”或“铝”)。
③电压值最终变为负值的原因是___________ 。
 溶液能快速反应产生
溶液能快速反应产生 的原因。
的原因。【查阅资料】与致密的
 相比
相比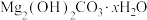 是质地疏松的难溶物。
是质地疏松的难溶物。
【实验过程】
如图所示,将打磨后的镁条分别加入试管①~③中,观察到:①中镁表面持续产生大量气泡,溶液显浑浊(经检验该浑浊物为
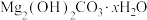 ),气体中检测到
),气体中检测到 ;②中镁表面有极微量气泡附着,滴加酚酞试液后,镁条附近至红色;③中镁表面无明显气泡。
;②中镁表面有极微量气泡附着,滴加酚酞试液后,镁条附近至红色;③中镁表面无明显气泡。(1)镁和水反应的化学方程式为
(2)设计实验③的目的是
(3)将②中镁条取出,加入到
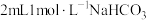 溶液中,观察到很快镁条表面开始产生大量气泡。综合上述实验,结合化学用语从化学反应平衡与速率的角度解释:Mg能与
溶液中,观察到很快镁条表面开始产生大量气泡。综合上述实验,结合化学用语从化学反应平衡与速率的角度解释:Mg能与 溶液能快速产生
溶液能快速产生 的原因是
的原因是(4)综合上述实验可知,在水溶液中,镁表面产生
 的快慢取决于
的快慢取决于(5)某同学根据上述结论,设计了如图左下原电池,得到了电压表数值随时间的变化(电压数值为正值时,镁片为负极)。

①50s后,铝片表面的电极反应式为
②50s前,原电池的负极为
③电压值最终变为负值的原因是
您最近一年使用:0次
2023-11-29更新
|
173次组卷
|
2卷引用:北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题
解题方法
9 . 某实验小组为探究CuSO4与Na2SO3反应后的产物,做如下探究实验。
【查阅资料】
①Cu2O为砖红色固体,不溶于水;
②Cu2SO3为黄色固体,不溶于水;
③[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃ 2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol∙L-1的Na2SO3溶液中滴加0.2mol∙L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)S元素在元素周期表中的位置为_______ 。N、O、S三种元素原子的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:_______ 。
(3)经检验,实验2所得溶液中有大量 、
、 生成。该实验中Cu2+表现
生成。该实验中Cu2+表现_______ 性,写出该实验中反应的离子方程式:_______ 。
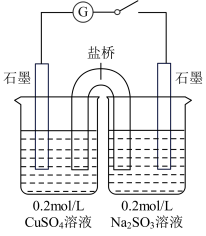
(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做_______ (填“正”或“负”)极,右侧烧杯中发生反应的电极反应式为_______ 。设计实验检验右侧烧杯中生成的阴离子,写出具体操作、现象和结论:_______ 。
【查阅资料】
①Cu2O为砖红色固体,不溶于水;
②Cu2SO3为黄色固体,不溶于水;
③[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃ 2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol∙L-1的Na2SO3溶液中滴加0.2mol∙L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)S元素在元素周期表中的位置为
(2)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:
(3)经检验,实验2所得溶液中有大量
 、
、 生成。该实验中Cu2+表现
生成。该实验中Cu2+表现(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做

您最近一年使用:0次
解题方法
10 . I.某研究性学习小组的同学对Zn、Cu、稀硫酸组成的原电池进行了探究,其中甲同学利用如图 所示装置进行探究,乙同学经过查阅资料后设计了图
所示装置进行探究,乙同学经过查阅资料后设计了图 装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。

(1)实验表明,图 中铜电极上有气泡产生,说明反应中有一部分化学能转化为
中铜电极上有气泡产生,说明反应中有一部分化学能转化为_______ 能。锌电极为_______ 极(填写“正”或“负”),电极反应为:_______ 。
(2)图 中实验过程中只有
中实验过程中只有 极上产生气泡,则
极上产生气泡,则 是
是_______ 溶液,正极上的电极反应式为_______ 。
(3)当图 装置中的溶液质量增加
装置中的溶液质量增加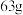 时,生成氢气
时,生成氢气_______ L(标准状况);当图 中锌电极的质量减少
中锌电极的质量减少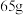 时,电路中转移的电子为
时,电路中转移的电子为_______ 
II.已知反应: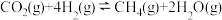
(4)已知下列数据:
若反应生成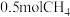
_______ (释放或者吸收)_______ 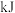 能量。
能量。
(5)在一定温度下,向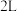 密闭容器中充入
密闭容器中充入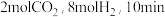 达到平衡,平衡时,测得
达到平衡,平衡时,测得 的体积分数为
的体积分数为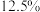 。
。 内,
内, 的平均反应速率为
的平均反应速率为_______ ,平衡时 的转化率为
的转化率为_______ 。
 所示装置进行探究,乙同学经过查阅资料后设计了图
所示装置进行探究,乙同学经过查阅资料后设计了图 装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
(1)实验表明,图
 中铜电极上有气泡产生,说明反应中有一部分化学能转化为
中铜电极上有气泡产生,说明反应中有一部分化学能转化为(2)图
 中实验过程中只有
中实验过程中只有 极上产生气泡,则
极上产生气泡,则 是
是(3)当图
 装置中的溶液质量增加
装置中的溶液质量增加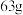 时,生成氢气
时,生成氢气 中锌电极的质量减少
中锌电极的质量减少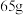 时,电路中转移的电子为
时,电路中转移的电子为
II.已知反应:
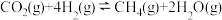
(4)已知下列数据:
| 化学键 |  |  | 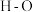 |  |
| 断裂化学键吸收的能量kJ/mol |  | 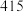 |  | 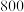 |
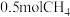
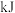 能量。
能量。(5)在一定温度下,向
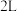 密闭容器中充入
密闭容器中充入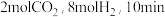 达到平衡,平衡时,测得
达到平衡,平衡时,测得 的体积分数为
的体积分数为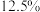 。
。 内,
内, 的平均反应速率为
的平均反应速率为 的转化率为
的转化率为
您最近一年使用:0次



