1 . 如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:

(1)通入氧气的电极为_____ (填“正极”或“负极”),通氢气一极的电极反应式为_________________ ;
(2)铁电极为_______ (填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________ 。
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为______ g;
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:
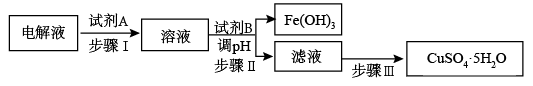
已知:几种金属阳离子开始沉淀和沉淀完全的pH:
①步骤I中加入试剂A的目的是_____________________________ ,试剂A应选择______ (填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因_____________________________________________________ ;
②步骤II中试剂B为_________ ,调节pH的范围是___________ ;
③步骤III的操作是加热浓缩、_______ 、___________ 。

(1)通入氧气的电极为
(2)铁电极为
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因
②步骤II中试剂B为
③步骤III的操作是加热浓缩、
您最近一年使用:0次
2018-01-27更新
|
690次组卷
|
4卷引用:河北省张家口市2017-2018学年高二上学期期末考试化学试题
解题方法
2 . 某研究性学习小组的同学对 、
、 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
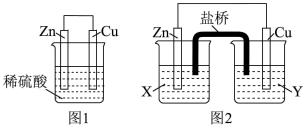
(1)实验表明,图1中铜电极上有气泡产生,说明反应中有一部分化学能转化为_______ 能。
(2)图2中的X、Y分别是 溶液、稀硫酸,实验过程中只有正极上产生气泡,则X是
溶液、稀硫酸,实验过程中只有正极上产生气泡,则X是_______ ,正极上的电极反应式为_______ 。
(3)当图1装置中的溶液质量增加 时,生成氢气
时,生成氢气_______ L(标准状况);当图2中锌电极的质量减少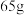 时,电路中转移的电子为
时,电路中转移的电子为_______  。
。
 、
、 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
(1)实验表明,图1中铜电极上有气泡产生,说明反应中有一部分化学能转化为
(2)图2中的X、Y分别是
 溶液、稀硫酸,实验过程中只有正极上产生气泡,则X是
溶液、稀硫酸,实验过程中只有正极上产生气泡,则X是(3)当图1装置中的溶液质量增加
 时,生成氢气
时,生成氢气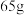 时,电路中转移的电子为
时,电路中转移的电子为 。
。
您最近一年使用:0次
2020-04-15更新
|
211次组卷
|
2卷引用:课时1 化学能转化为电能——A学习区 夯实基础(苏教版必修2)
名校
解题方法
3 . 氮的化合物在工业中应用十分广泛。
(1)工业上尿素【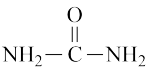 】由CO2和NH3在一定条件下合成,其热反应方程式CO2(g)+2NH3(g)=CO(NH2)2(g)+H2O(g);∆H=
】由CO2和NH3在一定条件下合成,其热反应方程式CO2(g)+2NH3(g)=CO(NH2)2(g)+H2O(g);∆H=___
(2)肼(N2H4)是一种无色易溶于水的油状液体。其具有碱性和极强的还原性,在工业生产中应用非常广泛。
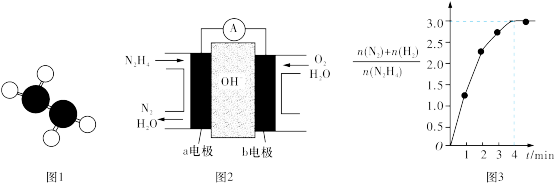
①已知肼的球棍模型如图1所示,试写出肼的电子式:_______ 。
②目前正在研发的一种肼燃料电池的结构如图2所示,_____ (填“a”或“b”)电极为电池的负极。
③在1 L固定体积的密闭容器中加入0.1 mol N2H4,在303 K、Pt催化下发生反应
N2H4(l)⇌N2(g)+2H2(g),测得容器中的[n(N2)+n(H2)]/n(N2H4)与时间的关系如图3所示,则0~4 min内氮气的平均反应速率v(N2)=________ 。
(1)工业上尿素【
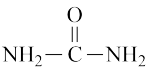 】由CO2和NH3在一定条件下合成,其热反应方程式CO2(g)+2NH3(g)=CO(NH2)2(g)+H2O(g);∆H=
】由CO2和NH3在一定条件下合成,其热反应方程式CO2(g)+2NH3(g)=CO(NH2)2(g)+H2O(g);∆H=化学键 | 键能(KJ·mol-1) |
C=O | 728 |
C—N | 305 |
N—H | 389 |
O—H | 464 |
(2)肼(N2H4)是一种无色易溶于水的油状液体。其具有碱性和极强的还原性,在工业生产中应用非常广泛。

①已知肼的球棍模型如图1所示,试写出肼的电子式:
②目前正在研发的一种肼燃料电池的结构如图2所示,
③在1 L固定体积的密闭容器中加入0.1 mol N2H4,在303 K、Pt催化下发生反应
N2H4(l)⇌N2(g)+2H2(g),测得容器中的[n(N2)+n(H2)]/n(N2H4)与时间的关系如图3所示,则0~4 min内氮气的平均反应速率v(N2)=
您最近一年使用:0次
4 . 人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,完成下面题目。
(1) 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移
,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_____________ mol电子。
(2)将铝片和铜片用导线相连,插入浓硝酸中,形成原电池,其中正极为_____________ (填“铜”或“铝”,下同),若将其插入烧碱溶液中,形成原电池,负极为_____________ 。
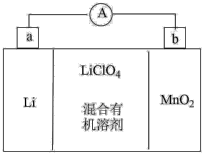
(3)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质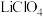 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成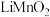 。
。_____________ (填字母,下同)极流向_____________ 极。
②电池正极反应式为___________________ ,每转移2mol电子,生成__________ g 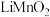 。
。
③不能用水代替电池中的混合有机溶剂,原因是__________________________ 。
④ 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为_________ 。
(4)在新能源体系下,氢能被视为与电能互补的优质二次能源。氢燃料电池能量转换率远高于氢气直接燃烧。
①碱性氢氧燃料电池工作时,负极反应式为____________________ 。
②氢氧熔融碳酸盐燃料电池是一种以熔融态碳酸盐为电解质的电池,其工作原理如图所示,有关该电池说法正确的是_____________ (填字母)。
B.该电池可利用工厂中排出的 ,减少温室气体的排放
,减少温室气体的排放
C.电子流向:氢电极—负载—氧电极—熔融碳酸盐—氢电极
D.电池工作时,外电路中流过0.2mol电子,消耗1.6g
(1)
 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移
,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移(2)将铝片和铜片用导线相连,插入浓硝酸中,形成原电池,其中正极为
(3)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质
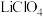 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成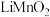 。
。
②电池正极反应式为
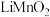 。
。③不能用水代替电池中的混合有机溶剂,原因是
④
 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为(4)在新能源体系下,氢能被视为与电能互补的优质二次能源。氢燃料电池能量转换率远高于氢气直接燃烧。
①碱性氢氧燃料电池工作时,负极反应式为
②氢氧熔融碳酸盐燃料电池是一种以熔融态碳酸盐为电解质的电池,其工作原理如图所示,有关该电池说法正确的是
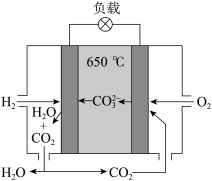
B.该电池可利用工厂中排出的
 ,减少温室气体的排放
,减少温室气体的排放C.电子流向:氢电极—负载—氧电极—熔融碳酸盐—氢电极
D.电池工作时,外电路中流过0.2mol电子,消耗1.6g

您最近一年使用:0次
名校
解题方法
5 . 任何化学反应都伴随着能量的变化,通过化学反应,化学能可以与热能、电能等不同形式的能量相互转化,用于生产、生活和科研。请回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋利用_____ (填“放热”或“吸热”)的化学变化或物理变化的原理。
(2)世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最。光伏电池能将_____ 直接转变为电能(填:“化学能”“太阳能”“热能”等)
(3)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过氨热分解法制氢气。相关化学键的键能数据
一定温度下,利用催化剂将 分解为
分解为 和3 mol
和3 mol  ,吸收90.8 kJ热量,则
,吸收90.8 kJ热量,则
_____ 。
(4)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“ ”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液
”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液_____ 。______ (填“正”或“负”)极,其电极反应式为_____ 。
②电池工作过程中,若A极区产生14 g ,则转移的电子数目为
,则转移的电子数目为______ 。
③有人提出可用甲烷去替代肼,此时惰性电极A发生的电极反应式为______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋利用
(2)世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最。光伏电池能将
(3)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过氨热分解法制氢气。相关化学键的键能数据
| 化学键 |  |  |  |
键能E/(kJ·mol ) ) | 946.0 | a | 390.8 |
 分解为
分解为 和3 mol
和3 mol  ,吸收90.8 kJ热量,则
,吸收90.8 kJ热量,则
(4)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“
 ”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液
”设计一个原电池,并在下面方框内画出简单原电池实验装置图,注明电极材料和电解质溶液
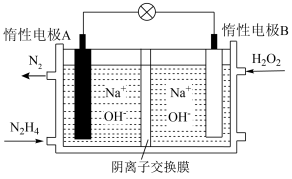
②电池工作过程中,若A极区产生14 g
 ,则转移的电子数目为
,则转移的电子数目为③有人提出可用甲烷去替代肼,此时惰性电极A发生的电极反应式为
您最近一年使用:0次
2024-04-05更新
|
730次组卷
|
4卷引用:广东省深圳市翠园中学、龙城高级中学2023-2024学年高一下学期第一次月考化学试题
广东省深圳市翠园中学、龙城高级中学2023-2024学年高一下学期第一次月考化学试题河南省安阳市林州市第一中学2023-2024学年高一下学期4月月考化学试题(已下线)猜想04 化学反应与热能、电能(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)名校期末好题汇编-化学反应与能量(非选择题)
名校
6 . 回答下列问题:
(1)氢气是一种热值高、环境友好型燃料。等物质的量的氢气完全燃烧生成液态水与生成气态水相比,生成液态水时放出热量_______ (填“多”“少”或“相等”)。
(2)拆开1mol共价键所吸收的能量或形成1mol共价键所释放的能量称为键能。已知H-H键能为436kJ/mol,H─N键能为391kJ/mol,N≡N键能为946kJ/mol。根据键能计算工业合成氨时消耗1molN2能_______ (填“吸收”或“放出”)_______ kJ热量。
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_______ ,当线路中转移0.4mol电子时,则被腐蚀铜的质量为_______ g。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:
①放电时,正极发生_______ (填“氧化”或“还原”)反应,已知负极反应式为Zn-2e-+2OH-=Zn(OH)2,则正极反应为_______ 。
②放电时,_______ (填“正”或“负”)极附近溶液的碱性增强。
(1)氢气是一种热值高、环境友好型燃料。等物质的量的氢气完全燃烧生成液态水与生成气态水相比,生成液态水时放出热量
(2)拆开1mol共价键所吸收的能量或形成1mol共价键所释放的能量称为键能。已知H-H键能为436kJ/mol,H─N键能为391kJ/mol,N≡N键能为946kJ/mol。根据键能计算工业合成氨时消耗1molN2能
(3)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,请回答下列问题:①放电时,正极发生
②放电时,
您最近一年使用:0次
2022-05-17更新
|
119次组卷
|
2卷引用:河南省濮阳市范县第一中学2021-2022学年高一下学期期中检测化学试题
7 . Ⅰ.某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若电解质溶液为0.5mol/L硫酸,电极为铜片和铝片,铝片上的电极的反应式为___________ 。
(2)若用浓硝酸作电解质溶液,电极为铜片和铝片,铝片为___________ 极(填“正”或“负”)。正极上发生的电极反应式为___________ 。
(3)若电解质溶液为0.5mol/L氢氧化钠溶液,电极为镁片和铝片,则正极发生的电极反应为_____ 。
Ⅱ.肼( )又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
(4)肼-空气燃料电池放电时:正极的电极反应式是___________ 。
(1)若电解质溶液为0.5mol/L硫酸,电极为铜片和铝片,铝片上的电极的反应式为
(2)若用浓硝酸作电解质溶液,电极为铜片和铝片,铝片为
(3)若电解质溶液为0.5mol/L氢氧化钠溶液,电极为镁片和铝片,则正极发生的电极反应为
Ⅱ.肼(
 )又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。(4)肼-空气燃料电池放电时:正极的电极反应式是
您最近一年使用:0次
8 . 广泛使用的消毒剂
Ⅰ.消毒剂可用于餐饮、衣物、环境消毒等,是生产生活中常用物品。常见的“84”消毒液、O3等都有较强的杀菌效果,可杀灭很多常见病毒。
(1)“84”消毒液的主要成分为NaClO,该消毒液___________。(双选)
(2)化学电池应用广泛,某电池企业通过回收废旧电池生产消毒液。
①如图Cu-Zn原电池中,导线中电子流向___________ 片(填 “Zn”或“Cu”)。Cu片上发生___________ 反应(填 “氧化”或“还原”)。
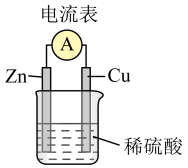
②若将铜片换成铁片,电流方向___________ 改变(填 “会”或“不会”)。
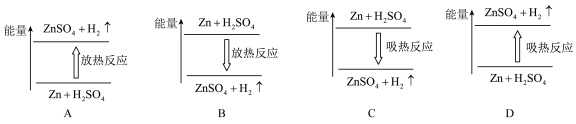
(3)若断开电路,则该反应中能量变化示意图正确的是___________ 。
Ⅱ.O3是一种清洁消毒剂,常温常压下在水溶液中发生的反应如下:2O3 3O2放热反应,下表为一定条件下,O3起始浓度为0.0216 mol•L-1时,O3浓度减少一半所需的时间。
3O2放热反应,下表为一定条件下,O3起始浓度为0.0216 mol•L-1时,O3浓度减少一半所需的时间。
(4)30°C、pH=5.0时,O3的平均反应速率为___________ 。
(5)若反应达平衡后降温,则平衡向___________ 移动,正反应速率___________ (填“增大”“减小”或“不变”)。
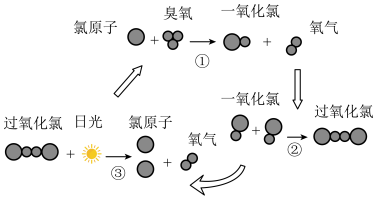
(6)大气中臭氧层能吸收和阻挡大部分紫外线进入地球。但氯原子能破坏臭氧层,其破坏过程如图所示,下列说法错误的是___________
(7)一些含硫物质也能做消毒剂。硫位于元素周期表中第___________ 周期,第___________ 族。用一个化学事实比较Cl和S的非金属性强弱___________ 。
Ⅰ.消毒剂可用于餐饮、衣物、环境消毒等,是生产生活中常用物品。常见的“84”消毒液、O3等都有较强的杀菌效果,可杀灭很多常见病毒。
(1)“84”消毒液的主要成分为NaClO,该消毒液___________。(双选)
| A.电离方程式:NaClO=Na+ + Cl- + O2- |
| B.和稀盐酸反应的产物无漂白性 |
| C.属于强电解质 |
| D.具有强氧化性 |
①如图Cu-Zn原电池中,导线中电子流向

②若将铜片换成铁片,电流方向
(3)若断开电路,则该反应中能量变化示意图正确的是

Ⅱ.O3是一种清洁消毒剂,常温常压下在水溶液中发生的反应如下:2O3
 3O2放热反应,下表为一定条件下,O3起始浓度为0.0216 mol•L-1时,O3浓度减少一半所需的时间。
3O2放热反应,下表为一定条件下,O3起始浓度为0.0216 mol•L-1时,O3浓度减少一半所需的时间。| pH t/min T/℃ | 3.0 | 4.0 | 5.0 |
| 20 | 301 | 231 | 169 |
| 30 | 158 | 108 | 54 |
| 50 | 35 | 26 | 15 |
(5)若反应达平衡后降温,则平衡向
(6)大气中臭氧层能吸收和阻挡大部分紫外线进入地球。但氯原子能破坏臭氧层,其破坏过程如图所示,下列说法错误的是___________

| A.反应中Cl作催化剂 |
| B.过氧化氯的分子式为:Cl2O2 |
| C.过氧化氯的结构式为:O-Cl-Cl-O |
| D.该过程中能量转化形式只有一种 |
您最近一年使用:0次
名校
9 . i.写出下列物质在水溶液中的电离方程式:
(1) :
:___________ 。
(2)磷酸的分步电离:___________ 。
ii.向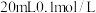 氨水中滴加
氨水中滴加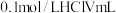 ,回答下列问题(填“>”“<”或“>”)。
,回答下列问题(填“>”“<”或“>”)。
(3)当 时,
时,
___________ 20。
(4)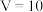 时,溶质是
时,溶质是 和
和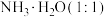 ,溶液显碱性,
,溶液显碱性,
_______ 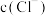 。
。
iii.利用反应 可得到清洁能源
可得到清洁能源 。
。
(5)该反应化学平衡常数表达式
___________ 。
(6)该反应的平衡常数随温度的变化如下表:
从上表可以推断:此反应是___________ (填“吸热”或“放热”)反应。
ⅳ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
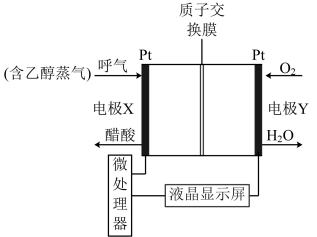
(7)电极 是该电池的
是该电池的___________ (填“正”或“负”)极。
(8)负极的电极反应式为___________ ,正极的电极反应式为___________ 。
(9)电池工作时, 通过交换膜
通过交换膜___________ (填“从左向右”或“从右向左”)迁移。
(1)
 :
:(2)磷酸的分步电离:
ii.向
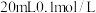 氨水中滴加
氨水中滴加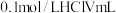 ,回答下列问题(填“>”“<”或“>”)。
,回答下列问题(填“>”“<”或“>”)。(3)当
 时,
时,
(4)
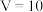 时,溶质是
时,溶质是 和
和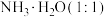 ,溶液显碱性,
,溶液显碱性,
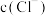 。
。iii.利用反应
 可得到清洁能源
可得到清洁能源 。
。(5)该反应化学平衡常数表达式

(6)该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数 | 10 | 9 | 1 | 0.6 |
ⅳ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

(7)电极
 是该电池的
是该电池的(8)负极的电极反应式为
(9)电池工作时,
 通过交换膜
通过交换膜
您最近一年使用:0次
名校
解题方法
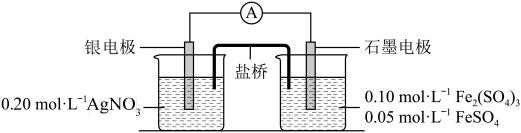
10 . 为验证反应 ,利用如图电池装置进行实验。
,利用如图电池装置进行实验。
(1)由 固体配制500mL
固体配制500mL
 溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、
溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、_______ (填写名称);在烧杯中溶解固体时,先加入一定体积的_______ 稀溶液,搅拌后再加入一定体积的水。
(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入_______ 电极溶液中。
(3)根据(2)实验结果,可知石墨电极的电极反应式为_______ ,银电极的电极反应式为_______ 。因此, 氧化性小于
氧化性小于_______ 。
(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为 ,反应一段时间后,可以观察到电流表指针反转,原因是
,反应一段时间后,可以观察到电流表指针反转,原因是_______ 。
 ,利用如图电池装置进行实验。
,利用如图电池装置进行实验。
(1)由
 固体配制500mL
固体配制500mL
 溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、
溶液,需要的仪器有胶头滴管、量筒、烧杯、玻璃棒、药匙、托盘天平、(2)电流表显示电流由银电极流向石墨电极。可知,盐桥中的阳离子进入
(3)根据(2)实验结果,可知石墨电极的电极反应式为
 氧化性小于
氧化性小于(4)电池装置中,盐桥连接两电极电解质溶液。如果盐桥中电解质为
 ,反应一段时间后,可以观察到电流表指针反转,原因是
,反应一段时间后,可以观察到电流表指针反转,原因是
您最近一年使用:0次
2022-12-07更新
|
162次组卷
|
2卷引用:河南郑州外国语学校2022-2023学年高三上学期调研考试2化学试题



