名校
解题方法
1 . 观察如图,回答问题:
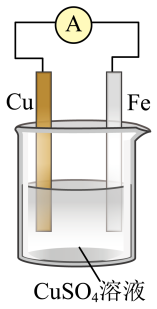
(1)该装置叫__ 装置,可以将__ 能转化为__ 能。
(2)负极是__ ,电极反应式为__ 。
(3)正极是__ ,电极反应式为__ 。
(4)电池总反应的离子方程式为__ 。

(1)该装置叫
(2)负极是
(3)正极是
(4)电池总反应的离子方程式为
您最近一年使用:0次
2020-01-29更新
|
181次组卷
|
3卷引用:海南省三亚华侨学校(南新校区)2020-2021学年高一下学期期中考试化学试题
名校
解题方法
2 . 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法不正确 的是( )


| A.Zn是负极 |
| B.电流由Cu极经导线流向Zn极 |
| C.溶液中的阴离子定向移向Zn极 |
| D.正极上发生氧化反应 |
您最近一年使用:0次
2020-01-17更新
|
132次组卷
|
2卷引用:海南省三亚华侨学校(南新校区)2020-2021学年高一下学期期中考试化学试题
3 . 根据组成原电池的条件,试以反应:Fe+Cu2+=Fe2++Cu设计一个原电池,画出示意图并标出原电池的正、负极和电子的流向(画在方框中)。_________________
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:______________ ,电极反应式:___________________ ,
正极材料:______________ ,电极反应式:___________________ ,
电解质溶液:__________________ 。
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:
正极材料:
电解质溶液:
您最近一年使用:0次
4 . 原电池反应的本质是____________ ,直接把_____ 能转变为_____ 能,电子由____ 极(填“正”或“负”)经导线流向____ 极(填“正”或“负”);在铜锌原电池中,以稀硫酸为电解质溶液,铜片上观察到的现象是_________________ ,锌为____ 极,电极上发生的是______ 反应(填“氧化”或“还原”),电极反应式为 __________________ ,溶液中的SO42-和H+的移动方向是________________________ 。
您最近一年使用:0次
名校
5 . 关于番茄电池的说法正确的是
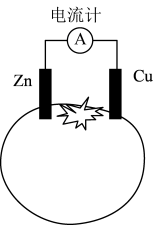

| A.Zn片作正极 |
| B.Cu片质量减少 |
| C.电子由Zn片经导线流向Cu片 |
| D.实现了电能向化学能的转化 |
您最近一年使用:0次
2019-10-24更新
|
477次组卷
|
5卷引用:海南省海口嘉勋高级中学2021-2022学年高一下学期5月月考(学考班)化学试题
6 . 理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+ =2 Ag +Cu2+ ”设制一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_______ ,发生_________ 反应(填“氧化”或“还原”),电解质溶液是_______ ;
(2)若导线上转移电子1 mol,则生成银___________ 克。
如图为某化学兴趣小组进行不同条件下化学能转变为电能探究的装置。请你回答下列问题:
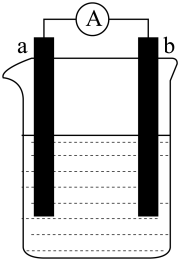
(3)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:___________ 。
(4)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置___________ (填“能”或“不能”)形成原电池,若不能,请说明理由;若能,请指出正、负极_________ 。
(1)该电池的负极材料是
(2)若导线上转移电子1 mol,则生成银
如图为某化学兴趣小组进行不同条件下化学能转变为电能探究的装置。请你回答下列问题:

(3)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(4)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置
您最近一年使用:0次
名校
7 . 将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知通入CH4的一极的电极反应为:CH4+10OH--8e-== CO32-+7H2O。下列叙述不正确的是
| A.通入CH4的电极为负极 |
| B.正极反应为:2O2+4H2O+8e-=8OH- |
| C.燃料电池工作时,溶液中的OH-向正极移动 |
| D.该电池使用一段时间后溶液中KOH的浓度将不变 |
您最近一年使用:0次
名校
解题方法
8 . 由铜、石墨和氯化铁溶液组成的原电池中,正极材料是_________ ,负极发生的电极反应是_________________ ,总的电池反应式(离子方程式)是_________________________________ 。当导线中有1.5 mol电子通过时,理论上两极的变化是______________ (填序号)。
①铜片溶解48g ②铜片增重48g ③石墨上析出28g Fe ④石墨质量不变
您最近一年使用:0次
名校
9 . 铁片和碳棒用导线连接平行放入稀硫酸中,铁片
| A.是正极 | B.是负极 | C.得到电子 | D.发生还原反应 |
您最近一年使用:0次
2017-05-16更新
|
105次组卷
|
2卷引用:海南省文昌中学2016-2017学年高一下学期期中段考(文)化学试题
9-10高一下·海南·期末
名校
10 . 将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
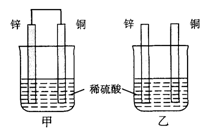

| A.两烧杯中溶液的pH均增大 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中铜片表面均无气泡产生 |
| D.甲、乙溶液均变蓝色 |
您最近一年使用:0次
2016-12-09更新
|
350次组卷
|
13卷引用:09—10年海南嘉积中学高一下学期期末考试化学卷(理科)
(已下线)09—10年海南嘉积中学高一下学期期末考试化学卷(理科)(已下线)2010年安徽省合肥八中高一第二学期期末考试化学试题(已下线)2010年安徽省双凤高中高一下学期期末考试化学试题(已下线)2011年河南省卫辉市第一中学高一上学期期末质量检测化学试卷(已下线)2010—2011学年山东省泗水一中高一下学期期末考试化学试卷(已下线)2012-2013学年湖南省浏阳一中高一6月阶段性考试化学试卷(已下线)2013-2014甘肃兰州一中高一下学期期末考试化学试卷2015-2016学年山西省祁县中学高一上学期升学化学试卷2015-2016学年甘肃省兰州一中高一下期末化学试卷天津市静海县第一中学2016-2017学年高一下学期期末终结性检测化学试题甘肃省会宁县第一中学2016-2017学年高一下学期期末考试化学试题陕西省黄陵中学高新部2016-2017学年高一下学期期末考试化学试题陕西省宝鸡市渭滨区2020-2021学年高一下学期期末考试化学试题



