名校
1 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。
(1)微型纽扣银锌电池(如下图)在生活中有广泛应用,其电极分别是 和
和 ,电解质为
,电解质为 溶液,电极反应分别为:
溶液,电极反应分别为: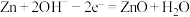 ;
;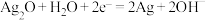 。
。 是电池的
是电池的___________ 极,电池的总反应方程式为___________ 。在使用过程中,电解质溶液的
___________ (填“增大”、“减小”或“不变”)。
(2)燃料电池必须从电池外部不断地向电池提供燃料。如甲烷 -空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为
-空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为___________ 极,正极的电极反应式为___________ 。当通入 (标准状况下)甲烷气体完全反应时,测得电路中转移
(标准状况下)甲烷气体完全反应时,测得电路中转移 电子,则甲烷的利用率为
电子,则甲烷的利用率为___________ 。
写出该装置负极的电极反应式___________ ,若此过程中转移了 电子,则理论上质子膜两侧电解液的质量变化差[
电子,则理论上质子膜两侧电解液的质量变化差[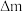 左
左 右]为
右]为___________ 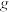 (忽略气体的溶解)。
(忽略气体的溶解)。
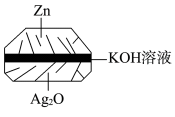
(1)微型纽扣银锌电池(如下图)在生活中有广泛应用,其电极分别是
 和
和 ,电解质为
,电解质为 溶液,电极反应分别为:
溶液,电极反应分别为: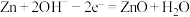 ;
;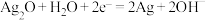 。
。
 是电池的
是电池的
(2)燃料电池必须从电池外部不断地向电池提供燃料。如甲烷
 -空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为
-空气燃料电池,工作原理如下图甲。ab均为惰性电极。a为 (标准状况下)甲烷气体完全反应时,测得电路中转移
(标准状况下)甲烷气体完全反应时,测得电路中转移 电子,则甲烷的利用率为
电子,则甲烷的利用率为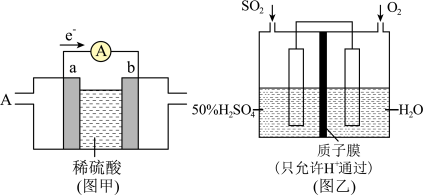
写出该装置负极的电极反应式
 电子,则理论上质子膜两侧电解液的质量变化差[
电子,则理论上质子膜两侧电解液的质量变化差[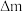 左
左 右]为
右]为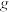 (忽略气体的溶解)。
(忽略气体的溶解)。
您最近一年使用:0次
2 . 某同学设计了如图原电池装置(盐桥装有琼脂吸附的饱和 溶液)。下列说法错误的是
溶液)。下列说法错误的是
 溶液)。下列说法错误的是
溶液)。下列说法错误的是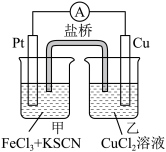
A.负极是 ,电池工作时, ,电池工作时, 发生了氧化反应 发生了氧化反应 |
| B.电池工作过程中,甲烧杯中溶液的颜色逐渐变浅 |
C.电池工作过程中,盐桥中的 向甲烧杯移动 向甲烧杯移动 |
D.该电池的反应原理是: |
您最近一年使用:0次
3 . 关于如图装置的叙述,正确的是
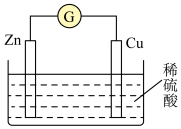
| A.锌是负极,反应过程中铜片质量逐渐减少 |
| B.该装置中,电流方向是从锌片经导线流向铜片 |
| C.工作一段时间后,电解质溶液的质量增加 |
D.该电池工作时,有大量 在铜片表面被氧化成 在铜片表面被氧化成 |
您最近一年使用:0次
名校
4 . 有A、B、C三块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀 中,B极产生大量气泡;
中,B极产生大量气泡;
②B、C用导线相连后,同时浸入稀 中,电流由B→导线→C;
中,电流由B→导线→C;
③A、C用导线相连后,同时浸入稀 中,C极发生氧化反应。
中,C极发生氧化反应。
据此判断三种金属的活动性顺序为
①A、B用导线相连后,同时浸入稀
 中,B极产生大量气泡;
中,B极产生大量气泡;②B、C用导线相连后,同时浸入稀
 中,电流由B→导线→C;
中,电流由B→导线→C;③A、C用导线相连后,同时浸入稀
 中,C极发生氧化反应。
中,C极发生氧化反应。据此判断三种金属的活动性顺序为
| A.A>B>C | B.A>C>B | C.C>A>B | D.B>C>A |
您最近一年使用:0次
名校
解题方法
5 . 浙江大学成功研制出低成本且能在数分钟之内将电量充满的 电池,若电池的总反应为:
电池,若电池的总反应为: 。下列说法不正确的是
。下列说法不正确的是
 电池,若电池的总反应为:
电池,若电池的总反应为: 。下列说法不正确的是
。下列说法不正确的是| A.放电时,锂电极作为负极 |
B.放电时,电解液中 向负极迁移 向负极迁移 |
C.放电时,负极反应式为: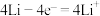 |
D.放电时,正极反应式为: |
您最近一年使用:0次
名校
解题方法
6 . 如图为水溶液锂离子电池体系,放电时的电池反应为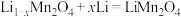 ,下列关于该电池体系的叙述
,下列关于该电池体系的叙述错误 的是
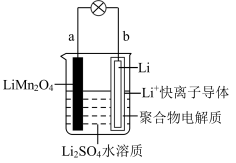
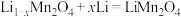 ,下列关于该电池体系的叙述
,下列关于该电池体系的叙述
| A.该电池中Li单质不可直接接触水溶液 |
| B.b为电池的负极 |
| C.放电时,电子从b极出发到a,经过Li2SO4水溶液回到b,最终形成一个回路 |
D.放电时,溶液中 从b向a迁移 从b向a迁移 |
您最近一年使用:0次
名校
解题方法
7 . 形形色色的电池在生产生活中有着重要的作用,请回答下列问题:
(1)碱性锌锰电池适合需要大电流供电的设备使用如照相机、野外摄像机、无线电控制的航模与海模、电动工具、电动玩具、收录机等,其结构如图所示,总反应为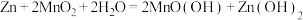 。该电池的正极为
。该电池的正极为__________ (填“Zn”或“ ”),其电极反应式为
”),其电极反应式为__________ 。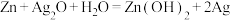 ,放电时,
,放电时, 发生
发生__________ (填“氧化”或“还原”)反应。一种废旧纽扣电池回收工艺流程如图所示,稀硫酸溶解时需要在无氧环境下进行,原因是__________ ;加入稀硝酸溶解银时,产物为 、NO和
、NO和 ,该反应的化学方程式为
,该反应的化学方程式为__________ ,调浆后,加入葡萄糖制备银粉,葡萄糖的作用为__________ 。__________ ,电路中每转移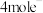 ,两极共消耗
,两极共消耗__________ L(换算成标准状况下)气体。
(1)碱性锌锰电池适合需要大电流供电的设备使用如照相机、野外摄像机、无线电控制的航模与海模、电动工具、电动玩具、收录机等,其结构如图所示,总反应为
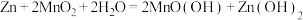 。该电池的正极为
。该电池的正极为 ”),其电极反应式为
”),其电极反应式为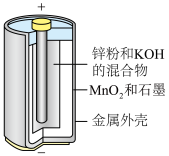
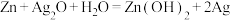 ,放电时,
,放电时, 发生
发生 、NO和
、NO和 ,该反应的化学方程式为
,该反应的化学方程式为
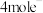 ,两极共消耗
,两极共消耗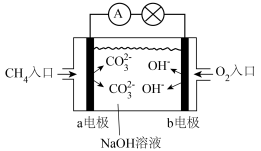
您最近一年使用:0次
2024-03-27更新
|
424次组卷
|
2卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题
名校
解题方法
8 . 碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+2H2O(l)=Zn(OH)2(s)+2MnOOH(s),下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为2MnO2(s)+2H2O(l)+2e-=2MnOOH(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
您最近一年使用:0次
2023-08-27更新
|
748次组卷
|
98卷引用:2014-2015广西桂林市第十八中学高一下学期期中考试化学试卷
2014-2015广西桂林市第十八中学高一下学期期中考试化学试卷广西河池市高级中学2016-2017学年高一下学期第二次月考化学试题广西桂林市第十八中学2019-2020学年高一下学期开学考试化学试题(已下线)2010年春季武汉睿升学校高一期中考试化学卷(已下线)09~10年大连23中高一下学期期末考试化学卷(已下线)2010-2011学年江西省安福中学高一下学期期中考试化学试卷(已下线)2010-2011学年江西省上饶市第五中学高一下学期期中考试化学试卷(已下线)2010-2011学年江西省泰和中学高一下学期期末化学模拟试卷(已下线)2011-2012学年甘肃省金昌市第一中学高一期中考试(理)化学试卷 (已下线)2011-2012学年河北省衡水中学高一下学期期末考试化学试卷(已下线)2012年人教版高中化学必修二2.2 化学能与电能练习卷(已下线)2012-2013学年吉林省白山市第一中学高一下学期期末考试化学试卷(已下线)2013-2014湖北省黄石市三中高一下学期期中考试化学试卷2014-2015辽宁省实验中学分校高一下学期期中考试化学试卷2014-2015学年北京市房山区周口店中学高一下期中考试化学试卷2014-2015学年浙江省杭州第二中学高一下期中考试化学试卷2015-2016学年河南省周口市商水一中高一下学期期中考试化学试卷2015-2016学年内蒙古平煤高中高一实验班下期中化学卷2015-2016学年辽宁省大连二十中高一6月月考化学试卷2015-2016学年河北省石家庄市辛集中学高一下第一次段考化学试卷2015-2016学年河北省永年二中高一下学期期末化学试卷2015-2016学年辽宁省庄河高中高一下期末化学试卷2016-2017学年河南师范大学附属中学高一3月月考化学试卷2016-2017学年广西桂林第18中学高一下学期期中模拟化学试卷2016-2017学年浙江省温州市“十五校联合体”高一下学期期中联考化学试卷湖南省邵阳市第二中学2016-2017学年高一下学期第三次月考化学试题高中化学人教版 选修四 第四章 电化学基础 第二节 化学电源 化学电源广西陆川县中学2017-2018学年高二12月月考化学试题安徽省定远重点中学2017-2018学年高一下学期教学段考化学试题【全国百强校】新疆维吾尔自治区乌鲁木齐八一中学2018-2019学年高一下学期期中考试化学试题广西蒙山县第一中学2017-2018学年高二上学期期末考试化学试题黑龙江省牡丹江市第一高级中学2018-2019学年高一下学期期末考试化学试题陕西省黄陵中学高新部2018-2019学年高一下学期期末考试化学试题江西省南昌市第二中学2019-2020学年高一下学期第一次月考化学试题河南省鹤壁市外国语中学2019-2020学年高一下学期段考化学试题(已下线)江苏省江阴市第一中学2018-2019高一下学期期中考试化学试卷(已下线)【镇江新东方】高一下第一次月考一中镇中联考江苏省射阳中学2022-2023学年高一下学期3月月考化学试题山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题(已下线)高考第一轮复习化学反应与能量变化单元测试(已下线)2010年广东省广州市番禹区高二下学期期中考试化学试题(已下线)2009—2010学年成都市玉林中学高二(下期)摸底测试化学(已下线)2010—2011年江苏盐城中学高二上学期期末考试化学卷(选修)(已下线)2011-2012学年甘肃省天水市一中高二上学期期末考试化学试卷(已下线)2012-2013学年陕西省三原县北城中学高二第四次月考化学试卷(已下线)2013届北京市大兴区高三上学期期末考试化学试卷(已下线)2014-2015河北省石家庄第二实验中学高二上学期期中化学(理)试卷2014-2015四川省雅安中学高二上学期期末模拟化学试卷2015-2016湖南浏阳市第一中学高二上入学考试化学试卷2015-2016学年河北成安一中、永年二中高二上期中联考化学试卷2015-2016学年福建省龙海市程溪中学高二上学期期中测试化学试卷2016届辽宁省大连八中高三上学期期中测试化学试卷2015-2016学年四川阆中中学校高二上第二次段考化学试卷2015-2016学年黑龙江省海林林业局一中高二上期末考试化学试卷2015-2016学年甘肃省甘谷一中高二上期末化学试卷(已下线)同步君 选修4 第4章 第2节 化学电源2016-2017学年山东省济南市长清一中高二上第一次质检化学卷2016-2017学年西藏拉萨中学高二上月考三化学卷云南省峨山彝族自治县第一中学2017-2018学年高二上学期期末市统测模拟考化学试题湖南省浏阳市第一中学2016-2017学年高二上学期入学考试化学试题广东省深圳高中联考联盟2017-2018学年高二上学期期末考试化学试题福建省厦门市湖滨中学2017-2018学年高二下学期第一次月考化学试题吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题陕西省黄陵中学2018-2019学年高二(重点班)上学期期中考试化学试题黑龙江省哈尔滨市呼兰区第一中学2019届高三上学期第三次(12月)月考化学试题陕西省黄陵中学2018-2019学年高二上学期期末考试化学试题江西省分宜中学2018-2019学年高二下学期第一次月考化学试题【校级联考】黑龙江省龙东南七校2018-2019学年高二上学期期末联考化学试题四川省成都市七中实验学校2018-2019学年高二5月月考化学试题(已下线)1.2.2 化学电源 练习《新教材同步备课》(鲁科版选择性必修1)云南省玉溪市新平彝族傣自治县第一中学2020-2021学年高三上学期开学考试化学试题福建省福清西山学校高中部2020-2021学年高二9月月考化学试题安徽省涡阳县育萃中学2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第2节 化学能转化为电能——电池 课时2 化学电源人教版(2019)高二化学选择性必修1第四章 化学反应与电能 第一节 原电池 课时2 化学电源(已下线)专题4.2 化学电源-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期期末考试化学试题天津市第八中学2020-2021学年高二上学期第三次统练化学试题(已下线)练习8 原电池 化学电源-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(已下线)第四章 电化学基础(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)4.2 化学电源(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)吉林省白城市第一中学2020-2021学年高二下学期3月月考化学试题(已下线)1.2.2 化学电源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)第4章 化学反应与电能(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第4章 电化学基础(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)四川省西充中学 2021-2022 学年高二上学期期中考试化学试题江苏省淮安市2021-2022学年高二上学期期末调研测试化学试题福建省福州市协作体四校2021-2022学年高二上学期期中联考化学试题四川省南充市2021-2022学年高二下学期期末考试化学试题第一节 原电池 第2课时 化学电源河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题宁夏吴忠中学2022-2023学年高二上学期期中考试化学试题作业(五) 化学电源内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期期中考试化学试题第四章 化学反应与电能 第一节 原电池 第2课时 化学电源(已下线)BBWYhjhx1110.pdf
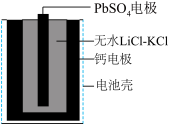
9 . 热激活电池(又称热电池)可用作导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能,该电池总反应为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.由于钙活泼,常温下在正负极间接上电流表,指针发生偏转 |
B.放电过程中, 向钙电极移动 向钙电极移动 |
C.负极反应是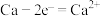 |
| D.钙电极换为铜电极也能使电池反应发生 |
您最近一年使用:0次
名校
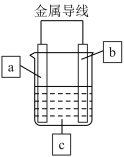
10 . 理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用反应“ ”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是
”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是
 ”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是
”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是
A.电极b的电极材料为铜,电极反应式为 |
| B.电极a的电极材料可以为Ag,也可以是石墨或铁 |
C.c溶液为AgNO3溶液,放电时 向b极移动 向b极移动 |
| D.装置放电时主要将电能转化为化学能 |
您最近一年使用:0次
2023-07-12更新
|
414次组卷
|
2卷引用:广西壮族自治区河池市2022-2023学年高一下学期期末教学质量检测化学试题



