名校
解题方法
1 . 铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如右图。若上端开口关闭,可得到强还原性的H·(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的·OH(羟基自由基)。下列说法正确的是
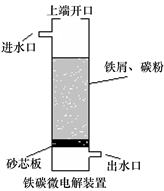
| A.无论是否鼓入空气,负极的电极反应式均为Fe-3e-= Fe3+ |
| B.鼓入空气时,每生成1mol·OH有2mol电子发生转移 |
| C.不鼓入空气时,正极的电极反应式为H+ + e- = H· |
| D.处理含有C2O42-的污水时,上端开口应关闭 |
您最近一年使用:0次
2017-04-24更新
|
832次组卷
|
2卷引用:云南省玉溪一中2019-2020学年高二上学期期末考试化学试题
名校
2 . 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
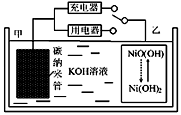

| A.放电时,甲电极反应为:NiO(OH)+H2O+e‾=Ni(OH)2+OH‾ |
| B.放电时,甲电极为正极,OH‾移向乙电极 |
C.电池总反应为H2+2NiO(OH)  2Ni(OH)2 2Ni(OH)2 |
| D.充电时,电池的碳电极与直流电源的正极相连 |
您最近一年使用:0次
2017-04-17更新
|
592次组卷
|
3卷引用:安徽省滁州市定远县西片三校2017-2018学年高二上学期期末考试化学试题
解题方法
3 . 为了国防现代化,某军事科研所研发了一种新型的Li-SO2Cl2军用电池,其组成结构示意图如图所示。
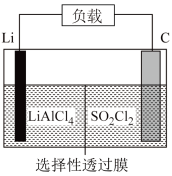
已知电池总反应为:2Li + SO2Cl2 =2LiCl + SO2↑。下列说法中不正确的是

已知电池总反应为:2Li + SO2Cl2 =2LiCl + SO2↑。下列说法中不正确的是
| A.电池的负极反应为:2Li-2e-=2Li+ |
| B.工作时电流方向:锂电极→导线→负载→碳棒 |
| C.正极电极反应为:SO2Cl2+2e-=2Cl-+SO2↑ |
| D.电池工作时,会在碳棒表面看到气泡产生 |
您最近一年使用:0次
2016-12-09更新
|
253次组卷
|
2卷引用:四川省凉山州西昌市第二中学2021-2022学年高二上学期期末检测化学试题
名校
4 . 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应
2SO2(g)+O2(g) 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
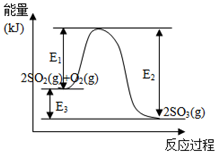
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为_______ ,反应放出_____________ 热量。(用E1、E2或E3表示)
(2)下列叙述能证明该反应已达化学平衡状态的是__________________ (填序号)
①SO2的体积分数不再发生变化
②容器内压强不再发生变化
③容器内气体原子总数不再发生变化
④相同时间内消耗2n molSO2的同时生成n molO2
⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)在反应体系中加入催化剂,反应速率增大, E3的变化是: E3____________ (填“增大”“减小”或“不变”)
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。写出通SO2电极的电极反应式:______________ 。
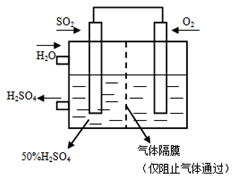
(5) SOCl2是一种无色液体,可与碳共同构成锂电池的正极材料,且其放电时也有SO2气体产生。写出SOCl2在电池中放电时的电极反应式_________________ 。
2SO2(g)+O2(g)
 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为
(2)下列叙述能证明该反应已达化学平衡状态的是
①SO2的体积分数不再发生变化
②容器内压强不再发生变化
③容器内气体原子总数不再发生变化
④相同时间内消耗2n molSO2的同时生成n molO2
⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)在反应体系中加入催化剂,反应速率增大, E3的变化是: E3
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。写出通SO2电极的电极反应式:

(5) SOCl2是一种无色液体,可与碳共同构成锂电池的正极材料,且其放电时也有SO2气体产生。写出SOCl2在电池中放电时的电极反应式
您最近一年使用:0次
9-10高二下·福建福州·期末
5 . 下图是铜锌原电池装置。其电池的总反应是: Zn(s) + CuSO4(aq)= ZnSO4(aq) + Cu(s)。
请回答以下问题:
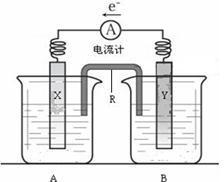
(1)R的名称是__________________ ,R中的阳离子移向_______ (填A或B)中的溶液。
(2)电极Y的材料是________ ,B中的电解质溶液是________________ 。
(3)X为原电池的______ 极,其电极反应式是____________________________ 。
请回答以下问题:

(1)R的名称是
(2)电极Y的材料是
(3)X为原电池的
您最近一年使用:0次



