1 . 铜及其化合物在生产和生活中有着广泛的应用。
(1)基态 的价层电子排布式:
的价层电子排布式:___________ 。
(2) 比
比 更稳定的原因是
更稳定的原因是___________ 。
 能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
(3)步骤I中反应的离子方程式为___________ ;___________ 。
(4)H—N—H键角大小:
___________  (填“>”、“=”或“<”),其原因是
(填“>”、“=”或“<”),其原因是___________ 。
(5)该实验能说明, 与
与 的结合能力
的结合能力___________ (填“大于”“小于”或“等于”) 与
与 的结合能力。
的结合能力。 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为___________ (填“平面正方形”或者“四面体形”)。
(6) 能与乙二胺(
能与乙二胺( )形成
)形成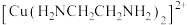 离子,结构如图,关于该配离子的说法正确的是___________。
离子,结构如图,关于该配离子的说法正确的是___________。
(1)基态
 的价层电子排布式:
的价层电子排布式:(2)
 比
比 更稳定的原因是
更稳定的原因是 能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。
能与多种物质形成配合物,为研究配合物的形成及性质,某小组进行如表实验。| 序号 | 实验步骤 | 实验现象或结论 |
| I | 向 溶液中逐滴加入氨水至过量 溶液中逐滴加入氨水至过量 | 产生蓝色沉淀,随后溶解并得到深蓝色的溶液 |
| Ⅱ | 再加入无水乙醇 | 得到深蓝色晶体 |
| Ⅲ | 测定深蓝色晶体的结构 | 晶体的化学式为 |
| Ⅳ | 将深蓝色晶体洗净后溶于水配成溶液,再加入稀NaOH溶液 | 无蓝色沉淀生成 |
(3)步骤I中反应的离子方程式为
(4)H—N—H键角大小:

 (填“>”、“=”或“<”),其原因是
(填“>”、“=”或“<”),其原因是(5)该实验能说明,
 与
与 的结合能力
的结合能力 与
与 的结合能力。
的结合能力。 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为(6)
 能与乙二胺(
能与乙二胺( )形成
)形成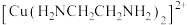 离子,结构如图,关于该配离子的说法正确的是___________。
离子,结构如图,关于该配离子的说法正确的是___________。
| A.该离子的配位数是4 | B.该离子的配体数是4 |
| C.形成配离子前后,Cu的化合价不变 | D.该离子中含离子键、非极性键与极性键 |
您最近一年使用:0次
名校
2 . 由CO、 、
、 组成的混合气体8.96L(标准状况),在足量
组成的混合气体8.96L(标准状况),在足量 中充分燃烧后,生成气体先通过足量浓
中充分燃烧后,生成气体先通过足量浓 ,再通过足量NaOH溶液,测知NaOH溶液增重26.4g,则原混合气体中乙烷的物质的量为
,再通过足量NaOH溶液,测知NaOH溶液增重26.4g,则原混合气体中乙烷的物质的量为
 、
、 组成的混合气体8.96L(标准状况),在足量
组成的混合气体8.96L(标准状况),在足量 中充分燃烧后,生成气体先通过足量浓
中充分燃烧后,生成气体先通过足量浓 ,再通过足量NaOH溶液,测知NaOH溶液增重26.4g,则原混合气体中乙烷的物质的量为
,再通过足量NaOH溶液,测知NaOH溶液增重26.4g,则原混合气体中乙烷的物质的量为| A.小于0.1mol | B.大于或等于0.1mol,小于0.2mol |
| C.一定等于0.2mol | D.大于0.2mol,小于0.3mol |
您最近一年使用:0次
名校
3 . MTP是一类重要的药物中间体,可以由TOME经环化后合成,其反应原理如图所示: ,反应过程中的液体体积变化忽略不计。下列说法正确的是
,反应过程中的液体体积变化忽略不计。下列说法正确的是
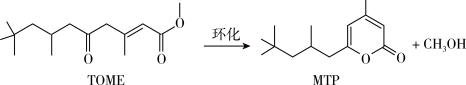
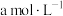 ,反应过程中的液体体积变化忽略不计。下列说法正确的是
,反应过程中的液体体积变化忽略不计。下列说法正确的是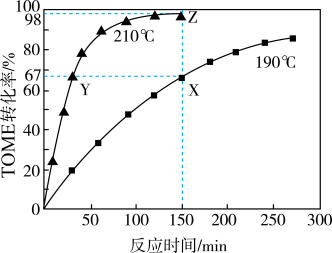
A.X点: |
| B.X、Y两点该反应的化学平衡常数相等 |
C.Z点溶液中: |
| D.反应物的消耗速率:Y点大于Z点 |
您最近一年使用:0次
名校
解题方法
4 . 催化氧化乳酸乙酯制备丙酮酸乙酯,一种可能的反应机理如图所示(其中,—Me表示 、—Et表示
、—Et表示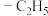 ):
):
 、—Et表示
、—Et表示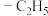 ):
):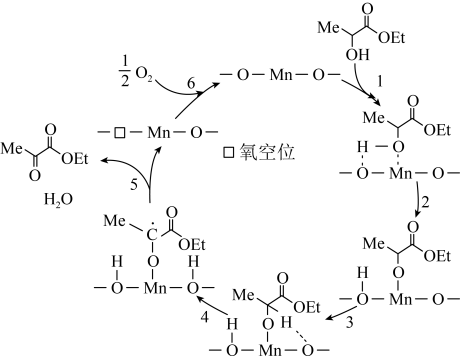
| A.反应过程中,Mn元素的化合价不发生变化 |
B.若不提供 ,则体系中也可产生丙酮酸乙酯 ,则体系中也可产生丙酮酸乙酯 |
C.理论上,消耗 可生成 可生成 丙酮酸乙酯 丙酮酸乙酯 |
D.若提供 ,则产物中含 ,则产物中含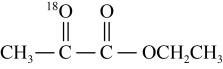 |
您最近一年使用:0次
7日内更新
|
228次组卷
|
3卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
名校
5 . 4-溴甲基肉桂酸甲酯是合成抗肿瘤药物帕比司他的重要中间体,其结构简式如图。关于该有机物的说法错误的是
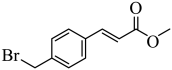
| A.能发生加成反应、氧化反应、聚合反应 |
| B.含有3种官能团 |
| C.其苯环上的二氯代物有四种(不考虑立体异构) |
| D.最多有18个原子共平面 |
您最近一年使用:0次
7日内更新
|
474次组卷
|
2卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
6 . 化合物Z是合成非诺洛芬的中间体,其合成路线如下:

A.X→Y反应中的 可以用 可以用 代替 代替 |
| B.根据Y→Z的反应可知NaBH4具有还原性 |
C.Y与足量 的加成产物中含2个手性碳原子 的加成产物中含2个手性碳原子 |
D.Y、Z可用 溶液进行鉴别 溶液进行鉴别 |
您最近一年使用:0次
名校
解题方法
7 . 有机物K是重要的药物中间体,一种K的合成路线如下:
(1)A→B的反应条件是___________ 。D→E的反应类型为___________ 。
(2)F的结构简式为___________ 。
(3)I的化学名称是___________ 。J中官能团的名称是___________ 。
(4)反应B→C的化学方程式为___________ 。
(5)鉴别D的水溶液与I的水溶液的化学试剂为___________ 。
(6)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有___________ 种;
①含有苯环;
②能发生水解反应且1molL需要2molNaOH发生反应。
其中,核磁共振氢谱有4组峰,且峰面积比为6:2:1:1的物质的结构简式为___________ (任写一种)。
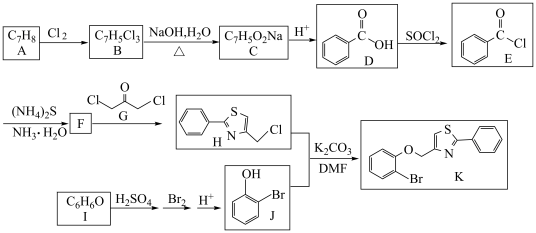
已知:①
②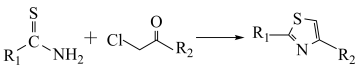
(1)A→B的反应条件是
(2)F的结构简式为
(3)I的化学名称是
(4)反应B→C的化学方程式为
(5)鉴别D的水溶液与I的水溶液的化学试剂为
(6)L是D与乙醇酯化后的产物,同时满足下列条件的L的同分异构体有
①含有苯环;
②能发生水解反应且1molL需要2molNaOH发生反应。
其中,核磁共振氢谱有4组峰,且峰面积比为6:2:1:1的物质的结构简式为
您最近一年使用:0次
名校
解题方法
8 . 胆矾(CuSO4·5H2O)的结构示意图如下所示。下列说法不正确 的是

A.基态Cu2+的价层电子轨道表示式是  |
| B.H2O中氧原子的VSEPR的价层电子对数是4 |
C.SO 中的O-S-O的键角小于H2O中的H-O-H的键角 中的O-S-O的键角小于H2O中的H-O-H的键角 |
D.胆矾中的H2O与Cu2+、H2O与SO 的作用力分别为配位键和氢键 的作用力分别为配位键和氢键 |
您最近一年使用:0次
名校
解题方法
9 . 某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收 溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为
溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为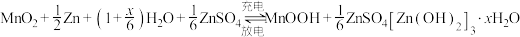 ,电池结构如图所示。
,电池结构如图所示。
(1)如图所示的几种含碳物质中,不与碳纳米管互为同素异形体的是___________ (填名称,下同),存在分子间作用力的是___________ ;属于共价晶体的是___________ 。 中
中 的化合价是
的化合价是_________ ,有机高聚物中C的杂化方式为__________ 。
(3) 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是___________ 。 的第二电离能
的第二电离能___________ (填“大于”或“小于”) 。
。
(4)一种新型稀磁半导体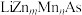 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。___________ ,n=___________ 。
②已知 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,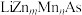 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为 。该晶体中
。该晶体中 原子与
原子与 原子之间的最短距离为
原子之间的最短距离为___________ nm(列出计算式)。
 溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为
溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为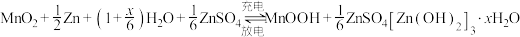 ,电池结构如图所示。
,电池结构如图所示。
(1)如图所示的几种含碳物质中,不与碳纳米管互为同素异形体的是

 中
中 的化合价是
的化合价是(3)
 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是 的第二电离能
的第二电离能 。
。(4)一种新型稀磁半导体
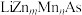 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。
②已知
 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,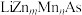 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为 。该晶体中
。该晶体中 原子与
原子与 原子之间的最短距离为
原子之间的最短距离为
您最近一年使用:0次
名校
解题方法
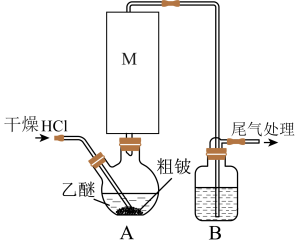
10 . 某实验小组以粗铍(含少量的Mg、Fe、Al、Cu、Si等)为原料制备、提纯BeCl2,并测定产品中BeCl2的含量。利用如图所示装置(夹持装置略)制BeCl2,实验开始前先通入一段时间的氩气。
②BeCl2溶于乙醚,不溶于苯,易发生水解;
③AlCl3溶于乙醚且溶于苯,FeCl2、MgCl2不溶于乙醚和苯;
④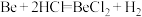 为放热反应。
为放热反应。
请回答下列问题:
(1)装置A中方框内的仪器M应为________ (填“直形冷凝管”或“球形冷凝管”),实验中装置A需置于温度15℃左右的水浴中,其主要目的是________ 。
(2)装置B中盛放的试剂为________ 。
(3)反应后,装置A中BeCl2的乙醚溶液先经过滤除去杂质________ ,再蒸馏滤液将乙醚蒸出得“固体”。为了除去“固体”中的其余杂质,可采取的操作为________ 。
(4)取 g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用
g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用 mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸
mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸 mL(已知:
mL(已知: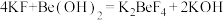 ;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为
;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为________ %(用含 、
、 和
和 的字母表示)。
的字母表示)。
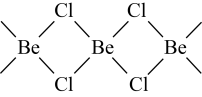
(5)氯化铍在气态时存在BeCl2分子(a)和二聚分子[(BeCl2)2](b),固态时则具有如下图所示的链状结构(c)。____ 。
②BeCl2溶于乙醚,不溶于苯,易发生水解;
③AlCl3溶于乙醚且溶于苯,FeCl2、MgCl2不溶于乙醚和苯;
④
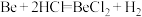 为放热反应。
为放热反应。请回答下列问题:
(1)装置A中方框内的仪器M应为
(2)装置B中盛放的试剂为
(3)反应后,装置A中BeCl2的乙醚溶液先经过滤除去杂质
(4)取
 g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用
g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用 mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸
mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸 mL(已知:
mL(已知: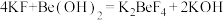 ;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为
;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为 、
、 和
和 的字母表示)。
的字母表示)。(5)氯化铍在气态时存在BeCl2分子(a)和二聚分子[(BeCl2)2](b),固态时则具有如下图所示的链状结构(c)。
您最近一年使用:0次



