湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
湖北
高三
模拟预测
2024-05-24
572次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、有机化学基础、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
湖北
高三
模拟预测
2024-05-24
572次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、有机化学基础、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
2. 化学与生产、生活密切相关。下列说法错误的是
| A.亚硝酸钠可作为食品添加剂 |
| B.稀土元素是“冶金工业的维生素” |
| C.糖类、油脂和蛋白质均是高分子化合物 |
| D.体积分数为75%的乙醇溶液可用于医用消毒 |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
3. 下列化学用语正确的是
A.乙炔的球棍模型: |
B. 的空间结构: 的空间结构: |
C.基态Br的简化电子排布式: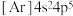 |
D.用电子式表示 的形成过程: 的形成过程: |
您最近一年使用:0次
单选题
|
较难(0.4)
4. 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.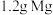 在空气中完全燃烧转移电子数为 在空气中完全燃烧转移电子数为 |
B.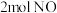 与 与 在密闭容器中充分反应后的分子数为 在密闭容器中充分反应后的分子数为 |
C. 与足量 与足量 溶液反应,所得溶液中 溶液反应,所得溶液中 的数目为 的数目为 |
D. 乙醇和 乙醇和 乙酸发生酯化反应,生成乙酸乙酯的分子数为 乙酸发生酯化反应,生成乙酸乙酯的分子数为 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 对于下列实验,描述其反应的离子方程式错误的是
A.用惰性电极电解硫酸铜溶液: |
B.向苯酚钠溶液中滴加稀盐酸: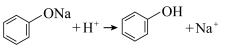 |
C.将 溶液滴入 溶液滴入 溶液中: 溶液中: |
D.向氢氧化钙溶液中滴加少量碳酸氢钙溶液: |
您最近一年使用:0次
7日内更新
|
271次组卷
|
3卷引用:湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷江苏省部分学校2024届高三下学期全真模拟测化学试卷 (已下线)第02讲 离子反应、离子方程式(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
单选题
|
适中(0.65)
解题方法
6. 我国科学家合成的喹草酮可用于高粱地除草,其结构如图所示。下列说法正确的是

A.分子式为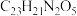 |
B.既能与盐酸反应,也能与 溶液反应 溶液反应 |
| C.分子中所有碳原子可能在同一个平面上 |
| D.使溴水和酸性高锰酸钾溶液褪色的原理相同 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
7. 下列实验装置能用于相应实验的是
|
|
| A.制备氨气 | B.制备乙二酸 |
|
|
| C.证明碳酸酸性比硅酸强 | D.检验气体中含 和 和 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-02更新
|
233次组卷
|
2卷引用:湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
单选题
|
较易(0.85)
名校
解题方法
8. X、Y、Z为短周期主族元素,X的原子序数是Y的8倍,X与Z同周期,且基态X、Z原子的未成对电子数相同。M是人体的必需微量元素之一,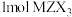 含有
含有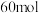 质子。下列说法一定正确的是
质子。下列说法一定正确的是
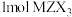 含有
含有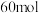 质子。下列说法一定正确的是
质子。下列说法一定正确的是| A.M在元素周期表中位于d区 | B. 中Z原子采用 中Z原子采用 杂化 杂化 |
| C.X、Z分别与Y形成化合物的沸点:X>Z | D.同周期元素中第一电离能比X大的有3种 |
您最近一年使用:0次
2024-06-02更新
|
141次组卷
|
2卷引用:湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
单选题
|
较难(0.4)
9. 钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。以钛铁矿(主要成分为 ,还含有少量
,还含有少量 )为原料制备钛的流程如图所示,已知
)为原料制备钛的流程如图所示,已知 沸点为136℃。下列说法错误的是
沸点为136℃。下列说法错误的是
 ,还含有少量
,还含有少量 )为原料制备钛的流程如图所示,已知
)为原料制备钛的流程如图所示,已知 沸点为136℃。下列说法错误的是
沸点为136℃。下列说法错误的是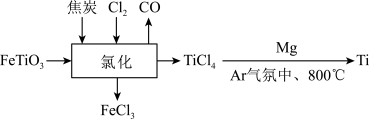
| A.为加快“氯化”速率,可将钛铁矿粉碎并与焦炭混合均匀 |
B.理论上,每制得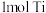 ,需要 ,需要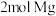 |
C. 固体为分子晶体 固体为分子晶体 |
| D.流程中的Ar气氛换成性质稳定的氮气也可以达到同样效果 |
您最近一年使用:0次
2024-05-27更新
|
201次组卷
|
2卷引用:湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
单选题
|
较易(0.85)
解题方法
10. 物质的燃烧推动了文明的进步和科技的发展,部分物质的燃烧热数据如下表:
下列热化学方程式正确的是
| 物质 |  |  |  |  |
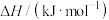 |  |  |  |  |
A. 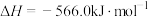 |
B.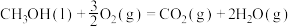 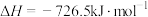 |
C.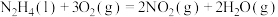 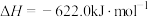 |
D. 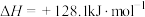 |
您最近一年使用:0次
单选题
|
较难(0.4)
11. 我国科学家开发了如图所示的电化学装置,实现了 的制备和废弃PET的回收利用。下列说法错误的是
的制备和废弃PET的回收利用。下列说法错误的是
 的制备和废弃PET的回收利用。下列说法错误的是
的制备和废弃PET的回收利用。下列说法错误的是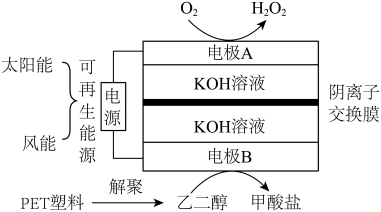
A.溶液中 移向电极B 移向电极B |
| B.电极B的电势高于电极A的电势 |
C.阳极区发生的反应为: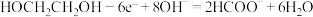 |
D.理论上每消耗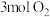 ,电极B消耗乙二醇 ,电极B消耗乙二醇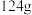 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
12. 下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 常温下,向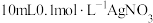 溶液中滴加5滴 溶液中滴加5滴 溶液,充分反应后,再滴加5滴 溶液,充分反应后,再滴加5滴 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 | Ksp(AgCl)>Ksp(AgI) |
| B | 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 | 醋酸是弱电解质 |
| C | 取两支试管,分别加入 的 的 溶液,将其中一支试管先加热,然后置于冷水中,与另一支试管对比 溶液,将其中一支试管先加热,然后置于冷水中,与另一支试管对比 | 探究温度对化学平衡的影响 |
| D | 向电石中滴加饱和食盐水,将产生的气体直接通入高锰酸钾溶液,观察高锰酸钾溶液是否褪色 | 乙炔具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
13. 碳化钼是碳原子嵌入金属钼的原子间隙形成的化合物,其晶胞结构如图所示,已知晶胞参数为a pm, 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是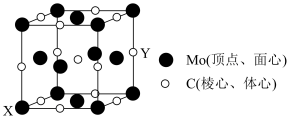
A.该晶体的化学式是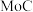 | B.碳原子位于Mo形成的八面体空隙中 |
C.图中X、Y原子间的距离为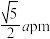 | D.该晶胞的密度是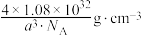 |
【知识点】 根据晶胞结构确定晶体化学式解读 晶胞的有关计算解读
您最近一年使用:0次
单选题
|
较难(0.4)
名校
解题方法
14. 催化氧化乳酸乙酯制备丙酮酸乙酯,一种可能的反应机理如图所示(其中,—Me表示 、—Et表示
、—Et表示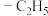 ):
):
 、—Et表示
、—Et表示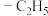 ):
):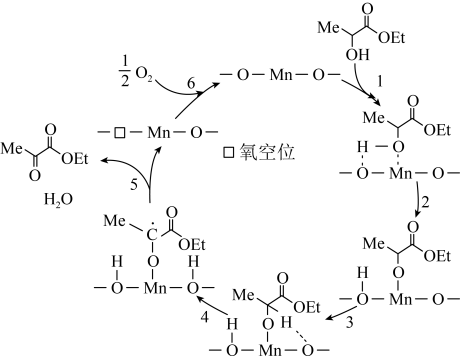
| A.反应过程中,Mn元素的化合价不发生变化 |
B.若不提供 ,则体系中也可产生丙酮酸乙酯 ,则体系中也可产生丙酮酸乙酯 |
C.理论上,消耗 可生成 可生成 丙酮酸乙酯 丙酮酸乙酯 |
D.若提供 ,则产物中含 ,则产物中含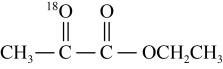 |
【知识点】 催化剂对化学反应速率的影响解读
您最近一年使用:0次
昨日更新
|
174次组卷
|
3卷引用:湖北省武汉市部分学校2023-2024学年高三下学期五月模拟训练题化学试卷
单选题
|
较难(0.4)
解题方法
15. 硫化浮选法主要是通过添加硫化剂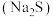 对矿物表面进行硫化来提高回收率。由大量浮选试验结果可知,蓝铜矿
对矿物表面进行硫化来提高回收率。由大量浮选试验结果可知,蓝铜矿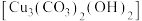 的最佳浮选pH为8.5~9.5,常温下
的最佳浮选pH为8.5~9.5,常温下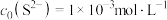 的
的 溶液中,含硫组分的分布系数
溶液中,含硫组分的分布系数 随pH的关系如图所示,分布系数
随pH的关系如图所示,分布系数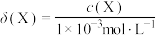 。下列说法错误的是
。下列说法错误的是
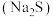 对矿物表面进行硫化来提高回收率。由大量浮选试验结果可知,蓝铜矿
对矿物表面进行硫化来提高回收率。由大量浮选试验结果可知,蓝铜矿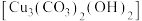 的最佳浮选pH为8.5~9.5,常温下
的最佳浮选pH为8.5~9.5,常温下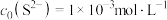 的
的 溶液中,含硫组分的分布系数
溶液中,含硫组分的分布系数 随pH的关系如图所示,分布系数
随pH的关系如图所示,分布系数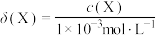 。下列说法错误的是
。下列说法错误的是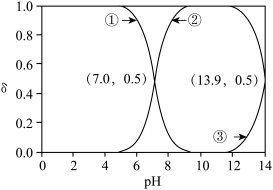
A.蓝铜矿表面硫化后形成 |
B. 时,含硫组分主要以 时,含硫组分主要以 的形式存在 的形式存在 |
C.最佳浮选pH范围内,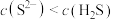 |
D.反应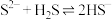 的平衡常数 的平衡常数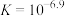 |
【知识点】 盐溶液中离子浓度大小的比较解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
解题方法
16. 电池作为一种储能装置,广泛应用于人们的日常生活中,某种锂离子电池放电时的结构示意图如图所示,溶液中金属离子开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)“负极”为嵌锂石墨,基态锂原子的价电子轨道表示式为___________ 。
(2)“电解液”常用六氟磷酸锂 做溶质,早期曾用
做溶质,早期曾用 、HF、
、HF、 反应来制备
反应来制备 ,同时生成
,同时生成 。下列说法正确的是___________。
。下列说法正确的是___________。
(3)“电解液”中常用有机试剂 来溶解
来溶解 ,该有机溶剂水解产物为
,该有机溶剂水解产物为 和
和___________ (用结构简式表示)。
(4)“隔膜”主要是聚乙烯等聚烯烃类,既为 的传输提供通道,又隔开正、负极防止短路。聚乙烯的单体分子中
的传输提供通道,又隔开正、负极防止短路。聚乙烯的单体分子中 键和
键和 键的数目之比为
键的数目之比为___________ 。
(5)正极材料为 (简称LFP),工业上以硫铁矿(主要成分是
(简称LFP),工业上以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 为原料制备
为原料制备 ,其流程如下图所示:
,其流程如下图所示:___________ 。
②加入“还原剂”的目的是___________ 。
③在生成磷酸铁沉淀时,滴加氨水时pH的控制是关键。如果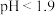 ,
, 沉淀不完全,影响产量;如果
沉淀不完全,影响产量;如果 ,则可能存在的问题是
,则可能存在的问题是___________ 。
④写出“煅烧”反应方程式,并用单线桥标明其电子转移方向和数目___________ 。

| 金属离子 |  |  |  |
| 开始沉淀pH | 1.9 | 7.0 | 3.4 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 |
(1)“负极”为嵌锂石墨,基态锂原子的价电子轨道表示式为
(2)“电解液”常用六氟磷酸锂
 做溶质,早期曾用
做溶质,早期曾用 、HF、
、HF、 反应来制备
反应来制备 ,同时生成
,同时生成 。下列说法正确的是___________。
。下列说法正确的是___________。| A.电负性:P>Cl>F | B.第一电离能: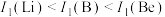 |
C.沸点: | D.分子稳定性: |
 来溶解
来溶解 ,该有机溶剂水解产物为
,该有机溶剂水解产物为 和
和(4)“隔膜”主要是聚乙烯等聚烯烃类,既为
 的传输提供通道,又隔开正、负极防止短路。聚乙烯的单体分子中
的传输提供通道,又隔开正、负极防止短路。聚乙烯的单体分子中 键和
键和 键的数目之比为
键的数目之比为(5)正极材料为
 (简称LFP),工业上以硫铁矿(主要成分是
(简称LFP),工业上以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 为原料制备
为原料制备 ,其流程如下图所示:
,其流程如下图所示: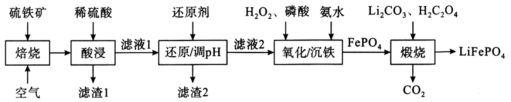
②加入“还原剂”的目的是
③在生成磷酸铁沉淀时,滴加氨水时pH的控制是关键。如果
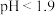 ,
, 沉淀不完全,影响产量;如果
沉淀不完全,影响产量;如果 ,则可能存在的问题是
,则可能存在的问题是④写出“煅烧”反应方程式,并用单线桥标明其电子转移方向和数目
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
17. 氧化铁黄 是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以
是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以 为原料制备
为原料制备 的流程如下:
的流程如下:
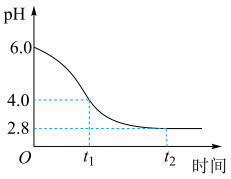
(1)若在实验室完成上述制备,不需要使用的仪器是___________ 。 时段,pH快速下降的原因是反应生成了
时段,pH快速下降的原因是反应生成了 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
② 时段,经历的反应为
时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
,该过程pH继续平缓下降的原因可能是___________ 。
(3)判断流程中产品洗涤干净的方法是___________ 。
(4)氧化铁黄 纯度可以通过产品的耗酸量确定,如下图所示。
纯度可以通过产品的耗酸量确定,如下图所示。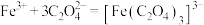 ,
, 不与稀碱液反应。
不与稀碱液反应。
①在溶液c中滴加 标准溶液,使用的指示剂为
标准溶液,使用的指示剂为___________ 。
②若实验时加入了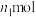 的
的 ,消耗
,消耗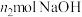 ,设氧化铁黄的摩尔质量为
,设氧化铁黄的摩尔质量为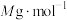 ,则氧化铁黄样品纯度为
,则氧化铁黄样品纯度为___________ (用含w、 、
、 、M的代数式表示)。
、M的代数式表示)。
③测定时,若滴入 不足量,会使实验结果
不足量,会使实验结果___________ (选填“偏大”“偏小”或“无影响”)。
 是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以
是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以 为原料制备
为原料制备 的流程如下:
的流程如下:
(1)若在实验室完成上述制备,不需要使用的仪器是
A. B.
B. C.
C. D.
D. E.
E.
 时段,pH快速下降的原因是反应生成了
时段,pH快速下降的原因是反应生成了 和
和 ,该反应的化学方程式为
,该反应的化学方程式为②
 时段,经历的反应为
时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
,该过程pH继续平缓下降的原因可能是(3)判断流程中产品洗涤干净的方法是
(4)氧化铁黄
 纯度可以通过产品的耗酸量确定,如下图所示。
纯度可以通过产品的耗酸量确定,如下图所示。
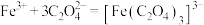 ,
, 不与稀碱液反应。
不与稀碱液反应。①在溶液c中滴加
 标准溶液,使用的指示剂为
标准溶液,使用的指示剂为②若实验时加入了
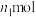 的
的 ,消耗
,消耗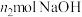 ,设氧化铁黄的摩尔质量为
,设氧化铁黄的摩尔质量为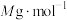 ,则氧化铁黄样品纯度为
,则氧化铁黄样品纯度为 、
、 、M的代数式表示)。
、M的代数式表示)。③测定时,若滴入
 不足量,会使实验结果
不足量,会使实验结果
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
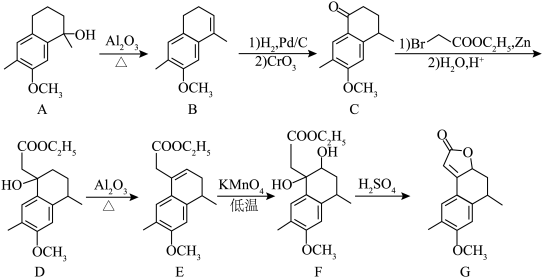
18. 化合物G是合成药物的重要中间体,其合成路线如下图所示。
(1)A→B的反应类型是___________ 。
(2)B→C的过程中,氧化得到的官能团是___________ (填名称)。
(3)F中有___________ 个手性碳原子。
(4)F→G的化学方程式为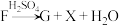 ,则X的结构简式为
,则X的结构简式为___________ 。
(5)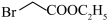 的同分异构体中,与其具有相同官能团的有
的同分异构体中,与其具有相同官能团的有___________ 种(不考虑立体异构和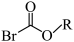 结构);其中核磁共振氢谱有两组峰,且峰面积之比为
结构);其中核磁共振氢谱有两组峰,且峰面积之比为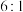 的结构简式为
的结构简式为___________ 。
(6)以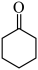 、乙醇为含碳原料,利用上述合成路线中“C→”的原理,合成化合物H(
、乙醇为含碳原料,利用上述合成路线中“C→”的原理,合成化合物H(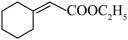 )。
)。___________ 。
②最后一步转化中,反应物的结构简式为___________ 。
(1)A→B的反应类型是
(2)B→C的过程中,氧化得到的官能团是
(3)F中有
(4)F→G的化学方程式为
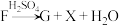 ,则X的结构简式为
,则X的结构简式为(5)
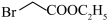 的同分异构体中,与其具有相同官能团的有
的同分异构体中,与其具有相同官能团的有 结构);其中核磁共振氢谱有两组峰,且峰面积之比为
结构);其中核磁共振氢谱有两组峰,且峰面积之比为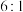 的结构简式为
的结构简式为(6)以
 、乙醇为含碳原料,利用上述合成路线中“C→”的原理,合成化合物H(
、乙醇为含碳原料,利用上述合成路线中“C→”的原理,合成化合物H(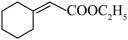 )。
)。已知:RCH2COOH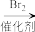

②最后一步转化中,反应物的结构简式为
您最近一年使用:0次
解答题-原理综合题
|
困难(0.15)
19. 正丁烷催化裂解为化工行业提供了丰富的原料,相关反应如下:
反应Ⅰ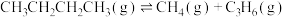

反应Ⅱ

回答下列问题:
(1)已知 ,
, 随着温度变化的三种趋势如图1中曲线所示。能用来表示反应Ⅱ的曲线是
随着温度变化的三种趋势如图1中曲线所示。能用来表示反应Ⅱ的曲线是___________ (填“x”、“y”或“z”)。 密闭的刚性容器中通入
密闭的刚性容器中通入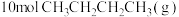 发生反应Ⅰ、反应Ⅱ,保持温度不变,正丁烷、丙烯的浓度随时间的变化关系如图2所示。
发生反应Ⅰ、反应Ⅱ,保持温度不变,正丁烷、丙烯的浓度随时间的变化关系如图2所示。
① 内
内
___________  。
。
②反应达到平衡后的压强是反应前的___________ 倍。
③反应Ⅱ的平衡常数
___________ 。
④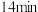 时,降低温度,丙烯的浓度随时间的变化对应图2中的曲线
时,降低温度,丙烯的浓度随时间的变化对应图2中的曲线___________ (填标号)。
(3)采用选择性膜技术(可选择性地让某气体通过而脱离体系)可提高 的选择性,其原因是
的选择性,其原因是___________ 。
(4)工业生产时向正丁烷中混入一定量的水蒸气以减少积碳对催化剂活性的影响,结合化学方程式说明这样操作的原因___________ 。
反应Ⅰ
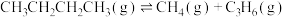

反应Ⅱ


回答下列问题:
(1)已知
 ,
, 随着温度变化的三种趋势如图1中曲线所示。能用来表示反应Ⅱ的曲线是
随着温度变化的三种趋势如图1中曲线所示。能用来表示反应Ⅱ的曲线是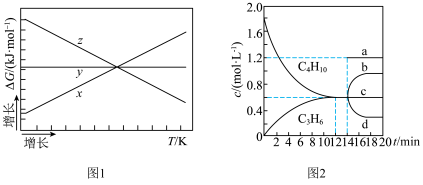
 密闭的刚性容器中通入
密闭的刚性容器中通入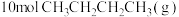 发生反应Ⅰ、反应Ⅱ,保持温度不变,正丁烷、丙烯的浓度随时间的变化关系如图2所示。
发生反应Ⅰ、反应Ⅱ,保持温度不变,正丁烷、丙烯的浓度随时间的变化关系如图2所示。①
 内
内
 。
。②反应达到平衡后的压强是反应前的
③反应Ⅱ的平衡常数

④
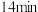 时,降低温度,丙烯的浓度随时间的变化对应图2中的曲线
时,降低温度,丙烯的浓度随时间的变化对应图2中的曲线(3)采用选择性膜技术(可选择性地让某气体通过而脱离体系)可提高
 的选择性,其原因是
的选择性,其原因是(4)工业生产时向正丁烷中混入一定量的水蒸气以减少积碳对催化剂活性的影响,结合化学方程式说明这样操作的原因
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、有机化学基础、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
试卷题型(共 19题)
题型
数量
单选题
15
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 硅酸盐 常见合金的组成 传统硅酸盐材料 | |
| 2 | 0.65 | 蛋白质的变性 高分子化合物的分类和表示方法 化学科学对人类文明发展的意义 食品添加剂 | |
| 3 | 0.94 | 有机物的结构式、结构简式、比例模型、球棍模型、最简式 共价化合物的结构及形成过程 电子排布式 利用杂化轨道理论判断分子的空间构型 | |
| 4 | 0.4 | 氧化还原反应与NA相关推算 一氧化氮的化学性质 盐类水解规律 乙酸的酯化反应 | |
| 5 | 0.65 | 离子方程式的正误判断 Fe2+的鉴别及其应用 电解池电极反应式及化学方程式的书写 苯酚的弱酸性 | |
| 6 | 0.65 | 含碳碳双键物质的性质的推断 有机分子中原子共面的判断 多官能团有机物的结构与性质 酰胺的性质与应用 | |
| 7 | 0.85 | 氨气的实验室制法 二氧化硫与其他强氧化剂的反应 醇与强氧化剂的氧化反应 物质性质实验方案的设计 | |
| 8 | 0.85 | 根据原子结构进行元素种类推断 电离能变化规律 利用杂化轨道理论判断分子的空间构型 | |
| 9 | 0.4 | 有关铁及其化合物转化的流程题型 电解池有关计算 晶体类型判断 物质分离、提纯综合应用 | |
| 10 | 0.85 | 表示燃烧热的热化学方程式书写 盖斯定律与热化学方程式 | |
| 11 | 0.4 | 电解原理的应用 电解原理的理解及判断 电解池电极反应式及化学方程式的书写与判断 电解池有关计算 | |
| 12 | 0.85 | 温度对化学平衡移动的影响 沉淀转化 实验室制取乙炔的原理 物质性质实验方案的设计 | |
| 13 | 0.65 | 根据晶胞结构确定晶体化学式 晶胞的有关计算 | |
| 14 | 0.4 | 催化剂对化学反应速率的影响 | |
| 15 | 0.4 | 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 16 | 0.65 | 酯的水解反应机理 电离能变化规律 共价键的形成及主要类型 物质制备的探究 | 工业流程题 |
| 17 | 0.4 | 硫酸根离子的检验 酸碱中和滴定原理的应用 物质分离、提纯综合应用 综合实验设计与评价 | 实验探究题 |
| 18 | 0.4 | 根据要求书写同分异构体 同分异构体的数目的确定 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |
| 19 | 0.15 | 化学平衡的移动及其影响因素 化学平衡图像分析 化学平衡常数的有关计算 化学反应进行方向的判据 | 原理综合题 |







