解题方法
1 . 反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图甲所示:
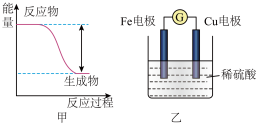
(1)该反应为______ (填”吸热”或“放热”)反应。
(2)该反应____ (填“是”或“否”)氧化还原反应;若将上述反应设计成原电池,装置如图乙,该装置工作时,电子沿导线流入_____ (填“Cu”或“Fe”)电极,该电极为____ (填“正”或“负”)极,电极反应式为____ ;若反应产生11.2L气体(标准状况下),则电路中应该有____ mol电子发生了转移。

(1)该反应为
(2)该反应
您最近半年使用:0次
解题方法
2 . 某化学兴趣小组的同学设计了如图所示的装置,完成下列问题:
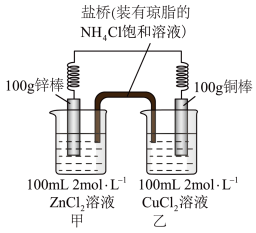
(1)反应过程中,_____ 棒质量减少,当一电极质量增加2 g,另一电极减轻的质量_____ (填“大于”、“小于”或“等于”)2g,正极的电极反应为_______ 。
(2)盐桥的作用是向甲、乙两烧杯中提供NH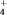 和Cl-,使两烧杯溶液中保持电荷守恒。
和Cl-,使两烧杯溶液中保持电荷守恒。
①反应过程中Cl-将进入______ (填“甲”或“乙”)烧杯。
②当外电路中转移0.2 mol电子时,乙烧杯中浓度最大的阳离子是______ 。

(1)反应过程中,
(2)盐桥的作用是向甲、乙两烧杯中提供NH
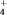 和Cl-,使两烧杯溶液中保持电荷守恒。
和Cl-,使两烧杯溶液中保持电荷守恒。①反应过程中Cl-将进入
②当外电路中转移0.2 mol电子时,乙烧杯中浓度最大的阳离子是
您最近半年使用:0次
2020-01-11更新
|
295次组卷
|
2卷引用:吉林省通化市梅河口市博文学校2019-2020学年高二上学期第二次月考化学试题
3 . 在由铜片、锌片和200 mL一定浓度的稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的H2时,硫酸恰好用完,请填空并计算:
①正极的电极反应式为______________ ;负极的电极反应式为______________ ;
②通过导线的电子的物质的量___________ ;
③求原稀硫酸的物质的量浓度___________ 。
①正极的电极反应式为
②通过导线的电子的物质的量
③求原稀硫酸的物质的量浓度
您最近半年使用:0次
10-11高一下·辽宁大连·阶段练习
4 . 由铜片、锌片和100mL稀硫酸溶液组成的原电池中,当铜片上产生2.24L(标态)气体时,硫酸恰好作用完,试计算:
⑴锌片质量减轻了_______ 克 ⑵原稀硫酸溶液的物质的量浓度是________________
⑴锌片质量减轻了
您最近半年使用:0次
11-12高二上·江苏盐城·期末
5 . 铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42— 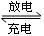 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是______________ ;电解液中H2SO4的浓度将变______ ;当外电路通过1 mol电子时,理论上负极板的质量增加________ g。
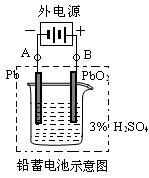
(2)电池使用一段时间后,若按图连接,则在A电极上生成_______ 、B电极上生成______ ,此时铅蓄电池的正负极的极性将______ 。(填“不变”或“对掉”)
 2PbSO4+2H2O
2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是

(2)电池使用一段时间后,若按图连接,则在A电极上生成
您最近半年使用:0次
9-10高一下·河南郑州·期末
6 . 在盛有500mL 0.4mol/LH2SO4混合溶液的大烧杯中。用锌、铜作电极,用导线连接形成原电池,当电极锌消耗6.5g时,试完成:
(1)写出电极反应式:负极_______________ ;正极_____________________ 。
(2)电极上共析出氢气的质量____________ 。
(1)写出电极反应式:负极
(2)电极上共析出氢气的质量
您最近半年使用:0次
9-10高一下·河北·期中
7 . 利用碳棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当碳棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。试计算:
(1)锌片的质量减少了_______________ ?
(2)原稀硫酸溶液的物质的量浓度_______________ 。
(3)有_________ 个电子通过了导线。
(1)锌片的质量减少了
(2)原稀硫酸溶液的物质的量浓度
(3)有
您最近半年使用:0次



