名校
1 . 用如图所示的新型电池可以处理含 的碱性废水,同时还可以淡化海水。
的碱性废水,同时还可以淡化海水。
 的碱性废水,同时还可以淡化海水。
的碱性废水,同时还可以淡化海水。
A.a极电极反应式: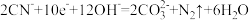 |
B.电池工作一段时间后,右室溶液的 减小 减小 |
| C.交换膜Ⅰ为阴离子交换膜,交换膜Ⅱ为阳离子交换膜 |
D.若将含有 的废水完全处理,理论上可除去 的废水完全处理,理论上可除去 的质量为 的质量为 |
您最近半年使用:0次
2 . 我国科学家研发了一种在废水处理中实现碳中和的绿色化学装置,同时获得乙酰胺,其原理如图。下列说法错误的是
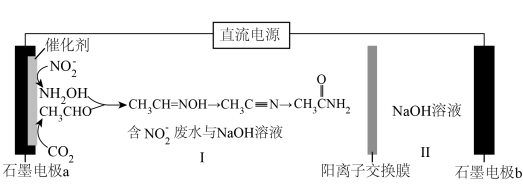

| A.石墨电极b为阳极,Na+由Ⅱ室移向Ⅰ室 |
| B.电解一段时间后,Ⅰ、Ⅱ室溶液的pH均逐渐增大 |
C. 发生还原反应: 发生还原反应: |
| D.理论上,每产生0.1mol乙酰胺的同时电极b有15.68L(STP)O2生成 |
您最近半年使用:0次
解题方法
3 . 液体锌电池具有成本低、安全性强等特点,其工作原理如图所示(KOH凝胶中允许离子存在、生成或迁移)。
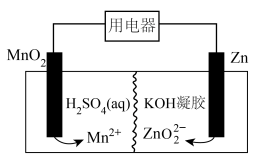
下列说法正确的是
A.电流由 极经用电器流向 极经用电器流向 极 极 |
B.负极反应式为 |
C.工作一段时间后,锌极区 升高 升高 |
D.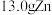 参与反应,理论上电路中转移 参与反应,理论上电路中转移 电子 电子 |
您最近半年使用:0次
名校
解题方法
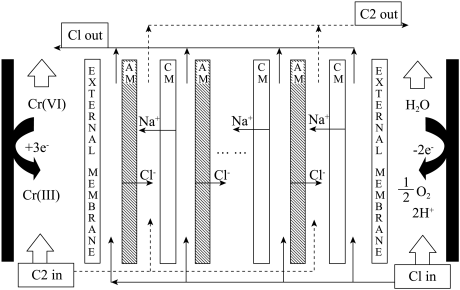
4 . 某课题组利用盐度梯度和氧化还原工艺成功设计了如图所示的电池装置,将酸性废水中存在的高毒性 转化为
转化为 后再经后续处理转化为
后再经后续处理转化为 离开溶液。设装置内温度恒定为
离开溶液。设装置内温度恒定为 。
。
已知:对于电池正极反应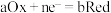 有
有 方程
方程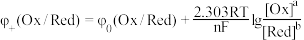
注:(1) 下,
下,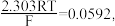 n为转移电子数;电势越高反应的趋势越大;
n为转移电子数;电势越高反应的趋势越大;
(2)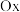 为氧化态物质,
为氧化态物质, 为还原态物质,
为还原态物质,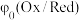 为定值;
为定值;
(3)对于除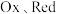 外还有其他如
外还有其他如 等参加反应的物质,它们的浓度的幂次方也要代入方程。
等参加反应的物质,它们的浓度的幂次方也要代入方程。
(参考数据: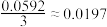 )
)
下列说法错误的是
 转化为
转化为 后再经后续处理转化为
后再经后续处理转化为 离开溶液。设装置内温度恒定为
离开溶液。设装置内温度恒定为 。
。
已知:对于电池正极反应
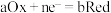 有
有 方程
方程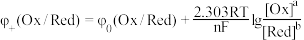
注:(1)
 下,
下,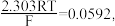 n为转移电子数;电势越高反应的趋势越大;
n为转移电子数;电势越高反应的趋势越大;(2)
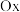 为氧化态物质,
为氧化态物质, 为还原态物质,
为还原态物质,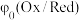 为定值;
为定值;(3)对于除
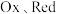 外还有其他如
外还有其他如 等参加反应的物质,它们的浓度的幂次方也要代入方程。
等参加反应的物质,它们的浓度的幂次方也要代入方程。(参考数据:
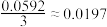 )
)下列说法错误的是
A.该电池利用溶液盐度梯度产生电势,“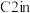 ”表示低浓度盐溶液 ”表示低浓度盐溶液 |
B.负极产生标准状况下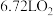 ,理论上转化 ,理论上转化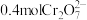 |
C.若要升高正极电势,可向正极区中加入 固体或升高正极区 固体或升高正极区 |
D.若正极区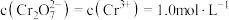 恒定,当正极区 恒定,当正极区 由1.0降低为0.5时,正极电势升高约 由1.0降低为0.5时,正极电势升高约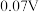 |
您最近半年使用:0次
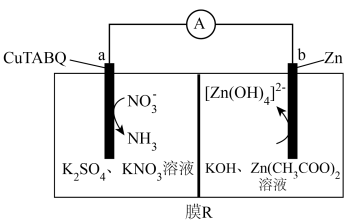
5 . 香港城市大学科研人员开发一种电极材料 (四氨基苯醌铜)可实现高效率地将硝酸根转化为氨,工作原理如图所示。下列叙述错误的是
(四氨基苯醌铜)可实现高效率地将硝酸根转化为氨,工作原理如图所示。下列叙述错误的是
 (四氨基苯醌铜)可实现高效率地将硝酸根转化为氨,工作原理如图所示。下列叙述错误的是
(四氨基苯醌铜)可实现高效率地将硝酸根转化为氨,工作原理如图所示。下列叙述错误的是
| A.装置工作时将化学能转化成电能 |
B.一段时间后,电极 附近溶液 附近溶液 升高 升高 |
C.电极 的电极反应式为 的电极反应式为 |
D.每生成17g 时有9mol 时有9mol 由膜 由膜 的左侧向右侧迁移 的左侧向右侧迁移 |
您最近半年使用:0次
6 . 铝空气燃料电池是一种新型高能量电池,具有能量密度大、无污染、可靠性高、寿命长、使用安全等优点。图1是一种盐水铝空气电池装置原理图,图2是石墨空气电极结构示意图。下列说法正确的是


| A.铝极为负极,发生还原反应 |
| B.该电池属于金属铝的吸氧腐蚀 |
C.石墨空气电极的电极反应式: |
| D.在石墨空气电极中,OH-能穿过多孔防水透气层进入右侧 |
您最近半年使用:0次
名校
解题方法
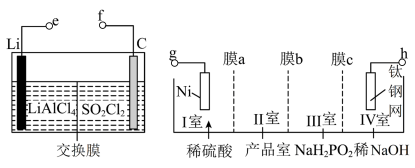
7 . 某研究机构使用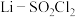 电池电解制备
电池电解制备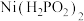 ,其工作原理如图所示。已知电池反应为
,其工作原理如图所示。已知电池反应为 。下列说法不正确的是
。下列说法不正确的是
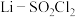 电池电解制备
电池电解制备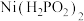 ,其工作原理如图所示。已知电池反应为
,其工作原理如图所示。已知电池反应为 。下列说法不正确的是
。下列说法不正确的是
| A.e接口连接g |
B.石墨(C)电极上反应式为 |
C.产品室增加 ,钛钢网电极上收集到标准状况下气体11.2L ,钛钢网电极上收集到标准状况下气体11.2L |
| D.膜a、膜c是阳离子交换膜,膜b是阴离子交换膜 |
您最近半年使用:0次
名校
8 . 某金属能和盐酸反应生成H2,该金属与锌组成原电池时,锌为负极,则该金属可能为
| A.铝 | B.铜 | C.锡 | D.铁 |
您最近半年使用:0次
9 . 某化学兴趣小组利用反应Zn+2FeCl3=ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是


| A.Zn为负极,发生氧化反应 |
| B.b电极反应式为2Fe3++2e-=2Fe2+ |
| C.电子流动方向是a电极→FeCl3溶液→b电极 |
| D.电池的正极材料可以选用石墨、铂电极,也可以用铜电极 |
您最近半年使用:0次
名校
解题方法
10 . 目前,我国光伏发电并网装机容量稳居全球首位。以四甲基氯化铵[(CH3)4NCl]为原料,采用光伏并网发电装置,通过电渗析法合成(CH3)4NOH,工作原理如图。下列说法正确的是
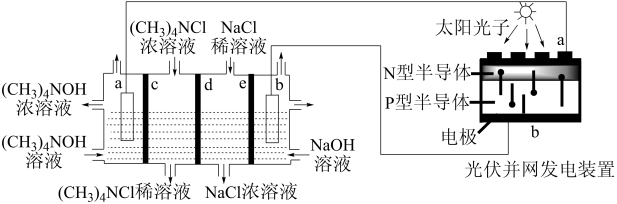

| A.光伏并网发电装置中N型半导体为负极 |
B.c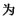 阳离子交换膜,d、e均为阴离子交换膜 阳离子交换膜,d、e均为阴离子交换膜 |
| C.保持电流恒定,升高温度可加快合成四甲基氢氧化铵的速率 |
| D.制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况) |
您最近半年使用:0次



