名校
解题方法
1 . 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法不正确 的是( )


| A.Zn是负极 |
| B.电流由Cu极经导线流向Zn极 |
| C.溶液中的阴离子定向移向Zn极 |
| D.正极上发生氧化反应 |
您最近一年使用:0次
2020-01-17更新
|
132次组卷
|
2卷引用:福建省晋江市养正中学2019-2020学年高二上学期第二次月考化学试题
2012·海南省直辖县级单位·一模
名校
解题方法
2 . 结合下图判断,下列叙述正确的是( )
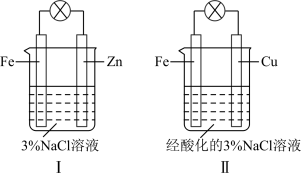

| A.Ⅰ和Ⅱ中正极均被保护 |
| B.Ⅰ和Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-=4OH- |
| D.Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀 |
您最近一年使用:0次
2020-01-16更新
|
312次组卷
|
16卷引用:2012届海南省琼海市高考模拟测试(一)化学试卷
(已下线)2012届海南省琼海市高考模拟测试(一)化学试卷(已下线)2013届吉林省松原市油田高中高三8月底摸底考试化学试卷(已下线)2013-2014学年天津市南开区高二上学期期末考试化学试卷2016届河北省枣强中学高三上学期期中测试化学试卷黑龙江省大庆第一中学2017-2018学年高二上学期期末(第四次月考)考试化学试题(已下线)解密09 电化学(教师版)——备战2018年高考化学之高频考点解密江西省南昌市八一中学、洪都中学等六校2019-2020学年高二上学期期末联考化学试题黑龙江省双鸭山市第一中学2019-2020学年高二上学期期末考试化学试题云南省文山马关实验高级中学2019-2020学年高二期末考试化学试题天津市静海区第一中学2020届高三下学期第六周周末训练化学试题辽宁省凌源市第二高级中学2019-2020学年高二下学期第二次网测化学试题山东省章丘市第一中学2020-2021学年高二上学期9月月考化学试题西藏日喀则市上海实验学校2019-2020学年高二上学期期末考试化学试题山东省济南德润高级中学2021-2022学年高二上学期10月月考化学试题天津市天津中学2022-2023学年高二上学期线上期末考试化学试题(已下线)北京市第四中学2023-2024学年高二上学期期中考试化学试题
名校
3 . 锌空气电池的电容量大,可作为汽车的清洁能源。总反应式为:2Zn+O2+2H2O=2Zn(OH)2。示意图如图所示:
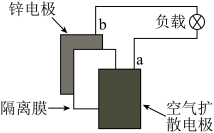
有关该电池的说法正确的是( )

有关该电池的说法正确的是( )
| A.电池可以用稀硫酸做电解质溶液 |
| B.电池工作时,电子由a电极沿导线流向b电极 |
| C.空气扩散电极上的电极反应:O2+2H2O+4e-=4OH- |
| D.阻隔空气进入锌--空气电池,电池停止工作 |
您最近一年使用:0次
2019-12-12更新
|
317次组卷
|
3卷引用:海南省2020年新高考模拟化学试题
4 . 根据组成原电池的条件,试以反应:Fe+Cu2+=Fe2++Cu设计一个原电池,画出示意图并标出原电池的正、负极和电子的流向(画在方框中)。_________________
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:______________ ,电极反应式:___________________ ,
正极材料:______________ ,电极反应式:___________________ ,
电解质溶液:__________________ 。
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:
正极材料:
电解质溶液:
您最近一年使用:0次
5 . 原电池反应的本质是____________ ,直接把_____ 能转变为_____ 能,电子由____ 极(填“正”或“负”)经导线流向____ 极(填“正”或“负”);在铜锌原电池中,以稀硫酸为电解质溶液,铜片上观察到的现象是_________________ ,锌为____ 极,电极上发生的是______ 反应(填“氧化”或“还原”),电极反应式为 __________________ ,溶液中的SO42-和H+的移动方向是________________________ 。
您最近一年使用:0次
名校
6 . 关于番茄电池的说法正确的是
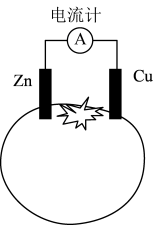

| A.Zn片作正极 |
| B.Cu片质量减少 |
| C.电子由Zn片经导线流向Cu片 |
| D.实现了电能向化学能的转化 |
您最近一年使用:0次
2019-10-24更新
|
477次组卷
|
5卷引用:上海市金山中学2017-2018学年高二下学期期中考试(合格)化学试题
13-14高三·广东·阶段练习
名校
7 . 某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理。下列叙述正确的是
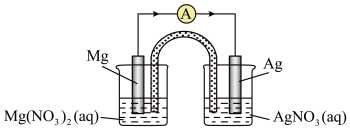

| A.银片为负极,发生的反应为Ag++e-=Ag |
| B.进行实验时,琼脂中K+移向Mg(NO3)2溶液 |
| C.用稀硫酸代替AgNO3溶液,可形成原电池 |
| D.取出盐桥,电流表依然有偏转 |
您最近一年使用:0次
2019-08-05更新
|
421次组卷
|
10卷引用:海南省海南枫叶国际学校2018-2019学年高二下学期期中考试化学试题
海南省海南枫叶国际学校2018-2019学年高二下学期期中考试化学试题(已下线)2014届广东省华附、省实、深中、广雅高三四校联考理综化学试卷福建省华安一中、龙海二中2019-2020学年高二上学期第一次联考化学试题(已下线)2019年11月23日 《每日一题》高二化学人教版(选修4)——周末培优甘肃省静宁县第一中学2019-2020学年高一下学期期中考试(第二次月考)化学试题吉林省长春实验中学2019-2020学年高一6月月考化学试题四川省南充高级中学2020-2021学年高二上学期期中考试化学试题(已下线)专题4.1 原电池-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)4.1 原电池(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)湖南省永州市祁阳县第四中学2023-2024学年高二上学期10月月考化学试题
8 . 理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+ =2 Ag +Cu2+ ”设制一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_______ ,发生_________ 反应(填“氧化”或“还原”),电解质溶液是_______ ;
(2)若导线上转移电子1 mol,则生成银___________ 克。
如图为某化学兴趣小组进行不同条件下化学能转变为电能探究的装置。请你回答下列问题:
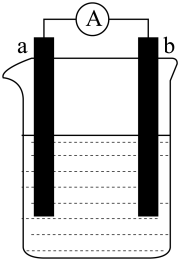
(3)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:___________ 。
(4)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置___________ (填“能”或“不能”)形成原电池,若不能,请说明理由;若能,请指出正、负极_________ 。
(1)该电池的负极材料是
(2)若导线上转移电子1 mol,则生成银
如图为某化学兴趣小组进行不同条件下化学能转变为电能探究的装置。请你回答下列问题:

(3)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(4)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置
您最近一年使用:0次
名校
9 . 硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。其工作原理如下图所示,下列说法正确的是
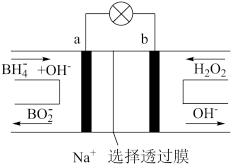

| A.电池的负极反应为BH4-+2H2O-8e-=BO2-+8H+ |
| B.放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4 |
| C.电池放电时Na+从b极区移向a极区 |
| D.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
您最近一年使用:0次
2019-07-16更新
|
3277次组卷
|
11卷引用:广东省揭阳市2018-2019学年高二下学期期末考试理综化学试题
广东省揭阳市2018-2019学年高二下学期期末考试理综化学试题广东省潮州市2019-2020学年高二下学期期末统考化学试题河南省驻马店市第二高级中学2019-2020学年高二下学期期末考试化学试题黑龙江省大庆铁人中学2020-2021学年高二上学期第一次月考化学试题海南省琼海市嘉积第二中学2021-2022学年高二下学期教学质量监测(段考)化学科试题 人教版2019必修第二册 第六章 专题强化练2 电极反应式的书写及新型电源四川省内江市第六中学2020-2021学年高一下期期中考试化学试题江西省赣县第三中学2021-2022学年高二上学期入学考试化学试题河南省信阳高级中学2021-2022学年高二上学期9月月考化学试题福建省福建师范大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第二册第六单元01讲核心
12-13高二上·海南·期末
名校
解题方法
10 . 微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH- 根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液的pH减小 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
您最近一年使用:0次



