2010·安徽合肥·三模
名校
解题方法
1 . 用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是
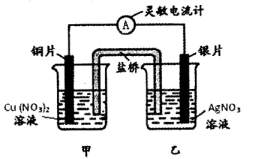

| A.电子通过盐桥从乙池流向甲池 |
| B.铜导线替换盐桥,原电池仍继续工作 |
| C.开始时,银片上发生的反应是:Ag—e=Ag+ |
| D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同 |
您最近一年使用:0次
2019-01-30更新
|
1012次组卷
|
7卷引用:海南省琼山中学2019-2020学年高二上学期期中考试化学试题
海南省琼山中学2019-2020学年高二上学期期中考试化学试题(已下线)安徽省合肥市2010年高三第三次教学质量检测(理科综合化学)(已下线)2014年高中化学人教版选修四第四章 电化学基础练习卷河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第三次月考化学试题福建省三明市三地三校2017-2018学年高二上学期期中联考化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期期末考试(实验班)化学试题吉林省白城市洮南市第一中学2020-2021学年高二上学期第三次月考化学试题
9-10高一下·广东·期末
名校
2 . 关于如图所示装置的叙述,正确的是
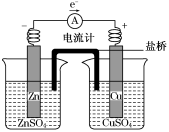

| A.铜是阳极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.铜离子在铜片表面被还原 |
您最近一年使用:0次
2018-01-11更新
|
653次组卷
|
20卷引用:2014届海南省琼海市嘉积中学高三上学期教学质量监测化学试卷
(已下线)2014届海南省琼海市嘉积中学高三上学期教学质量监测化学试卷(已下线)09—10年广东实验中学高一下学期期末考试(模块二)化学卷(已下线)2010年黑龙江省拜泉一中高二上学期期末考试化学试卷(已下线)2010—2011学年吉林省北师大宁江附中高二上学期期末考试化学试卷(已下线)2011-2012学年陕西省岐山县高二上学期期末质量检测理科化学试卷(已下线)2012-2013学年四川省雅安中学高二下学期期中考试化学试卷湖南省师范大学附属中学2016-2017学年高二(理科)上学期期末考试化学试题【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题福建省东山县第二中学2018-2019学年高二上学期第一次(10月)月考化学试题浙江省杭州市西湖高级中学2017-2018学年高二12月月考化学试题浙江省温州市求知中学2018-2019学年高二上学期期中考试(选考)化学试题【全国百强校】西藏自治区拉萨中学2018-2019学年高二上学期第四次月考(期末)理科综合化学试题河南省郑州市106中学2019-2020学年高二9月月考化学(理)试题黑龙江漠河市高级中学2020-2021学年高二上学期期末考试化学试题青海省北外附属西宁新华联国际学校2020-2021学年高二上学期期末考试化学试题甘肃省玉门市油田第一中学2020-2021学年高二上学期期末考试化学试题甘肃省宁县第二中学2020-2021学年高二上学期期末考试化学试题上海市上海中学2021-2022学年高一下学期期末考试化学试题甘肃省武威市凉州区2020-2021学年高二上学期期末考试化学试题甘肃省天水市秦安县第一中学2022-2023学年高二上学期期末考试化学试题
名校
3 . 将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知通入CH4的一极的电极反应为:CH4+10OH--8e-== CO32-+7H2O。下列叙述不正确的是
| A.通入CH4的电极为负极 |
| B.正极反应为:2O2+4H2O+8e-=8OH- |
| C.燃料电池工作时,溶液中的OH-向正极移动 |
| D.该电池使用一段时间后溶液中KOH的浓度将不变 |
您最近一年使用:0次
名校
解题方法
4 . 由铜、石墨和氯化铁溶液组成的原电池中,正极材料是_________ ,负极发生的电极反应是_________________ ,总的电池反应式(离子方程式)是_________________________________ 。当导线中有1.5 mol电子通过时,理论上两极的变化是______________ (填序号)。
①铜片溶解48g ②铜片增重48g ③石墨上析出28g Fe ④石墨质量不变
您最近一年使用:0次
名校
5 . 铁片和碳棒用导线连接平行放入稀硫酸中,铁片
| A.是正极 | B.是负极 | C.得到电子 | D.发生还原反应 |
您最近一年使用:0次
2017-05-16更新
|
105次组卷
|
2卷引用:海南省文昌中学2016-2017学年高一下学期期中段考(文)化学试题
9-10高一下·海南·期末
名校
6 . 将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
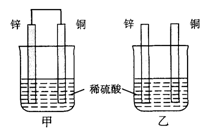

| A.两烧杯中溶液的pH均增大 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中铜片表面均无气泡产生 |
| D.甲、乙溶液均变蓝色 |
您最近一年使用:0次
2016-12-09更新
|
350次组卷
|
13卷引用:09—10年海南嘉积中学高一下学期期末考试化学卷(理科)
(已下线)09—10年海南嘉积中学高一下学期期末考试化学卷(理科)(已下线)2010年安徽省合肥八中高一第二学期期末考试化学试题(已下线)2010年安徽省双凤高中高一下学期期末考试化学试题(已下线)2011年河南省卫辉市第一中学高一上学期期末质量检测化学试卷(已下线)2010—2011学年山东省泗水一中高一下学期期末考试化学试卷(已下线)2012-2013学年湖南省浏阳一中高一6月阶段性考试化学试卷(已下线)2013-2014甘肃兰州一中高一下学期期末考试化学试卷2015-2016学年山西省祁县中学高一上学期升学化学试卷2015-2016学年甘肃省兰州一中高一下期末化学试卷天津市静海县第一中学2016-2017学年高一下学期期末终结性检测化学试题甘肃省会宁县第一中学2016-2017学年高一下学期期末考试化学试题陕西省黄陵中学高新部2016-2017学年高一下学期期末考试化学试题陕西省宝鸡市渭滨区2020-2021学年高一下学期期末考试化学试题
11-12高一下·广东佛山·期中
名校
解题方法
7 . 原电池中,正极是
| A.发生氧化反应的电极 | B.电子流出的电极 |
| C.发生还原反应的电极 | D.与负极相比较,金属性较活泼的一极 |
您最近一年使用:0次
真题
名校
8 . Li—SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4—SOCl2。电池的总反应可表示为4Li+2SOCl2===4LiCl+S+SO2↑。请回答下列问题:
(1)电池的负极材料为________ ,发生的电极反应为__________________ 。
(2)电池正极发生的电极反应为___________________________ 。
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是___________________ ,反应的化学方程式为______ 。
(4)组装该电池必须在无水、无氧的条件下进行,原因是__________________ 。
(1)电池的负极材料为
(2)电池正极发生的电极反应为
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是
(4)组装该电池必须在无水、无氧的条件下进行,原因是
您最近一年使用:0次
2016-12-09更新
|
2942次组卷
|
21卷引用:2009年普通高等学校招生统一考试化学试题(海南卷)
2009年普通高等学校招生统一考试化学试题(海南卷)(已下线)2010—2011浙江省嘉兴一中高一下学期期中考试化学试卷(已下线)2011-2012学年江苏省南京三中高二下学期期末考试化学选修试卷(已下线)2012-2013学年四川省成都七中高一下学期期末考试化学试卷2015-2016学年河北省文安一中高二上学期第一次月考化学试卷(已下线)同步君 选修4 第4章 第2节 化学电源江西省南昌市八一中学、洪都中学、麻丘中学等六校2016-2017学年高一5月联考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第二次月考化学试题高中化学人教版 选修四 第四章 电化学基础 第二节 化学电源 化学电源2017-2018学年高一化学人教版必修2:第二章检测题(已下线)2018年11月26日 《每日一题》人教选修4 - 一次电池的工作原理(已下线)2019年3月24日 《每日一题》 必修2 每周一测(已下线)2019年11月25日《每日一题》化学人教版(选修4)—— 一次电池的工作原理人教版本必修二高中化学第二章《化学反应与能量》测试卷2020届高考化学二轮复习大题精准训练——高考大题中方程式(电极、氧化还原、热化学)书写专练(已下线)1.2.2 化学电源 练习《新教材同步备课》(鲁科版选择性必修1)云南省新平一中2020-2021学年高一下学期期中考试化学试题(已下线)1.2.2 化学电源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)课后-6.1.3 设计原电池、化学电源-人教2019必修第二册湖北省襄阳市襄州区第二高级中学2021-2022学年高一下学期期中考试化学试题山东省临沂第四中学2022-2023学年高一下学期6月月考化学试题
名校
解题方法
9 . 流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4===CuSO4+PbSO4+2H2O。下列说法不正确的是( )
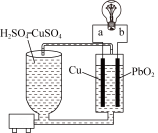

| A.a为负极,b为正极 |
| B.该电池工作时PbO2电极附近溶液的pH增大 |
| C.a极的电极反应为Cu-2e-===Cu2+ |
| D.调节电解质溶液的方法是补充CuSO4 |
您最近一年使用:0次
2016-11-15更新
|
1420次组卷
|
18卷引用:海南省万宁市北京师范大学万宁附属中学2020-2021学年高二上学期第一次月考化学试题
海南省万宁市北京师范大学万宁附属中学2020-2021学年高二上学期第一次月考化学试题2016-2017学年黑龙江大庆一中高二上10月月考化学卷2018-2019学年人教版高中化学选修四电化学基础章末综合测评题(四)甘肃省兰州市第五十八中学2018-2019学年高二(理科)第一学期期末考试化学试题云南省曲靖市富源县第六中学2019-2020学年高二上学期期末考试化学试题河南省鹤壁市高级中学2018-2019学年高一下学期精英对抗赛化学试题(已下线)1.2.2 化学电源 练习《新教材同步备课》(鲁科版选择性必修1)河北省邯郸市大名县第一中学2020-2021学年高二上学期9月月考化学试题黑龙江省大庆铁人中学2020-2021学年高二上学期第一次月考化学试题福建省连城县第一中学2020-2021学年高二上学期第一次月考化学试题福建省三明市泰宁第一中学2020-2021学年高二上学期学分认定暨第一次阶段考试化学试题河北省武安市第三中学2021届高三上学期期中考试化学试题河南省驻马店市2020-2021学年高二上学期期终考试化学试题重庆实验中学2020-2021学年高二上学期第二阶段考试化学试题宁夏平罗中学2021-2022学年高三上学期第一次月考化学试题(已下线)第12练 原电池原理及其应用-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)福建省福州第三中学2021-2022学年高三上学期第六次质量检测化学试题陕西省西安交通大学附属中学2023-2024年高二上学期第一次月考化学试题
名校
10 . 下面是利用盐桥电池从某些含碘盐中提取碘的两个装置, 下列说法中正确的是
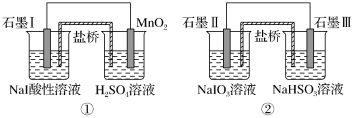

| A.两个装置中石墨I和石墨II作负极 |
| B.碘元素在装置①中被氧化,在装置②中被还原 |
| C.①中MnO2的电极反应式为:MnO2+2H2O+2e-=Mn2++4OH‑ |
| D.反应①、②中生成等量的I2时导线上通过的电子数之比为1∶5 |
您最近一年使用:0次
2016-06-27更新
|
474次组卷
|
2卷引用:2016届海南省海口中学高三全真模拟二化学试卷



