1 . 如图所示,将锌、铜通过导线相连,置于稀硫酸中。
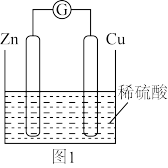
(1)锌片为____ 极,电极反应为:____ 。
(2)铜片为____ 极,电极反应为:____ 。
(3)若反应中有0.2mol电子转移,则生成的氢气在标准状况下的体积为____ 。

(1)锌片为
(2)铜片为
(3)若反应中有0.2mol电子转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
2 . 近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇(CH3OH)是其中的一个研究项目。该研究发生的主要反应如下:
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)上述反应符合原子经济性的是反应___________ (I或II)。
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是___________。
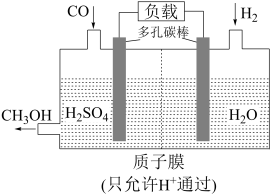
(4)H2还原CO电化学法制备甲醇(CO + 2H2 = CH3OH)的工作原理如图所示:___________ 极(填“正”或“负”),电池工作过程中H+通过质子膜向___________ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________ 。
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)(1)上述反应符合原子经济性的是反应
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
| A.恒温恒容下,再充入CO | B.升高温度 |
| C.恒温恒容下,向其中充入Ar | D.恒温恒压下,向其中充入Ar |
| A.单位时间内消耗3molH2,同时生成1mol的CH3OH |
| B.CH3OH的体积分数不再发生变化 |
| C.3v(CO2)=v(H2) |
| D.容器内气体密度不再改变 |
您最近一年使用:0次
2022-03-31更新
|
1468次组卷
|
6卷引用:重庆市主城区六校2020-2021学年高一下学期期末联考化学试题
重庆市主城区六校2020-2021学年高一下学期期末联考化学试题(已下线)【期末复习】必刷题(2)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)安徽省合肥市庐江县2021-2022学年高一下学期期末考试化学试题陕西西安三中2022-2023学年高一下学期第二次月考化学试题江苏省常州市联盟学校2022-2023学年高一下学期期末考试化学试题(已下线)综合期末压轴85+18题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
名校
解题方法
3 . 氢燃料电池是目前最具发展前景的新能源方式,如能普及并应用在车辆及其他高污染之发电工具上,将能显著减轻空气污染及温室效应。下列有关氢燃料电池的说法正确的是

| A.通入氢气的电极发生还原反应 |
| B.电解液中阳离子向通入氢气的方向移动 |
| C.正极的电极反应式为:O2+4H++4e-═2H2O |
| D.放电过程中电解液的浓度不断增大 |
您最近一年使用:0次
2022-03-29更新
|
906次组卷
|
7卷引用:福建省宁德市部分达标中学2020-2021学年高一下学期期中联合考试化学试题
名校
解题方法
4 . 锌−空气电池(原理如图所示)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时下列说法正确的是


| A.氧气在石墨电极上发生还原反应 |
| B.该电池放电时OH-向Zn电极移动 |
C.该电池的正极反应为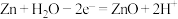 |
| D.电池工作时,电子从石墨电极经电解质溶液流向Zn电极 |
您最近一年使用:0次
2022-03-17更新
|
422次组卷
|
2卷引用:河北省武安市第一中学2020-2021学年高一下学期第二次月考化学试卷题
名校
解题方法
5 . 填空。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O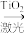 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为_______ 能;分解海水的反应属于_____ 反应(填“放热”或“吸热”)
(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式_______ 。
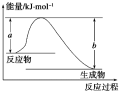
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=_______ kJ∙mol−1,x=________ 。
(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O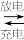 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为_____ 。
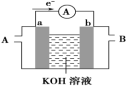
(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为______ 。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
| A.氢气分子内每个氢原子都达到稳定结构 |
| B.氢气分子的能量比两个氢原子的能量低 |
| C.1molH2离解成2molH要放出437.6kJ热量 |
| D.氢原子比氢气分子稳定 |
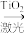 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=

(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为

您最近一年使用:0次
名校
解题方法
6 . 如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是
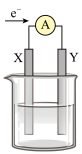

| A.电子流动方向为:X→外电路→Y→溶液→X |
| B.若两电极分别为Zn和石墨棒,则X为石墨棒,Y为Zn |
C. 移向X电极,Y电极上有氢气产生 移向X电极,Y电极上有氢气产生 |
| D.X极上发生的是还原反应,Y极上发生的是氧化反应 |
您最近一年使用:0次
2023-04-17更新
|
832次组卷
|
27卷引用:6.1.2 化学反应与电能(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
(已下线)6.1.2 化学反应与电能(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)湖南师范大学附属中学2020-2021学年高一下学期第一次月考化学试题浙江省瑞安中学2020-2021学年高一下学期期初考试化学试题山西省长治市第二中学校2020-2021学年高一下学期期中考试化学试题黑龙江省齐齐哈尔市第八中学校2020-2021学年高一下学期期中考试化学试题北京市第二十中学2020-2021学年高一下学期期末考试化学试题陕西省延安市富县高级中学2020-2021学年高一下学期期中考试化学试题【全国百强校】广西桂林市第十八中学2017-2018学年高一下学期期中考试化学试题甘肃省临泽县第一中学2017-2018学年高一下学期6月月考化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高一下学期期中联考化学试题【全国百强校】贵州省凯里市第一中学2018-2019学年高一(文)下学期期中考试化学试题湖南省株洲市2019-2020学年高一上学期期中考试化学试题陕西省咸阳市武功县普集高级中学2019-2020学年高一下学期第二次月考化学试题广西壮族自治区桂林市第十八中学2019-2020学年高一下学期期中考试化学试题新疆巴音郭楞蒙古自治州库尔勒市2017-2018学年高一下学期期末考试化学试题辽宁省抚顺县高级中学2019-2020学年高一下学期期中网课学习质量检测化学试题甘肃省武威市民勤县第四中学2021届高三上学期期末考试(实验班)化学试题(已下线)第06讲 化学电源-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)湖南省长沙市第一中学2021-2022学年高一下学期期中考试化学试题海南省屯昌县屯昌中学2021-2022学年高一下学期期中考试化学试题北京市第一六一中学2021-2022学年高一下学期期中阶段(选考班)化学试题宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题安徽省黄山市屯溪第一中学2022-2023学年高一下学期4月期中考试化学试题6.3.1化学能转化为电能(课后)-2019苏教版必修2课前课中课后河北省邢台市第二中学2020-2021学年高二上学期开学摸底考试化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二3月月考化学试题新疆维吾尔自治区喀什第二中学2023-2024学年高二上学期开学测试化学试题
名校
解题方法
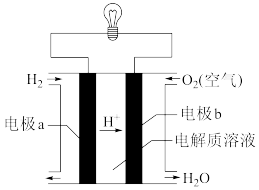
7 . 燃料电池是一种高效、环境友好的发电装置,某氢氧燃料电池的构造示意图如下,该电池工作时,下列说法正确的是
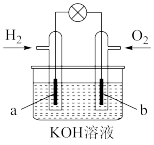
| A.O2在b电极上发生氧化反应 |
| B.电解质溶液中OH-向正极移动 |
| C.该装置实现了电能到化学能的转化 |
| D.氢氧燃料电池是一种具有应用前景的绿色电源 |
您最近一年使用:0次
2022-02-27更新
|
3361次组卷
|
10卷引用:广东省潮州市潮安区2020-2021学年高一上学期期末考试化学试题
广东省潮州市潮安区2020-2021学年高一上学期期末考试化学试题(已下线)第12讲 化学电池(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)江西省萍乡市芦溪中学2021-2022学年高一下学期3月月考化学试题(已下线)【知识图鉴】单元讲练测必修第二册第六单元03巩固练第六章 化学反应与能量(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第六章 化学反应与能量【单元测试B卷】(已下线)专题05 化学反应与能量变化(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)辽宁省大连市庄河市高级中学2022-2023学年高三上学期12月月考化学(B卷)试题湖南省株洲市南方中学2023届高三上学期第一次月考化学试题河南省周口市沈丘县长安高级中学2022-2023学年高三上学期第二次月考化学试题
解题方法
8 . 完成下列问题。
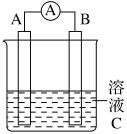
(1)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如下图所示的原电池装置。则A(正极)极材料为___________ ,B(负极)极材料为___________ ,溶液C为___________ ,A(正极)电极上发生反应的类型为___________ (填“氧化”或“还原”)反应,B(负极)电极上发生的电极反应为___________ ,当有1.6g铜溶解时,通过外电路的电子的物质的量为___________ 。___________ (填“正”或“负”)极,该电池正极的电极反应式为___________ 。
(1)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如下图所示的原电池装置。则A(正极)极材料为
您最近一年使用:0次
2022-02-27更新
|
740次组卷
|
5卷引用:广东省潮州市潮安区2020-2021学年高一上学期期末考试化学试题
广东省潮州市潮安区2020-2021学年高一上学期期末考试化学试题(已下线)【期末复习】必刷题(2)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)陕西省汉中市2021-2022学年高一下学期期末联考化学试题(已下线)期末模拟题(一)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)(已下线)重难点03 原电池原理的应用与化学电源-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
名校
解题方法
9 . 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 | D.产生气泡的速度甲比乙慢 |
您最近一年使用:0次
2024-01-13更新
|
130次组卷
|
3卷引用:广东省普通高中2020-2021学年高一学业水平合格性考试(会考)化学模拟测试卷(三)
名校
解题方法
10 . 锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应式是Li+MnO2=LiMnO2。下列说法正确的是
| A.Li是负极,电极反应为Li-e-=Li+ |
| B.Li是正极,电极反应为Li+e-=Li- |
C.MnO2是负极,电极反应为MnO2+e-=MnO |
| D.Li是负极,电极反应为Li-2e-=Li2+ |
您最近一年使用:0次
2023-03-17更新
|
716次组卷
|
11卷引用:河北省唐山市英才国际学校2020-2021学年高一下学期期中考试化学试题
河北省唐山市英才国际学校2020-2021学年高一下学期期中考试化学试题2020年人教版高中化学必修2第二章《化学反应与能量》测试卷2(已下线)专题05 化学能与电能(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)吉林省长春市实验中学2019-2020学年高一下学期期末考试化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高一下学期期中考试化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高二上学期期中联考化学试题河北省邢台市第二中学2019-2020学年高二上学期期中考试化学试题黑龙江省绥化市青冈县第一中学2020-2021学年高二上学期开学考试化学试题(已下线)专题五 锂电池和锂离子电池(练习)宁夏银川市唐徕中学2022-2023学年高二下学期3月月考化学试题(已下线)题型16 锂电池和锂离子电池的应用



