1 . 硼化钒(VB2)—空气电池是目前储电能力最高的电池,工作原理如图所示,该电池工作时反应为: 4VB2+11O2 = 4B2O3+2V2O5。不正确 的是
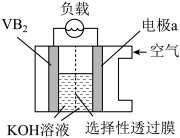
| A.电极a发生还原反应 |
| B.电流由电极a经负载流向VB2极 |
| C.VB2极发生的电极反应为:2VB2 +22OH−-22e−=V2O5+2B2O3 +11H2O |
| D.图中选择性透过膜允许阳离子选择性透过 |
您最近一年使用:0次
名校
解题方法
2 . 有关下列四个常用电化学装置的叙述中,正确的是
 | 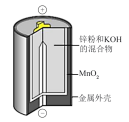 | 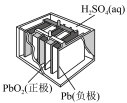 | 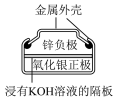 |
| 图1碱性锌锰电池 | 图2普通锌锰电池 | 图3铅酸蓄电池 | 图4银锌纽扣电池 |
| A.图1所示电池中,MnO2的作用是作氧化剂 |
| B.图2所示电池中,电子从锌筒出发沿导线经电解质溶液流向石墨电极 |
| C.图3所示装置工作过程中,负极的质量逐渐减少 |
| D.图4所示电池中,Zn是还原剂,在电池工作过程中被还原 |
您最近一年使用:0次
名校
解题方法
3 . 采用强碱性电解质的3D-Zn-NiOOH二次电池结构如图所示。电池反应为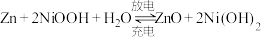 。下列说法不正确的是
。下列说法不正确的是

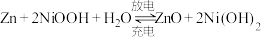 。下列说法不正确的是
。下列说法不正确的是
| A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高 |
B.充电时阳极反应为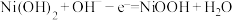 |
C.放电时负极反应为 |
| D.放电过程中OH-通过隔膜从正极区移向负极区 |
您最近一年使用:0次
名校
解题方法
4 . Mg-H2O2电池可用于驱动无人驾收的潜航器。该电池以海水为电解质资液,示意图如图,该电池工作时,下列说法不正确的是
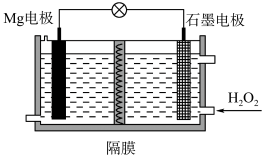

| A.Mg电极是该电池的负极 |
| B.溶液中Cl-向正极移动 |
| C.石墨电极附近溶液的pH增大 |
| D.若在石墨电极区加入一定量盐酸,则发生的电极反应式为:2H++H2O2+2e-=2H2O |
您最近一年使用:0次
名校
解题方法
5 . 一种电化学装置的工作原理:首先,太阳能转化为电能,先对碱性镍铁二次电池充电,实现电能储存;当镍铁电池充电完成后,过剩的电能再接着用于电解水,实现氢能储存。下列说法不正确的是


A.镍铁电池充电时, 从B电极移向A电极 从B电极移向A电极 |
B.镍铁电池充电完成后,继续通电所产生的气体Ⅰ为 |
C.镍铁电池放电时理论上每消耗0.1molNiOOH,Fe失去电子数为 |
D.镍铁电池放电时,正极附近溶液的 增大 增大 |
您最近一年使用:0次
2023-11-05更新
|
366次组卷
|
2卷引用:江苏省徐州市第一中学2023-2024学年高二上学期期中考试化学试题
名校
6 . 碱性Na2Sx—空气二次电池可用于储能,其放电时工作原理如图所示。下列说法不正确 的是


| A.离子交换膜a为阳离子交换膜 |
| B.放电时Ⅲ室中NaOH溶液的浓度减小 |
C.放电时的负极反应为2 - 2e-= - 2e-= 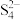 |
| D.使用储液罐可储存与释放更多能量 |
您最近一年使用:0次
2023-07-13更新
|
376次组卷
|
2卷引用:江苏省扬州市2022-2023学年高二下学期开学考试化学试题
7 . γ-丁内酯为无色油状液体,高温时易分解,是重要的化工原料和医药中间体。工业利用1,4-丁二醇生产γ-丁内酯的主、副反应的化学方程式如下:
主反应: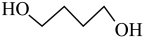 (g)
(g)
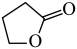 (g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
(g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
副反应: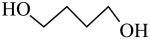 (g)
(g)
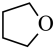 (g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(1)反应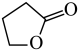 (g)+2H2(g)
(g)+2H2(g)
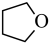 (g)+H2O(g)的△H=
(g)+H2O(g)的△H=_______ kJ•mol-1。
(2)由1,4-丁二醇合成γ-丁内酯的一种机理如图所示(“★”表示此微粒吸附在催化剂表面)
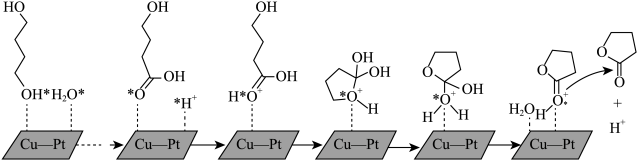
①步骤Ⅱ历程是质子化的过程,H+和氧原子间形成的作用力是______ 。
②H+在上述合成γ-丁内酯过程中的作用是_______ 。
③γ-丁内酯分子中σ键与π键数目之比为_______ 。
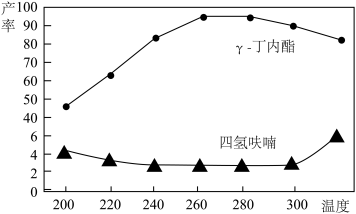
(3)将1,4-丁二醇与H2的混合气体以一定流速通过填充有催化剂的反应器,反应相同时间,测得γ-丁内酯和四氢呋喃的产率如图所示。
已知:1,4-丁二醇的沸点为228℃。
①当温度低于220℃,1,4-丁二醇的转化率较低,可能的原因是_______ 。
②当温度高于260℃,γ-丁内酯的产率下降,可能的原因是_______ 。
(4)铜基催化剂(Cu/Pt)能高效加快由1.4-丁二醇合成γ-丁内酯的合成速率,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。
①1,4-丁二醇中混有少量的1,4-丁二硫醇(HSCH2CH2CH2CH2SH)。合成时加入ZnO可有效避免铜基催化剂失活,其原理用化学反应方程式表示为_______ 。
②将失活的铜基催化剂分为两份,第一份直接在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化剂活性恢复。说明催化剂失活的另外可能的原因是______ 。
(5)含有1,4-丁二醇的强酸性污水可用“铁碳微电池”法处理,过程中两电极分别产生的Fe2+和活性氢原子(H•)都具有较高的化学活性,在厌氧条件下将1,4-丁二醇转化为甲烷,假设两电极只生成Fe2+和H•,且全部参与该转化过程,写出该过程的离子方程式:_______ 。
主反应:
 (g)
(g)
 (g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
(g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1副反应:
 (g)
(g)
 (g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1(1)反应
 (g)+2H2(g)
(g)+2H2(g)
 (g)+H2O(g)的△H=
(g)+H2O(g)的△H=(2)由1,4-丁二醇合成γ-丁内酯的一种机理如图所示(“★”表示此微粒吸附在催化剂表面)

①步骤Ⅱ历程是质子化的过程,H+和氧原子间形成的作用力是
②H+在上述合成γ-丁内酯过程中的作用是
③γ-丁内酯分子中σ键与π键数目之比为
(3)将1,4-丁二醇与H2的混合气体以一定流速通过填充有催化剂的反应器,反应相同时间,测得γ-丁内酯和四氢呋喃的产率如图所示。
已知:1,4-丁二醇的沸点为228℃。
①当温度低于220℃,1,4-丁二醇的转化率较低,可能的原因是
②当温度高于260℃,γ-丁内酯的产率下降,可能的原因是

(4)铜基催化剂(Cu/Pt)能高效加快由1.4-丁二醇合成γ-丁内酯的合成速率,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。
①1,4-丁二醇中混有少量的1,4-丁二硫醇(HSCH2CH2CH2CH2SH)。合成时加入ZnO可有效避免铜基催化剂失活,其原理用化学反应方程式表示为
②将失活的铜基催化剂分为两份,第一份直接在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化剂活性恢复。说明催化剂失活的另外可能的原因是
(5)含有1,4-丁二醇的强酸性污水可用“铁碳微电池”法处理,过程中两电极分别产生的Fe2+和活性氢原子(H•)都具有较高的化学活性,在厌氧条件下将1,4-丁二醇转化为甲烷,假设两电极只生成Fe2+和H•,且全部参与该转化过程,写出该过程的离子方程式:
您最近一年使用:0次
解题方法
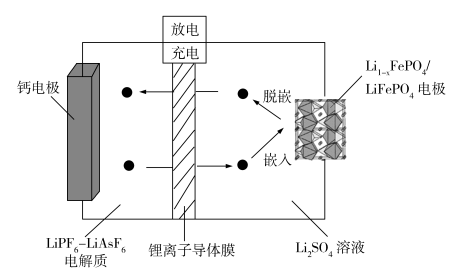
8 . 一款新型的Ca-LiFePO4可充电电池的工作示意图如图,锂离子导体膜只允许Li+通过。该电池总反应式为:xCa2++2LiFePO4 xCa+2Li1-xFePO4+2xLi+。下列说法
xCa+2Li1-xFePO4+2xLi+。下列说法不正确 的是
 xCa+2Li1-xFePO4+2xLi+。下列说法
xCa+2Li1-xFePO4+2xLi+。下列说法
| A.充电时,钙电极与直流电源的负极相连 |
| B.充电时,每转移0.2mol电子左室中电解质的质量减轻4.0g |
| C.Li1-xFePO4/LiFePO4电极充电时发生Li+脱嵌,放电时发生Li+嵌入 |
| D.放电时,正极反应为:Li1-xFePO4+xe-+xLi+=LiFePO4 |
您最近一年使用:0次
9 . 2023年1月31日常州氢湾在“两湖”创新区核心区正式启动,有百利科技等生产氢燃料电池零部件的8家高科技企业落户氢湾。某生物燃料电池以 和
和 为原料可在一定温度下制取
为原料可在一定温度下制取 ,电池中含有固氮酶和氢化酶两种蛋白酶,工作原理如图。下列说法正确的是
,电池中含有固氮酶和氢化酶两种蛋白酶,工作原理如图。下列说法正确的是

 和
和 为原料可在一定温度下制取
为原料可在一定温度下制取 ,电池中含有固氮酶和氢化酶两种蛋白酶,工作原理如图。下列说法正确的是
,电池中含有固氮酶和氢化酶两种蛋白酶,工作原理如图。下列说法正确的是
| A.a电极是燃料电池的正极 |
B.电极b的电极反应式为: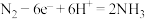 |
| C.该电池适宜在高温下使用 |
| D.电池工作时氢离子通过交换膜由a极区向b极区移动 |
您最近一年使用:0次
解题方法
10 . 钴酸锂( )电池放电时的反应为
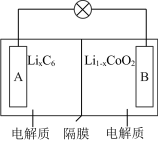
)电池放电时的反应为 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是
 )电池放电时的反应为
)电池放电时的反应为 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是
| A.放电时,电能主要转化为化学能 |
B.放电时, 由A极脱出,通过隔膜后嵌入B极 由A极脱出,通过隔膜后嵌入B极 |
C.充电时,B极的电极反应式为 |
D.充电时,理论上若转移 ,A极将增重 ,A极将增重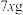 |
您最近一年使用:0次



