1 . 一种水性电解液Zn-MnO2离子选择双隔膜的二次电池如图所示(KOH溶液中, 以
以 存在)。下列叙述错误的是
存在)。下列叙述错误的是

 以
以 存在)。下列叙述错误的是
存在)。下列叙述错误的是
A.放电时,Ⅱ区的 通过隔膜向Ⅰ区迁移 通过隔膜向Ⅰ区迁移 |
B.放电时,负极的电极反应: |
| C.充电时,阳极区溶液的pH会减小 |
D.充电时,电路中转移1 mol  ,则Ⅱ区溶质质量减少87 g ,则Ⅱ区溶质质量减少87 g |
您最近半年使用:0次
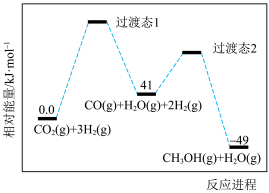
2 . 甲醇是一种基本的有机化工原料,用途十分广泛。应用CO2催化加氢规模化生产甲醇是综合利用CO2,实现“碳达峰”的有效措施之一、我国科学家研究发现二氧化碳电催化还原制甲醇的反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H,需通过以下两步实现:
I.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) △H2
反应过程中各物质的相对能量变化情况如图所示。
(1)
_______ ,稳定性:过渡态1_______ 过渡态2(填“大于”“小于”或“等于”)。
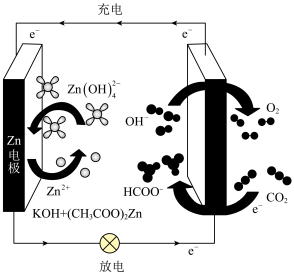
(2)基于催化剂 的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为
的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为_______ ,若电池工作t min,Zn电极的质量变化为 ,则理论上消耗CO2的物质的量为
,则理论上消耗CO2的物质的量为_______ 。
(3)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有 )的原理示意图如下图所示。
)的原理示意图如下图所示。

①M极的电极反应式为_______ ,N极附近的pH_______ (填“变大”或“变小”或“不变”)。
②写出电解池中 转化为Cr3+的离子方程式
转化为Cr3+的离子方程式_______ 。
I.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) △H2
反应过程中各物质的相对能量变化情况如图所示。

(1)

(2)基于催化剂
 的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为
的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为 ,则理论上消耗CO2的物质的量为
,则理论上消耗CO2的物质的量为
(3)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有
 )的原理示意图如下图所示。
)的原理示意图如下图所示。
①M极的电极反应式为
②写出电解池中
 转化为Cr3+的离子方程式
转化为Cr3+的离子方程式
您最近半年使用:0次
名校
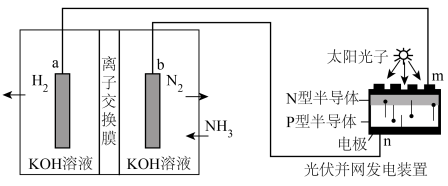
3 . 利用光伏并网发电装置电解 得到高纯度
得到高纯度 的装置如图所示。下列说法正确的是
的装置如图所示。下列说法正确的是
 得到高纯度
得到高纯度 的装置如图所示。下列说法正确的是
的装置如图所示。下列说法正确的是
| A.m极电势高于n极电势 |
| B.离子交换膜最好为阳离子交换膜 |
C.b电极的电极反应式为: |
D.电解产生2.24L 时导线中通过0.2mol电子 时导线中通过0.2mol电子 |
您最近半年使用:0次
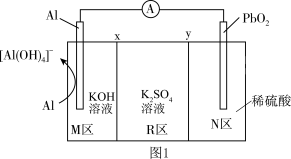
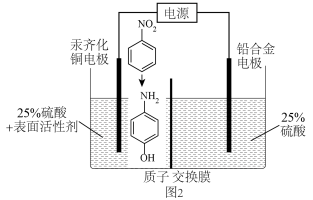
4 . 对氨基苯酚可用作农药、医药、染料等精细化学品的中间体,利用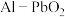 电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中
电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中 溶液浓度增大,下列说法错误的是
溶液浓度增大,下列说法错误的是
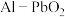 电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中
电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中 溶液浓度增大,下列说法错误的是
溶液浓度增大,下列说法错误的是

A. 通过 通过 膜移向 膜移向 区 区 |
B.铅合金电极应与 电极相连 电极相连 |
C.消耗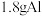 时, 时, 区域电解质溶液质量减少 区域电解质溶液质量减少 |
D.汞齐化铜电极的反应式为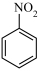 +4H++4e- +4H++4e- 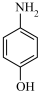 +H2O +H2O |
您最近半年使用:0次
名校
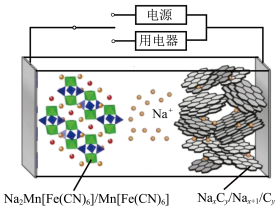
5 . 2023年星恒电源发布“超钠F1”开启钠电在电动车上产业化元年。该二次电池的电极材料为 (普鲁士白)和
(普鲁士白)和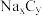 (嵌钠硬碳)。下列说法错误的是
(嵌钠硬碳)。下列说法错误的是
 (普鲁士白)和
(普鲁士白)和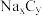 (嵌钠硬碳)。下列说法错误的是
(嵌钠硬碳)。下列说法错误的是
| A.放电时,左边电极电势高 |
B.放电时,负极的电极反应式可表示为: |
C.充电时,用铅酸蓄电池作电源,负极质量增重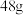 ,则阳极质量增加 ,则阳极质量增加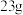 |
| D.其他条件相同时,锂离子电池比能量高于钠离子电池 |
您最近半年使用:0次
6 . 某科研小组用氢氧燃料电池提供的电能电解处理含 的酸性废水,设计如图所示装置。下列说法正确的是
的酸性废水,设计如图所示装置。下列说法正确的是
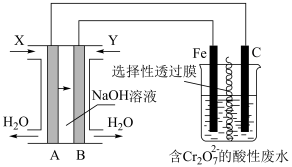
已知:① ;
;
② 和
和 最终转化为
最终转化为 和
和 沉淀除去。
沉淀除去。
 的酸性废水,设计如图所示装置。下列说法正确的是
的酸性废水,设计如图所示装置。下列说法正确的是
已知:①
 ;
;②
 和
和 最终转化为
最终转化为 和
和 沉淀除去。
沉淀除去。| A.气体X为氧气,气体Y为氢气 |
B.该燃料电池负极的电极反应式为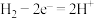 |
C.若选择性透过膜为阴离子交换膜,则 、 、 沉淀在铁极附近产生 沉淀在铁极附近产生 |
D.理论上除去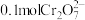 ,消耗3.36L氧气(标准状况) ,消耗3.36L氧气(标准状况) |
您最近半年使用:0次
解题方法
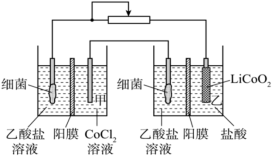
7 . 近年来随着电动汽车的普及,电池企业开始大力发展锂电池回收业务。现设计如图装置回收锂电池中的金属钴,电极材料均为石墨,右侧装置为原电池。工作时,细菌降解乙酸盐生成 ,废旧锂电池的正极材料
,废旧锂电池的正极材料 转化为
转化为 ,一段时间后可将乙室溶液转入到甲室。下列说法错误的是
,一段时间后可将乙室溶液转入到甲室。下列说法错误的是
 ,废旧锂电池的正极材料
,废旧锂电池的正极材料 转化为
转化为 ,一段时间后可将乙室溶液转入到甲室。下列说法错误的是
,一段时间后可将乙室溶液转入到甲室。下列说法错误的是
A.装置工作时, 溶液一侧石墨电极的电势低于乙室中 溶液一侧石墨电极的电势低于乙室中 电极的电势 电极的电势 |
B.乙酸盐发生的电极反应式为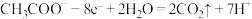 |
| C.装置工作一段时间后,乙室应该补充盐酸 |
D.若甲室回收得到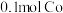 时,理论上乙室参加反应的 时,理论上乙室参加反应的 也为 也为 |
您最近半年使用:0次
名校
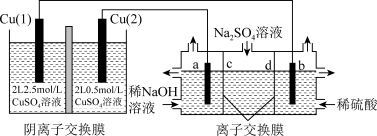
8 . 相同金属在其不同浓度盐溶液中可形成浓差电池。如图所示装置是利用浓差电池电解 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、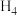 、
、 和
和 。下列说法正确的是
。下列说法正确的是
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、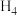 、
、 和
和 。下列说法正确的是
。下列说法正确的是
A.电池放电过程中, 作正极,电极反应为 作正极,电极反应为 |
| B.c、d离子交换膜依次为阳离子交换膜和阴离子交换膜 |
C.a为电解池的阳极,电极反应为 |
D.电池从开始工作到停止放电,电解池理论上可制得 |
您最近半年使用:0次
名校
解题方法
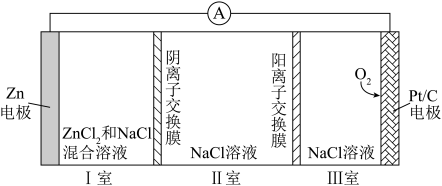
9 . 2023年杭州亚运会期间使用的部分电子展示板中用到了一种可充电锌—空气电池,该电池放电时的工作原理如下图所示。下列说法错误的是 的形式存在,并存在电离平衡
的形式存在,并存在电离平衡 。
。
 的形式存在,并存在电离平衡
的形式存在,并存在电离平衡 。
。A.放电时,Ⅰ室溶液中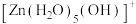 浓度增大 浓度增大 |
| B.放电时,若将Ⅱ室中的溶液换成海水,则一段时间后,可将海水适度淡化 |
C.充电时, 电极附近可能有 电极附近可能有 产生 产生 |
D.充电时,每生成 ,Ⅲ室溶液质量理论上减少 ,Ⅲ室溶液质量理论上减少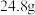 |
您最近半年使用:0次
2024-01-26更新
|
75次组卷
|
2卷引用:湖北省宜荆荆随恩2023-2024学年高二上学期12月联考化学试题
10 . 氯碱工业的一种节能新工艺是将电解池与燃料电池相结合,相关物料的传输与转化关系如图所示(电极未标出)。下列说法错误的是
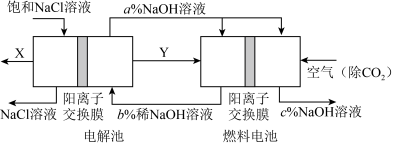
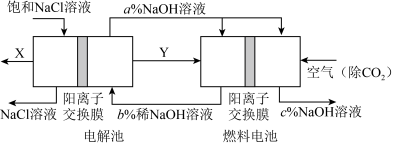
| A.电解池的阴极反应式为:2H2O+2e-═H2↑+2OH- |
| B.通入空气的电极为正极,电极反应为:O2+2H2O+4e-=4OH- |
| C.电解池中产生2molCl2时,理论上燃料电池中消耗1molO2 |
| D.a、b、c的大小关系为:c>b>a |
您最近半年使用:0次



