1 . 随着能源结构的改变,甲醇将成为21世纪具有竞争力的清洁能源,工业上常利用CO或 来生产甲醇。回答下列问题:
来生产甲醇。回答下列问题:
(1)二氧化碳加氢制甲醇时,一般认为可通过如下步骤来实现:
第一步:

第二步:

① 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
②若第一步为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
A.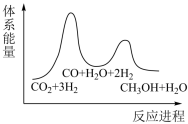 B.
B.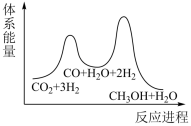 C.
C.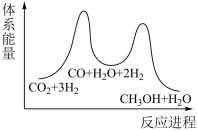 D.
D.
(2)气态甲醇用作燃料时,可发生如下两个反应:

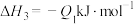

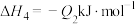
则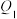
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)某同学设计了如下电化学装置,利用 制取甲醇。
制取甲醇。
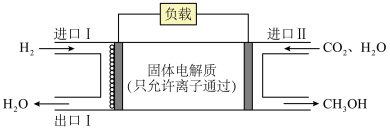
①固体电解质采用___________ (填“氧离子导体”或“质子导体”)。
②正极的电极反应式为___________ 。
(4)利用可再生能源电还原 制取甲醇的装置如下图所示,高浓度的
制取甲醇的装置如下图所示,高浓度的 用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为
用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为___________ ,当制得 时,标准状况下理论上阳极产生的气体体积为
时,标准状况下理论上阳极产生的气体体积为___________ 。

 来生产甲醇。回答下列问题:
来生产甲醇。回答下列问题:(1)二氧化碳加氢制甲醇时,一般认为可通过如下步骤来实现:
第一步:


第二步:


①
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为②若第一步为慢反应,下列示意图中能体现上述反应能量变化的是
A.
 B.
B. C.
C. D.
D.
(2)气态甲醇用作燃料时,可发生如下两个反应:

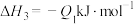

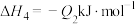
则
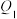
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)某同学设计了如下电化学装置,利用
 制取甲醇。
制取甲醇。
①固体电解质采用
②正极的电极反应式为
(4)利用可再生能源电还原
 制取甲醇的装置如下图所示,高浓度的
制取甲醇的装置如下图所示,高浓度的 用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为
用于抑制酸性电解液中的析氢反应来提高甲醇的生成率,Cu电极上发生的电极反应为 时,标准状况下理论上阳极产生的气体体积为
时,标准状况下理论上阳极产生的气体体积为
您最近一年使用:0次
2024-02-14更新
|
83次组卷
|
2卷引用:新疆乌鲁木齐市第101中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
2 . 请按要求回答下列问题。
(1) ,
, 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度约为
浓度约为______  。
。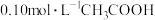 溶液加适量的水稀释,下列表达式的数值变大的是
溶液加适量的水稀释,下列表达式的数值变大的是______ (填标号)。
A. B.
B. C.
C. D.
D.
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是________(填标号)。
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。
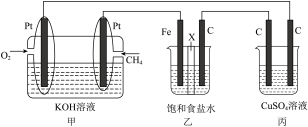
①甲装置中负极反应式为________ 。
②乙装置中石墨电极上生成的气体为________ (填化学式)。
③丙装置中 足量,工作一段时间后,溶液的
足量,工作一段时间后,溶液的
________ (填“变大”、“变小”或“不变”),反应的化学方程式为________ ,若要将电解后的溶液复原,需加入一定量的________ (填化学式)。
(1)
 ,
, 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度约为
浓度约为 。
。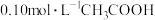 溶液加适量的水稀释,下列表达式的数值变大的是
溶液加适量的水稀释,下列表达式的数值变大的是A.
 B.
B. C.
C. D.
D.
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是________(填标号)。
A.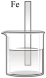 | B. | C.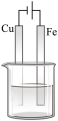 | D.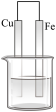 |

①甲装置中负极反应式为
②乙装置中石墨电极上生成的气体为
③丙装置中
 足量,工作一段时间后,溶液的
足量,工作一段时间后,溶液的
您最近一年使用:0次
2023-02-13更新
|
844次组卷
|
6卷引用:新疆乌鲁木齐市高级中学2023-2024学年高二上学期1月期末化学试题



