解题方法
1 . 如下图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
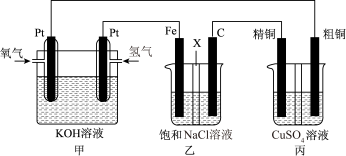
根据要求回答相关问题:
(1)通入氧气的电极为________ (填“正极”或“负极”),负极的电极反应式为______________ 。
(2)铁电极为________ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______________ 。
(3)反应一段时间后,乙装置中生成氢氧化钠主要在________ 区。(填“铁极”或“石墨极”)
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将________ (填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为________ ;丙装置中阴极析出铜的质量为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)反应一段时间后,乙装置中生成氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
您最近一年使用:0次
2016-12-09更新
|
161次组卷
|
5卷引用:河北省鸡泽县第一中学2016-2017学年高一下学期期中考试化学试题
河北省鸡泽县第一中学2016-2017学年高一下学期期中考试化学试题(已下线)2011-2012学年辽南协作体高二上学期期中考试化学试卷2015-2016学年山东省淄博六中高二上学期期末化学试卷河南省郑州市中牟县二中2017-2018学年高二第一次月考化学试题黑龙江省嫩江市第一中学2021-2022学年高二下学期开学考试化学试题
名校
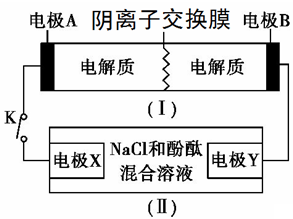
2 . 装置(Ⅰ)为铁镍(Fe-Ni)可充电电池:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
 Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,Y附近溶液先变红。下列说法正确的是
| A.闭合K时,X的电极反应式为:2H++2e-= H2↑ |
| B.闭合K时,A电极反应式为:NiO2+2e-+2H+= Ni(OH)2 |
| C.给装置(Ⅰ)充电时,B极参与反应的物质被氧化 |
| D.给装置(Ⅰ)充电时,OH- 通过阴离子交换膜,移向A电极 |
您最近一年使用:0次
2016-12-09更新
|
478次组卷
|
6卷引用:河北省唐山一中2017-2018学年高一下学期期中考试化学试题
解题方法
3 . 下列关于电化学的说法中错误的是
| A.原电池的负极、电解池的阳极均发生氧化反应 |
| B.原电池将化学能转化为电能,电解池将电能转化为化学能 |
| C.电解水制取H2和O2时,为了增强导电性,可加入NaOH、NaCl、H2SO4 |
| D.利用原电池原理可制备化学电源,利用电解池原理可制备化学物质 |
您最近一年使用:0次
2016-12-09更新
|
414次组卷
|
3卷引用:2014-2015江西省白鹭洲中学高一下学期期中考试化学试卷
名校
4 . 碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
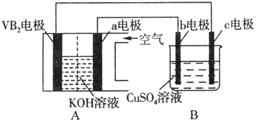

| A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,c电极表面先有红色物质析出,后有气泡产生 |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
您最近一年使用:0次
2016-12-09更新
|
328次组卷
|
4卷引用:浙江省宁波市效实中学2015-2016学年高一下期中化学卷
名校
5 . 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
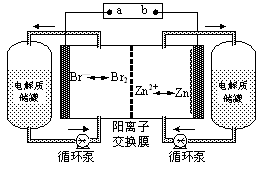

| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
您最近一年使用:0次
2016-12-09更新
|
727次组卷
|
7卷引用:2015-2016学年辽宁省沈阳二中高一下期中化学试卷
2015-2016学年辽宁省沈阳二中高一下期中化学试卷(已下线)2013-2014江苏省南通市高三第三次调研测试化学试卷(已下线)2013-2014江苏省淮安市高三第三次调研测试化学试卷(已下线)2013-2014广东省广州市越秀区高二下学期期末水平调研化学试卷2015届江苏省扬州中学高三4月双周测化学试卷2016届安徽省六安一中高三下学期综合训练(三)理综化学试卷云南省丽江市宁蒗县第一中学2019—2020学年高二上学期期末考试化学试题
2013·湖北荆州·一模
名校
解题方法
6 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业的原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
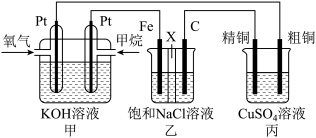
(1)甲烷燃料电池负极反应式为________________________ 。
(2)石墨(C)极的电极反应式为_______________________ 。
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成的气体的体积为________ L;丙装置中阴极析出铜的质量为________ g。
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。
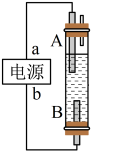
若用于制漂白液,a为电池的________ 极,电解质溶液最好用)________________
若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用________ 作电极。

(1)甲烷燃料电池负极反应式为
(2)石墨(C)极的电极反应式为
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成的气体的体积为
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。

若用于制漂白液,a为电池的
若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用
您最近一年使用:0次
2016-12-09更新
|
936次组卷
|
9卷引用:2013-2014浙江省温州中学高一下学期期中化学试卷
(已下线)2013-2014浙江省温州中学高一下学期期中化学试卷内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期期中考试化学试题(已下线)2013届湖北省荆州市高三毕业班质量检查(Ⅰ)化学试卷(已下线)2014届高考化学二轮冲刺非选择题增分专练 基本概念、基本理论练习卷(已下线)二轮复习 专题10 电化学及其应用 押题专练(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(押题专练)河北省大名县第一中学2019-2020学年高二9月月考化学试题河北省邯郸大名一中2019-2020学年高二上学期第一次月考化学试题河南省开封市五县2021-2022学年高二上学期期末考试化学试题
名校
解题方法
7 . 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2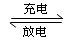 Cd+2NiOOH+2H2O,由此可知,该电池充电时的阴极材料是
Cd+2NiOOH+2H2O,由此可知,该电池充电时的阴极材料是
 Cd+2NiOOH+2H2O,由此可知,该电池充电时的阴极材料是
Cd+2NiOOH+2H2O,由此可知,该电池充电时的阴极材料是| A.Cd(OH)2 | B.Ni(OH)2 | C.Cd | D.NiOOH |
您最近一年使用:0次
2016-12-09更新
|
816次组卷
|
16卷引用:2014-2015江西省临川市一中高一下学期期中考试化学试卷
2014-2015江西省临川市一中高一下学期期中考试化学试卷(已下线)2013-2014四川省雅安中学下学期期中考试高二化学试卷2014-2015学年福建省晋江市平山中学高二下学期期中考试化学试卷福建省三明市三地三校2017-2018学年高二上学期期中联考化学试题(已下线)2010年福建省福州八中高二第二学期期末考试化学试题(已下线)2010-2011学年江苏省南京六中高二下学期期末考试化学试题(已下线)2011-2012学年福建省龙岩一中上学期高二期末考试化学试卷(已下线)2012-2013学年黑龙江省庆安三中高二上学期期末考试化学试卷2014-2015甘肃省白银市会宁县五中高二上学期期末化学试卷2014-2015河北省邯郸市高二上学期期末考试化学试卷2014-2015内蒙古赤峰市宁城县高二上学期期末考试化学试卷2015-2016学年贵州省凯里一中高二上学期期末化学试卷2015-2016学年吉林省长春外国语学校高二上学期期末化学试卷2015-2016学年安徽省阜阳市太和八中高二上学期期末理化学试卷湖南省醴陵市第一中学2018-2019学年高二上学期入学考试化学试题云南省峨山彝族自治县第一中学2018-2019学年高二6月月考化学试题
10-11高一下·浙江温州·期中
8 . 电化学原理在化学工业中有广泛应用。请根据下图回答有关问题
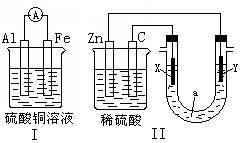
(1)装置I中能量的转化形式是_________ 。导线上电子定向移动方向从____ 极到____ 极。其电极反应式______________________________ 。
(2)装置II中若X、Y都是惰性电极,a是CuCl2溶液。则发生氧化反应的电极是_____ 和_____ 。检验X电极反应产物的方法是_________________________ 。
若a是饱和NaCl溶液(氯碱工业生产原理),电极材料是石墨电极和铁电极。实验开始时,同时在两极各滴入几滴酚酞试液,则_______ (填“石墨或铁”)附近溶液先变红,其电极反应式__________________________________________ 。
(3)当装置I和装置II的电路中均转移0.2mol电子时,则装置I中铁电极质量的变化
_______ g(填写“增加”或“减少”及具体质量),装置II中收集到的气体共有_____ L(标准状况下)(以装置II中X、Y是惰性电极,a是CuCl2溶液计算)。

(1)装置I中能量的转化形式是
(2)装置II中若X、Y都是惰性电极,a是CuCl2溶液。则发生氧化反应的电极是
若a是饱和NaCl溶液(氯碱工业生产原理),电极材料是石墨电极和铁电极。实验开始时,同时在两极各滴入几滴酚酞试液,则
(3)当装置I和装置II的电路中均转移0.2mol电子时,则装置I中铁电极质量的变化
您最近一年使用:0次
9-10高一下·辽宁·期中
9 . 如右图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,电流表指针发生偏转,以下表述不正确的是
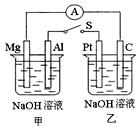

| A.甲池发生了原电池反应 |
| B.Mg是正极 |
| C.乙烧杯中可以用乙醇代替氢氧化钠溶液,电流表仍会偏转 |
| D.甲池pH逐渐减小 |
您最近一年使用:0次
名校
10 . 关于下图所示各装置的叙述中,正确的是


| A.装置①是原电池,总反应是:Cu + 2Fe3+= Cu2++ 2Fe2+ |
| B.装置①中,铁做负极,电极反应式为:Fe3++ e-= Fe2+ |
| C.装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深 |
| D.若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
您最近一年使用:0次
2016-12-09更新
|
546次组卷
|
7卷引用:陕西省西安市铁一中2017-2018学年高一下学期期中考试化学试题
陕西省西安市铁一中2017-2018学年高一下学期期中考试化学试题(已下线)2010年河北省正定中学高二第二学期期中考试化学试题福建省三明市三地三校2017-2018学年高二上学期期中联考化学试题(已下线)高三模拟考试化学试题(已下线)2014届甘肃省玉门市油田一中高三第三次摸底考试化学试卷甘肃省酒泉市敦煌中学2020届高三上学期第二次调研考试化学试题云南省第一民族中学2021-2022学年高三下学期2月份开学测试化学试题



