名校
1 . 二甲醚(CH3OCH3)直接燃料电池具有启动快、效率高等优点,用二甲醚燃料电池电解甲基肼(CH3—NH—NH2)制氢的装置如图所示,其中X、Y、M、N均为惰性电极。下列说法不正确的是


A.M极的电极反应式为CH3—NH—NH2+12OH−-10e− CO32-+N2↑+9H2O CO32-+N2↑+9H2O |
| B.乙中的交换膜是阴离子交换膜,OH−透过交换膜向M极移动 |
| C.若忽略水的消耗与生成,甲中电解质溶液的pH减小,乙中电解质溶液的pH增大 |
| D.理论上,标况下当生成6.72 L H2时,消耗CH3OCH3的质量为2.3 g |
您最近一年使用:0次
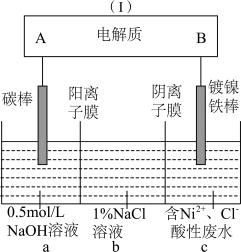
2 . 装置为锂钒氧化物二次电池,其成本较低,且对环境无污染:V2O5+xLi LixV2O5;在下图中用该电池电解含镍酸性废水可得到单质镍。下列说法正确的是
LixV2O5;在下图中用该电池电解含镍酸性废水可得到单质镍。下列说法正确的是
 LixV2O5;在下图中用该电池电解含镍酸性废水可得到单质镍。下列说法正确的是
LixV2O5;在下图中用该电池电解含镍酸性废水可得到单质镍。下列说法正确的是
| A.电解过程中,b中NaCl溶液的物质的量浓度会增大 |
| B.锂钒氧化物二次电池可以用LiCl水溶液作为电解液 |
| C.该电池充电时,B电极的电极反应式为LixV2O5-xe-=V2O5+xLi+ |
| D.当锂钒氧化物二次电池中有7gLi参与放电时,一定能得到29.35g镍 |
您最近一年使用:0次
名校
3 . 某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其他均为Cu电极,则下列叙述正确的是


| A.电子流动方向:电极Ⅳ→Ⓐ→电极Ⅰ |
| B.电极Ⅰ发生氧化反应 |
| C.电极Ⅱ质量不变 |
| D.电极Ⅲ的电极反应Cu2++2e-=Cu |
您最近一年使用:0次
2019-02-22更新
|
339次组卷
|
4卷引用:安徽省阜阳市第三中学2018-2019学年高二下学期开学考试化学试题
名校
4 . 镍氢电池是近几年开发出来的可充电电池,它可以取代会产生的镉污染的镉镍电池。氢镍电池的总反应式是:1/2H2+NiO(OH)=Ni(OH)2据此反应式判断,下列叙述中正确的是( )
| A.电池放电时,电池负极周围的溶液pH不断增大 |
| B.电池放电时,镍元素被氧化 |
| C.电池充电时,镍元素被还原 |
| D.电池放电时,H2是负极 |
您最近一年使用:0次
名校
5 .  燃料电池具有理论电压高、能量密度大等优点。以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是
燃料电池具有理论电压高、能量密度大等优点。以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是

 燃料电池具有理论电压高、能量密度大等优点。以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是
燃料电池具有理论电压高、能量密度大等优点。以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是 
A.每消耗2.24 (标准状况)时,A电极的质量减轻12.8g (标准状况)时,A电极的质量减轻12.8g |
B.离子交换膜应为阳离子交换膜, 由左极室向右极室迁移 由左极室向右极室迁移 |
C.该燃料电池的负极反应式为 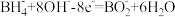 |
| D.粗铜中的Ag、Au沉在阳极区,电解质溶液的浓度基本保持不变 |
您最近一年使用:0次
名校
6 . 下图中甲池是以甲醇为原料,KOH为电解质的高效燃料电池,电化学过程的如图,下列说法中不正确的是
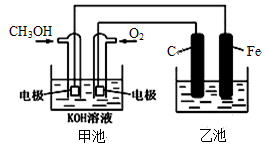

| A.甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O |
| B.若乙池中为足量AgNO3溶液,则阳极的电极反应为: 4OH--4e-= 2H2O+O2↑ |
| C.甲池中随着反应的不断进行,溶液的pH减小 |
| D.若乙池中为一定量CuSO4溶液,通电一段时间后,向溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为0.2NA |
您最近一年使用:0次
2019-01-27更新
|
373次组卷
|
3卷引用:【全国百强校】安徽省黄山市屯溪第一中学2018-2019学年高二下学期入学摸底考试化学试题
名校
7 . 微生物燃料电池在净化废水的同时能获得能源或得到有价值的化学产品,图1为其工作原理,图2为废水中Cr2O72-离子浓度与去除率的关系。下列说法不正确的是
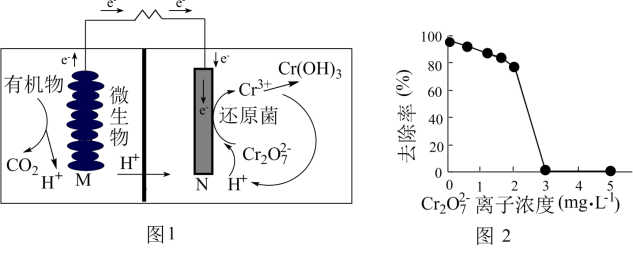

| A.M为电源负极,有机物被氧化 |
| B.处理1 mol Cr2O72-时有6 mol H+从交换膜左侧向右侧迁移 |
| C.电池工作时,N极附近溶液pH增大 |
| D.Cr2O72-离子浓度较大时,可能会造成还原菌失活 |
您最近一年使用:0次
2018-12-26更新
|
382次组卷
|
8卷引用:安徽省舒城中学2020-2021学年高二上学期开学考试化学试题
名校
8 . 下列图示中关于铜电极的连接错误的是
A.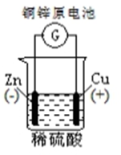 | B.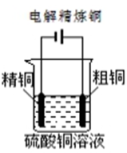 |
C.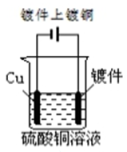 | D. |
您最近一年使用:0次
2018-12-11更新
|
640次组卷
|
36卷引用:安徽省六安市舒城中学2020-2021学年高二下学期开学考试化学试题
安徽省六安市舒城中学2020-2021学年高二下学期开学考试化学试题2015-2016学年安徽省蚌埠二中高二下学期期中化学试卷2017届安徽省安庆市怀宁中学等六校高三第一次联考化学试卷江西省宜春市宜丰县宜丰中学2019-2020学年高二下学期开学考试化学试题(已下线)2010年福建省福州八中高二第二学期期末考试化学试题(已下线)2013-2014吉林省长春市十一中高一下学期期末考试化学试卷2014-2015福建省福州市第八中学高二下学期期中化学试卷2016届贵州省贵阳市普通高中高三8月摸底考试化学试卷2015-2016学年广东省惠阳高级中学高二上学期期中理综化学试卷2015-2016学年福建省连江县尚德中学高二上期中考试化学试卷山东省垦利第一中学2017-2018学年高二上学期第一次月考化学试题山东省济南第一中学2017-2018学年高二上学期期中考试化学试题河南省郑州市第106中学2018-2019学年高二上学期第一次月考化学试题福建省福州市第三中学2017-2018学年高二下学期期末考试化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高二上学期第一次月考化学试题广东省惠州市惠东县惠东高级中学2018-2019学年高二上学期10月月考化学试题福建省东山县第二中学2018-2019学年高二上学期第一次(10月)月考化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高二(理)上学期期中考试化学试题陕西省黄陵中学2018-2019学年高二(重点班)上学期期中考试化学试题(已下线)2018年12月7日 《每日一题》人教选修4-电镀铜与精炼铜的比较福建省惠安惠南中学2018-2019学年高二上学期期中考试化学试题陕西省黄陵中学2018-2019学年高二上学期期末考试化学试题北京市朝阳区陈经纶中学 2019-2020学年高二下学期期中自主检测化学试题河北省邢台市第二中学2019-2020学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第3节 电能转化为化学能——电解人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第二节 电解池辽宁省辽河油田第二高级中学2020-2021学年高二上学期期中考试化学试题(已下线)练习9 电解池-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)江西省南昌市第十中学2020-2021学年高二上学期期末考试化学试题(已下线)模块八 电化学基础(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷宁夏银川一中2021-2022学年高二上学期期末考试化学试题(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第六章 化学反应与能量 第37练 电解池 金属的腐蚀与防护
名校
9 . 蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2,下列有关爱迪生电池的推断不正确的是
Fe(OH)2+Ni(OH)2,下列有关爱迪生电池的推断不正确的是
 Fe(OH)2+Ni(OH)2,下列有关爱迪生电池的推断不正确的是
Fe(OH)2+Ni(OH)2,下列有关爱迪生电池的推断不正确的是| A.放电时,Fe是负极,NiO2是正极 |
| B.蓄电池的电极可以浸入某种酸性电解质溶液中 |
| C.充电时,阴极上的电极反应为:Fe(OH)2 + 2e-= Fe + 2OH- |
| D.放电时,电解质溶液中的阴离子向负极方向移动 |
您最近一年使用:0次
2018-10-19更新
|
427次组卷
|
6卷引用:安徽省安庆市第七中学2023-2024学年高二下学期开学考试化学试题
名校
10 . 某粗铜产品中含有Zn、Ag、Au等杂质,如图所示,用CH3OH-碱性燃料电池电解硫酸铜溶液。闭合电键K进行电解。下列说法中不正确的是( )


| A.左池负极反应式为CH3OH -6e-+8OH-=CO32-+ 6H2O |
| B.通电一段时间后,Ag、Au杂质金属沉积在电解槽底部 |
| C.若粗铜电极质量减少6.4g,则纯铜电极增重大于6.4g |
| D.电解过程中右池纯铜和粗铜分别为阴极和阳极 |
您最近一年使用:0次
2018-01-16更新
|
610次组卷
|
8卷引用:安徽省怀宁中学2019-2020学年高二上学期开学考试化学试题



