名校
1 . 在直流电源作用下,双极膜中间层中的 解离为
解离为 和
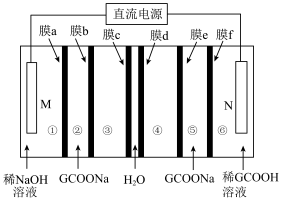
和 。某技术人员利用双极膜(膜c、膜d)电解技术从含葡萄糖酸钠(用GCOONa表示)的溶液中提取NaOH和葡萄糖酸(GCOOH),工作原理如图所示。下列说法错误的是
。某技术人员利用双极膜(膜c、膜d)电解技术从含葡萄糖酸钠(用GCOONa表示)的溶液中提取NaOH和葡萄糖酸(GCOOH),工作原理如图所示。下列说法错误的是
 解离为
解离为 和
和 。某技术人员利用双极膜(膜c、膜d)电解技术从含葡萄糖酸钠(用GCOONa表示)的溶液中提取NaOH和葡萄糖酸(GCOOH),工作原理如图所示。下列说法错误的是
。某技术人员利用双极膜(膜c、膜d)电解技术从含葡萄糖酸钠(用GCOONa表示)的溶液中提取NaOH和葡萄糖酸(GCOOH),工作原理如图所示。下列说法错误的是
| A.M为阴极 |
| B.③室和④室所得产物相同 |
| C.膜a为阳离子交换膜,膜b为阴离子交换膜 |
D.N极电极反应式为 |
您最近半年使用:0次
2023-10-26更新
|
836次组卷
|
9卷引用:安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题河南省豫北名校2024届高三毕业班上学期一轮复习联考(二)化学试题山西省部分学校2023-2024学年高三上学期10月月考(一轮复习联考(二))化学试题河北省石家庄部分高中2023-2024学年高三上学期10月期中考试化学试题甘肃省部分校2024届高三上学期10月月考化学试题辽宁省部分学校2023-2024学年高三上学期一轮复习联考(二)化学试题重庆市百师联盟2024届高三一轮复习联考(二)江西省宜春市宜丰中学创新部2023-2024学年高三上学期期中考试化学试题(已下线)寒假作业09 电解池 金属的腐蚀与防护-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
名校
2 . 某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,装置如图所示。其中乙装置中X为阳离子交换膜。下列有关说法错误的是
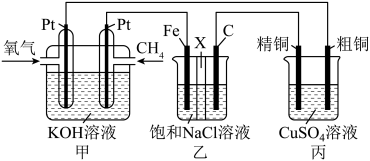

| A.通入O2的Pt极为正极,该电极反应式为O2-4e-+2H2O=4OH- |
| B.乙装置中铁电极为阴极,电极反应式为2H2O+2e-=H2↑+2OH- |
| C.反应一段时间后,乙装置中在铁电极区生成氢氧化钠溶液 |
| D.反应一段时间后,丙装置中硫酸铜溶液浓度可能减小 |
您最近半年使用:0次
2023-06-05更新
|
211次组卷
|
4卷引用:安徽省淮南市第一中学2023-2024学年高二下学期开学考试化学试题
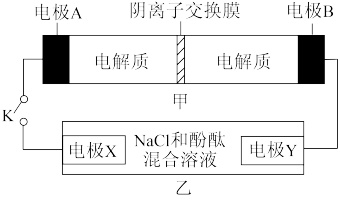
3 . 装置甲为铁镍可充电电池: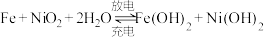 ;装置乙为电解池(两电极均为惰性电极),当闭合开关K时,Y附近溶液先变红。下列说法正确的是
;装置乙为电解池(两电极均为惰性电极),当闭合开关K时,Y附近溶液先变红。下列说法正确的是
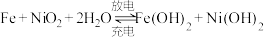 ;装置乙为电解池(两电极均为惰性电极),当闭合开关K时,Y附近溶液先变红。下列说法正确的是
;装置乙为电解池(两电极均为惰性电极),当闭合开关K时,Y附近溶液先变红。下列说法正确的是
| A.闭合K时,Y极发生氧化反应 |
B.闭合K时,A电极反应式为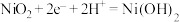 |
| C.理论上,电解一段时间后X极与Y极产生的气体物质的量相等 |
D.装置甲充电时, 通过阴离子交换膜,移向B电极 通过阴离子交换膜,移向B电极 |
您最近半年使用:0次
解题方法
4 . 通过控制开关可使同一装置发生不同的化学反应。
(1)研究模拟钢铁的电化学防护装置如图所示:
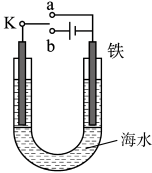
①若X为Zn,开关K置于a处,一段时间后,取适量Fe电极周围的溶液于试管中,滴加_______ (填化学式)溶液未出现蓝色沉淀,证明铁未被腐蚀。
②若X为石墨,开关K置于b处,一段时间后,Fe电极周围溶液的pH_______ (填“变大”或"变小”);该电化学防护法称为_______ 。
(2)模拟氯碱工业的电化学装置如图(II)所示:
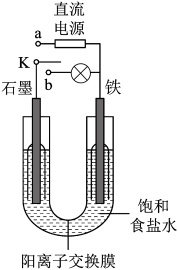
①开关K置于a处时,两极试管内均有气泡产生,则Fe电极为_______ (填“阴”或“阳”)极。
②一段时间后,使开关K与a断开,再将K置于b处时,观察到两极试管内的气体逐渐减少,此时的装置称为_______ (填“电解池”或“原电池”),Fe电极上的电极反应式为_______ 。
(3)利用太阳能光伏电池电解水制高纯氢的工作原理如图所示,通过控制开关连接a或b,可交替得到 和
和 。
。
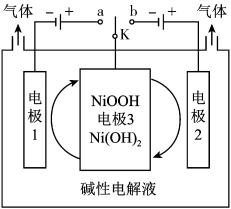
①制 时,K置于
时,K置于_______ 处(填“a”或“b”)。
②制 时,电极3的电极反应式为
时,电极3的电极反应式为_______ 。
(1)研究模拟钢铁的电化学防护装置如图所示:

①若X为Zn,开关K置于a处,一段时间后,取适量Fe电极周围的溶液于试管中,滴加
②若X为石墨,开关K置于b处,一段时间后,Fe电极周围溶液的pH
(2)模拟氯碱工业的电化学装置如图(II)所示:

①开关K置于a处时,两极试管内均有气泡产生,则Fe电极为
②一段时间后,使开关K与a断开,再将K置于b处时,观察到两极试管内的气体逐渐减少,此时的装置称为
(3)利用太阳能光伏电池电解水制高纯氢的工作原理如图所示,通过控制开关连接a或b,可交替得到
 和
和 。
。
①制
 时,K置于
时,K置于②制
 时,电极3的电极反应式为
时,电极3的电极反应式为
您最近半年使用:0次
2023-02-13更新
|
149次组卷
|
2卷引用:安徽省十校联盟2022-2023学年高二下学期开学考试化学试题
5 . 近日,中国科学院青岛生物能源与过程研究所开发了二次镁电池正极材料 ,该正极材料通过储存
,该正极材料通过储存 ,实现了镁电池的高体积能量密度。充电装置如图所示(
,实现了镁电池的高体积能量密度。充电装置如图所示( 、
、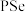 为电极后应的中间物质)
为电极后应的中间物质)

下列叙述正确的是
 ,该正极材料通过储存
,该正极材料通过储存 ,实现了镁电池的高体积能量密度。充电装置如图所示(
,实现了镁电池的高体积能量密度。充电装置如图所示( 、
、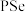 为电极后应的中间物质)
为电极后应的中间物质)
下列叙述正确的是
A.放电时, 向正极区移动,嵌入正极材料 向正极区移动,嵌入正极材料 |
| B.充电时,Mg电极与外接电源的正极相连 |
C.充电时,电子流向为 电极→b→a→Mg电极 电极→b→a→Mg电极 |
D.放电时,正极区的电极反应式为: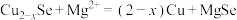 |
您最近半年使用:0次
名校
解题方法
6 . 利用所学电化学反应原理,解决以下问题:
(1)如图是电解未知浓度的硝酸银溶液的示意图,请根据要求答题。

①Fe电极叫做____ 极,C电极的反应式为____ 。
②当某电极的固体质量增重21.6g时,整个装置共产生气体(标准状况下)体积2.24L,推断该气体的组成____ 。
(2)图中甲池的总反应式为____ 。
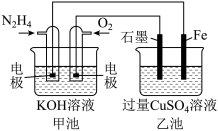
①甲池中负极上的电极反应式为____ 。
②乙池中石墨电极上发生的反应为____ 。
③要使乙池恢复到电解前的状态,应向溶液中加入适量的____ 。
A.CuOB.Cu(OH)2C.CuCO3D.CuSO4
(3)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:____ 。
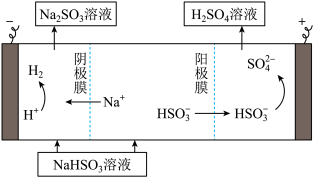
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图。请写出开始时阳极反应的电极反应式:____ 。
(1)如图是电解未知浓度的硝酸银溶液的示意图,请根据要求答题。

①Fe电极叫做
②当某电极的固体质量增重21.6g时,整个装置共产生气体(标准状况下)体积2.24L,推断该气体的组成
(2)图中甲池的总反应式为

①甲池中负极上的电极反应式为
②乙池中石墨电极上发生的反应为
③要使乙池恢复到电解前的状态,应向溶液中加入适量的
A.CuOB.Cu(OH)2C.CuCO3D.CuSO4
(3)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图。请写出开始时阳极反应的电极反应式:

您最近半年使用:0次
2022-10-30更新
|
260次组卷
|
3卷引用:安徽省滁州市定远县育才学校2021-2022学年高二(实验班)下学期开学摸底考试化学试题
7 . 氟离子热电池是一种新型电池,具有极高的能量密度,其放电时变化原理如下图所示。下列说法错误的是
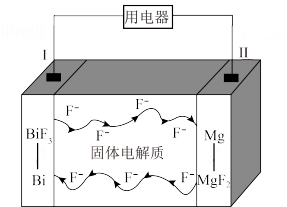

| A.放电时电极上电势:电极Ⅰ>电极Ⅱ |
B.电能转化为化学能时总反应: |
C.放电时电极Ⅰ上电极反应式: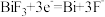 |
D.充电时当电极Ⅱ减少 时,电路中有 时,电路中有 电子转移 电子转移 |
您最近半年使用:0次
2022-08-30更新
|
215次组卷
|
2卷引用:安徽省A10联盟2022-2023学年高三上学期开学考试化学试题
解题方法
8 . 电解质浓度不同形成的浓差电池,称为离子浓差电池。以浓差电池为电源,以石墨为电极将NH3转化为高纯H2的装置如图所示。下列说法错误的是
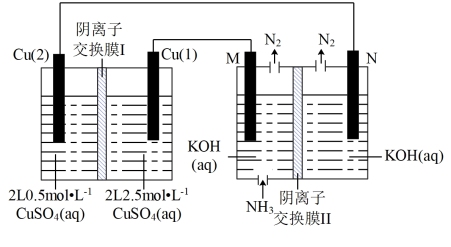

| A.Cu(1)为阳极,N为负极 |
| B.M极电极反应为:2NH3-6e-+6OH-=N2+6H2O |
C.工作时,左池SO 从右侧经膜I移向左侧,右池OH-从右侧经膜Ⅱ移向左侧 从右侧经膜I移向左侧,右池OH-从右侧经膜Ⅱ移向左侧 |
| D.当浓差电池停止放电时,理论上可得到22.4L标准状况下的H2(溶液体积变化忽略不计) |
您最近半年使用:0次
名校
解题方法
9 . 用如下装置进行实验:
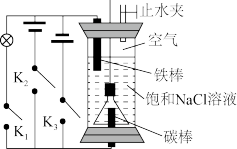
(1)关闭上端止水夹,接通K1,一段时间后用压强传感器测得装置上部压强减小,铁棒表面出现锈迹。则铁棒主要发生,_______ 腐蚀(填“析氢”或“吸氧”);此时碳棒上的电极反应式为:_______ 。
(2)Na2FeO4是一种新型净水剂,可以通过以下反应制备:Fe(OH)2+2Cl2+6NaOH=Na2FeO4+4NaCl+4H2O,为制得Na2FeO4,用一支倒扣的漏斗罩住碳极,如图,首先打开止水夹,断开K1、K2,接通K3。几分钟后,漏斗中产生的气体是_______ ;此时发生的总反应化学方程式为:_______ 。
(3)断开K1、K3,接通K2。阳极的电极反应式为_______ 。打开漏斗上口软塞,发生(2)中反应生成Na2FeO4。
(4)Na2FeO4有强氧化性可用于杀菌消毒,还可净水,其净水的原理是_______ 。

(1)关闭上端止水夹,接通K1,一段时间后用压强传感器测得装置上部压强减小,铁棒表面出现锈迹。则铁棒主要发生,
(2)Na2FeO4是一种新型净水剂,可以通过以下反应制备:Fe(OH)2+2Cl2+6NaOH=Na2FeO4+4NaCl+4H2O,为制得Na2FeO4,用一支倒扣的漏斗罩住碳极,如图,首先打开止水夹,断开K1、K2,接通K3。几分钟后,漏斗中产生的气体是
(3)断开K1、K3,接通K2。阳极的电极反应式为
(4)Na2FeO4有强氧化性可用于杀菌消毒,还可净水,其净水的原理是
您最近半年使用:0次
解题方法
10 . 以NaCl饱和溶液为电解质溶液,利用下图所示的电解池可将CO2转化为CO,下列说法错误的是
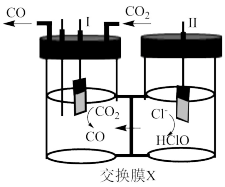

| A.电极II上电极反应式为Cl--2e-+ H2O =HClO+H+ |
| B.电极I应接电源负极 |
| C.X膜应是阴离子交换膜 |
| D.当电路中右2mol电子转移时,就会有44g物质被还原 |
您最近半年使用:0次



