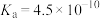名校
解题方法
1 . 氯碱工业以电解精制饱和食盐水的方法制取系列化工产品的重要化学工业。但氯碱工业是高耗能产业,某氯碱厂工程师设计如下新工艺,相关物料的传输与转化关系如图所示,将电解池与原电池相结合的新工艺可以节能30%以上,这样大大降低能耗,节约资源。请回答下列问题:
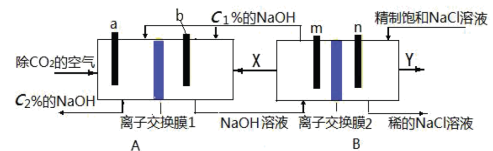
(1)装置中,A为___________ ,B为___________ (填“电解池”、“原电池”)。已知离子交换膜1为阳离子交换膜,离子交换膜2是___________ (填“质子交换膜”、“阳离子交换膜”、“阴离子交换膜”)。
(2)图中a、b、m、n均为惰性电极,b为___________ 极,m为___________ 极(填“阴、阳、正、负”)。X、Y分别是___________ 、___________ (填物质名称),
___________  (填“>”、“<”或“=”)。分别写出a、m电极的电极反应式:
(填“>”、“<”或“=”)。分别写出a、m电极的电极反应式:___________ ;___________ 。
(3)这样的设计,主要节能之处在于(写出两处):___________ ;___________ 。
(4)在标准状况下,若生成Y的体积为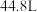 ,则至少通入的空气体积为
,则至少通入的空气体积为___________ L(只考虑空气的主要成分 和
和 )。
)。

(1)装置中,A为
(2)图中a、b、m、n均为惰性电极,b为

 (填“>”、“<”或“=”)。分别写出a、m电极的电极反应式:
(填“>”、“<”或“=”)。分别写出a、m电极的电极反应式:(3)这样的设计,主要节能之处在于(写出两处):
(4)在标准状况下,若生成Y的体积为
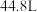 ,则至少通入的空气体积为
,则至少通入的空气体积为 和
和 )。
)。
您最近一年使用:0次
名校
2 . 回答下列问题:
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
(1)25℃时, 盐酸的pH约为
盐酸的pH约为______ ,该溶液中水电离出的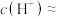
______  。
。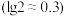
(2)少量的 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为______ 。
(3) 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为______ ;25℃时, 的水解平衡常数
的水解平衡常数
______ 其电离平衡常数 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显______ 性。
Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为______ (填“原电池”“电解池”或“电镀池”),通入 电极的电极反应式正确的为
电极的电极反应式正确的为______ 。
A. B.
B.
C.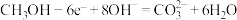 D.
D.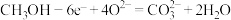
(5)当甲池中消耗 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加______ g。
(6)丙池中发生的总反应化学方程式为______ ;为了防止丙池中两极产物相互反应,实际生产中在两极之间设有______ 离子交换膜(填“阴”或“阳”或“质子”)。
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
弱电解质 |
|
| HClO |
电离常数 |
|
|
|
(1)25℃时,
 盐酸的pH约为
盐酸的pH约为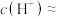
 。
。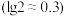
(2)少量的
 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为(3)
 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为 的水解平衡常数
的水解平衡常数
 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为
 电极的电极反应式正确的为
电极的电极反应式正确的为A.
 B.
B.
C.
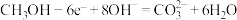 D.
D.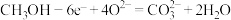
(5)当甲池中消耗
 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加(6)丙池中发生的总反应化学方程式为
您最近一年使用:0次
名校
3 . 某化学兴趣小组同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池中负极的电极反应为_______ 。
(2)乙池中A(石墨)电极为________ (填“正极”、“负极”、“阴极”或“阳极”)。乙池中B极质量增加10.8g时,甲池中理论上消耗O2的体积为________ L(标准状况),丙池中________ (填“C”或“D”)极析出_______ g铜。
(3)一种以CO2和甲醇为原料,利用SnO2(mSnO2/CC)和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。

注: (甲酸)的化学式为HCOOH,书写方程式时采用HCOOH即可。
(甲酸)的化学式为HCOOH,书写方程式时采用HCOOH即可。
①图中电极a为________ 极,电解过程中阳极电极反应式为________ 。
②当有8molH+通过质子交换膜时,理论上装置中生成HCOO-和HCOOH共计________ mol。

请回答下列问题:
(1)甲池中负极的电极反应为
(2)乙池中A(石墨)电极为
(3)一种以CO2和甲醇为原料,利用SnO2(mSnO2/CC)和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。

注:
 (甲酸)的化学式为HCOOH,书写方程式时采用HCOOH即可。
(甲酸)的化学式为HCOOH,书写方程式时采用HCOOH即可。①图中电极a为
②当有8molH+通过质子交换膜时,理论上装置中生成HCOO-和HCOOH共计
您最近一年使用:0次
名校
4 . 以二甲醚( )-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为
)-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为 。
。

回答下列问题:
(1)装置A为___________ (填“原电池”或“电解池”),X极的电极名称为___________ (填“正极”、“负极”、“阴极”、“阳极”,下同),b极名称为___________ 。
(2)b极附近可能的现象是___________ 。
(3)a极上发生___________ (填“氧化”或“还原”)反应,其电极反应式为___________ 。
(4)若装置A中消耗标准状况下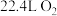 ,则理论上装置C中可得纯铜的质量为
,则理论上装置C中可得纯铜的质量为___________ g。
 )-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为
)-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为 。
。
回答下列问题:
(1)装置A为
(2)b极附近可能的现象是
(3)a极上发生
(4)若装置A中消耗标准状况下
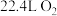 ,则理论上装置C中可得纯铜的质量为
,则理论上装置C中可得纯铜的质量为
您最近一年使用:0次
名校
解题方法
5 . 铁和铁的化合物在生活、生产、国防建设中有广泛的应用。请回答下列有关问题:
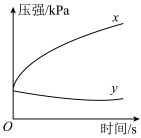
(1)在不同酸性介质中,金属铁的腐蚀原理并不相同,如图是在密闭容器中,生铁在 和
和 的盐酸中容器内压强随时间的变化过程。其负极反应式为
的盐酸中容器内压强随时间的变化过程。其负极反应式为_______ ;代表 的曲线是
的曲线是_______ (填“x”或“y”)。
(2)高铁酸钾( )是一种新型非氯高效消毒剂。用下图所示的装置可以制取
)是一种新型非氯高效消毒剂。用下图所示的装置可以制取 。
。
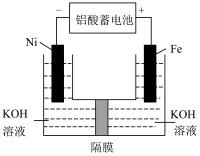
①该化合物中铁元素的化合价为_______ ; 净水时,起絮凝作用的原理是
净水时,起絮凝作用的原理是_______ (结合化学用语和文字说明)。
②铅酸蓄电池的正极反应式为_______ ;该装置中,若外电路转移了 ,理论上消耗
,理论上消耗 物质的量为
物质的量为_______ 。
③隔膜最好是交换膜_______ (填“阳离子”或“阴离子”):电解时阳极附近的
_______ (填“增大”“减小”或“不变”),阳极的电极反应式为_______ 。

(1)在不同酸性介质中,金属铁的腐蚀原理并不相同,如图是在密闭容器中,生铁在
 和
和 的盐酸中容器内压强随时间的变化过程。其负极反应式为
的盐酸中容器内压强随时间的变化过程。其负极反应式为 的曲线是
的曲线是(2)高铁酸钾(
 )是一种新型非氯高效消毒剂。用下图所示的装置可以制取
)是一种新型非氯高效消毒剂。用下图所示的装置可以制取 。
。
①该化合物中铁元素的化合价为
 净水时,起絮凝作用的原理是
净水时,起絮凝作用的原理是②铅酸蓄电池的正极反应式为
 ,理论上消耗
,理论上消耗 物质的量为
物质的量为③隔膜最好是交换膜

您最近一年使用:0次
6 . 各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
(1)传统汽车中使用的电池主要是铅蓄电池,其构造如图。

①放电时,铅蓄电池总反应式为:______ ;
②充电时,电源正极与______ (填“Pb”或“ ”)连接,溶液的pH会
”)连接,溶液的pH会______ (填“增大”、“减小”或“不变”)。
(2)重庆在新能源汽车的制造和开发上走在时代的前列。新能源汽车使用的主要是锂离子电池,某锂离子电池工作原理如图所示。
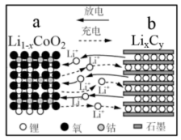
总反应式为:
①放电时,电极b是______ 极,a电极反应式为______ ;
②充电时,当导线中通过2mol 时,阴极的固体质量增加
时,阴极的固体质量增加______ g。
③与传统的铅蓄电池相比,锂电池具有的优点有:______ (一点即可)。
(3)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:
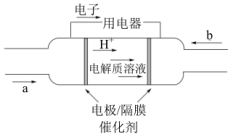
①a处通入的气体是______ ;
②电池每消耗5.6L(标准状况下)氢气,电路中通过的电子数目为______ 。
(1)传统汽车中使用的电池主要是铅蓄电池,其构造如图。

①放电时,铅蓄电池总反应式为:
②充电时,电源正极与
 ”)连接,溶液的pH会
”)连接,溶液的pH会(2)重庆在新能源汽车的制造和开发上走在时代的前列。新能源汽车使用的主要是锂离子电池,某锂离子电池工作原理如图所示。

总反应式为:

①放电时,电极b是
②充电时,当导线中通过2mol
 时,阴极的固体质量增加
时,阴极的固体质量增加③与传统的铅蓄电池相比,锂电池具有的优点有:
(3)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:

①a处通入的气体是
②电池每消耗5.6L(标准状况下)氢气,电路中通过的电子数目为
您最近一年使用:0次
名校
7 . I.根据电化学相关知识,回答问题:
(1)如甲图为电解精炼银的示意图,_____ (填“a”或“b”)极为含有杂质的粗银。
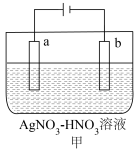
(2)利用如乙图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。阳极电极反应式为______ ,电解过程中Li+向______ (填“A”或“B”)电极迁移。

II.如图X是直流电源,c、d为石墨棒,e、f是质量相同的铜棒。接通电路后,发现d附近显红色。

(3)①b为电源的______ 极(填“正”“负”“阴”或“阳”,下同)。
②Z池中e为______ 极。
③连接Y、Z池线路,电子流动的方向是d_____ e(用“→”或“←”填空)。
(4)写出c极上反应的电极反应式:______ 。
(1)如甲图为电解精炼银的示意图,

(2)利用如乙图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。阳极电极反应式为

II.如图X是直流电源,c、d为石墨棒,e、f是质量相同的铜棒。接通电路后,发现d附近显红色。

(3)①b为电源的
②Z池中e为
③连接Y、Z池线路,电子流动的方向是d
(4)写出c极上反应的电极反应式:
您最近一年使用:0次
名校
解题方法
8 . 能源、材料、环境和健康等领域与化学息息相关。
(1)如图为利用甲烷燃料电池电解AlCl3溶液的装置,电极材料均为石墨。秋林同学用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。

①x为图2电池的_______ (填“正”“负”“阴”“阳”)极;图1电池工作时,OH-向_______ (填“a”或“b”)极移动。
②a极电极反应式为_______ 。
③每消耗3molCH4,理论上生成_______ g白色沉淀。
(2)A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。
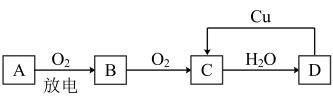
写出D→C的化学方程式:_______ ;其中D表现出_______ 性。
(3)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2工艺的主要反应机理如图所示。
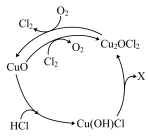
①X为_______ 。
②总反应化学方程式式为_______ 。
(1)如图为利用甲烷燃料电池电解AlCl3溶液的装置,电极材料均为石墨。秋林同学用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。

①x为图2电池的
②a极电极反应式为
③每消耗3molCH4,理论上生成
(2)A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。

写出D→C的化学方程式:
(3)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2工艺的主要反应机理如图所示。

①X为
②总反应化学方程式式为
您最近一年使用:0次
名校
解题方法
9 . 利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中
+6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中 减少0.1mol。
减少0.1mol。

(1)工作时,甲池内的NO3-向石墨_______ 极移动(填“I”或“II”);在相同条件下,消耗的O2和NO2的体积比为_______ 。
(2)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨I是电池的_______ 极;石墨I附近发生的电极反应式为_______ 。
(3)丙池中阳极的电极反应式为_______ ,阳极产生气体的体积为_______ L(标况下),若阴极生成气体为6.72L(标况下),则可以加入_______ 复原(填字母序号)。
A.0.3molCu(OH)2 B.0.15molCu2(OH)2CO3 C.0.3molCuO D.0.3molCuCO3
 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中
+6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中 减少0.1mol。
减少0.1mol。
(1)工作时,甲池内的NO3-向石墨
(2)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨I是电池的
(3)丙池中阳极的电极反应式为
A.0.3molCu(OH)2 B.0.15molCu2(OH)2CO3 C.0.3molCuO D.0.3molCuCO3
您最近一年使用:0次
解题方法
10 . 电化学的发展是化学对人类的一项重大贡献。探究原电池和电解池原理,对生产生活具有重要的意义。
(1)利用甲醇燃料电池(甲池)作电源同时电解乙池和丙池。
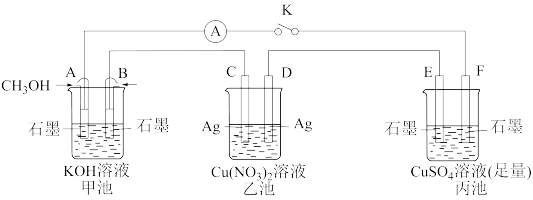
①放电时, 向
向_______ (填“A极”或“B极”)移动; 溶液过量时,甲池中负极的电极反应式为
溶液过量时,甲池中负极的电极反应式为_______ 。
②当乙池中C极质量减轻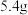 时,甲池中B极理论上消耗
时,甲池中B极理论上消耗 的体积为
的体积为_______  (标准状况)。
(标准状况)。
③一段时间后,断开电键K,欲使丙池恢复到反应前的浓度,可加入的试剂是_______ (填化学式)。
(2)氯碱工业是高耗能产业,将电解池与燃料电池相组合的新工艺可以节能30%以上,相关物料的传输与转化关系如图所示,其中的电极未标出所用的离子膜都只允许阳离子通过。

①图中Y是_______ (填化学式);X与 稀溶液反应的离子方程式为
稀溶液反应的离子方程式为_______ 。
②比较图示中氢氧化钠的质量分数a%与b%的大小:_______ 。
③若用装置B作为装置A的辅助电源,则每消耗标准状况下 氧气时,装置B可向装置A提供的电量约为
氧气时,装置B可向装置A提供的电量约为_______ (一个 的电量为
的电量为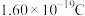 ,计算结果精确到0.01)。
,计算结果精确到0.01)。
(1)利用甲醇燃料电池(甲池)作电源同时电解乙池和丙池。

①放电时,
 向
向 溶液过量时,甲池中负极的电极反应式为
溶液过量时,甲池中负极的电极反应式为②当乙池中C极质量减轻
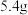 时,甲池中B极理论上消耗
时,甲池中B极理论上消耗 的体积为
的体积为 (标准状况)。
(标准状况)。③一段时间后,断开电键K,欲使丙池恢复到反应前的浓度,可加入的试剂是
(2)氯碱工业是高耗能产业,将电解池与燃料电池相组合的新工艺可以节能30%以上,相关物料的传输与转化关系如图所示,其中的电极未标出所用的离子膜都只允许阳离子通过。

①图中Y是
 稀溶液反应的离子方程式为
稀溶液反应的离子方程式为②比较图示中氢氧化钠的质量分数a%与b%的大小:
③若用装置B作为装置A的辅助电源,则每消耗标准状况下
 氧气时,装置B可向装置A提供的电量约为
氧气时,装置B可向装置A提供的电量约为 的电量为
的电量为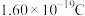 ,计算结果精确到0.01)。
,计算结果精确到0.01)。
您最近一年使用:0次