名校
1 . 化学是一门以实验为基础的科学探究与创新能力是化学学科核心素养之一,实验探究也是化学学习的重要方法。回答下列问题:
(1)探究浓度、温度对化学平衡的影响。CuCl2溶液中存在下列化学平衡: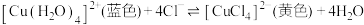
 ,用编号为
,用编号为 的3支试管各取
的3支试管各取 的
的 溶液(蓝绿色)进行下列实验:
溶液(蓝绿色)进行下列实验:
①试管a中进行的操作可以是____ (填标号)。
A.加入蒸馏水稀释 B.滴加浓盐酸 C.滴加AgNO3溶液
②对试管b中溶液加热时,平衡____ (填“正向”“逆向”或“不”)移动。
③对试管c不进行任何操作,其作用是____ 。
(2)利用如图所示装置探究氢氧燃料电池的工作原理。

①电解制备H2、O2:打开K2,闭合K1,连接电池负极的石墨Ⅱ为____ (填“阳极”或“阴极”),阳极的电极反应式为_______ ;_____ (填“石墨I”或“石墨Ⅱ”)附近的溶液变红。
②探究燃料电池的工作原理:在上述实验①结束后,立即打开K1,闭合K2,可以观察到电流表指针偏转,则外电路中电子的流动方向是________ (填“石墨Ⅱ流向石墨Ⅰ”或“石墨Ⅰ流向石墨Ⅱ”);负极的电极反应式是________ 。
(1)探究浓度、温度对化学平衡的影响。CuCl2溶液中存在下列化学平衡:
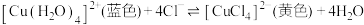
 ,用编号为
,用编号为 的3支试管各取
的3支试管各取 的
的 溶液(蓝绿色)进行下列实验:
溶液(蓝绿色)进行下列实验:| 实验操作(改变的条件) | 实验现象 |
| 试管a:___________ | 溶液变为黄绿色 |
| 试管b:在热水浴中加热 |
A.加入蒸馏水稀释 B.滴加浓盐酸 C.滴加AgNO3溶液
②对试管b中溶液加热时,平衡
③对试管c不进行任何操作,其作用是
(2)利用如图所示装置探究氢氧燃料电池的工作原理。

①电解制备H2、O2:打开K2,闭合K1,连接电池负极的石墨Ⅱ为
②探究燃料电池的工作原理:在上述实验①结束后,立即打开K1,闭合K2,可以观察到电流表指针偏转,则外电路中电子的流动方向是
您最近一年使用:0次
名校
解题方法
2 . 电解原理在化学工业中有广泛应用。
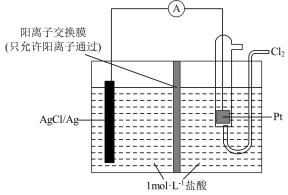
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如下图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
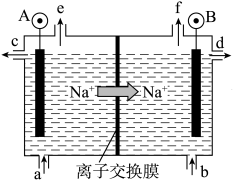
①电解饱和食盐水总反应的离子方程式为________ 。
②电解饱和食盐水时,在b口加入的物质为_______ (写化学式)。
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图。该电池放电时总反应为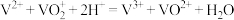 。
。
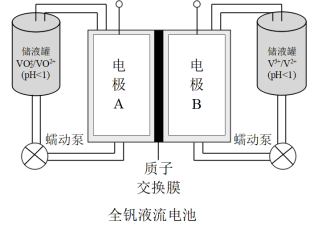
①当完成储能时,阴极区溶液的颜色是_______ 。
②放电时,每转移 就有
就有______ 通过质子交换膜进入电极_____ 区(填“A”或“B”)
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如下图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

①电解饱和食盐水总反应的离子方程式为
②电解饱和食盐水时,在b口加入的物质为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图。该电池放电时总反应为
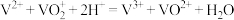 。
。
| 离子种类 | 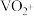 |  |  |  |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |
②放电时,每转移
 就有
就有
您最近一年使用:0次
2024-02-14更新
|
107次组卷
|
2卷引用:海南省海南中学2023- 2024学年高三上学期第4次月考化学试题
名校
3 . 以CH3OH燃料电池为电源电解法制取ClO2,二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
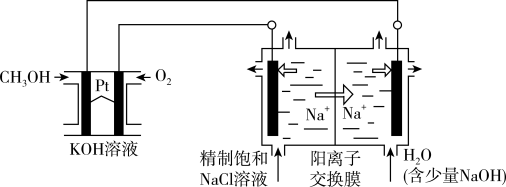
(1)CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH___________ (填“增大减小”或“不变”),负极反应式为。________________ 。
(2)图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为_______________ 。
(3)电解一段时间,从阴极处收集到的气体比阳极处收集到的气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为___________ mol。

(1)CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH
(2)图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为
(3)电解一段时间,从阴极处收集到的气体比阳极处收集到的气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
您最近一年使用:0次
2023-12-02更新
|
98次组卷
|
2卷引用:海南省农垦中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
4 . 回答下列问题
(1)在下图所示的原电池装置中,负极的电极反应为___________ ,电池总反应为___________ ,当电路中通过 电子时,交换膜左侧溶液中离子减少的物质的量为
电子时,交换膜左侧溶液中离子减少的物质的量为___________ 。
(2)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
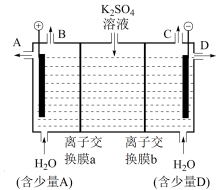
①该电解槽的阴极反应式为___________ 。
②离子交换膜b为___________ (填“阳离子交换膜”或“阴离子交换膜”)。
③出口A获得___________ 产品。
(1)在下图所示的原电池装置中,负极的电极反应为
 电子时,交换膜左侧溶液中离子减少的物质的量为
电子时,交换膜左侧溶液中离子减少的物质的量为
(2)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为
②离子交换膜b为
③出口A获得
您最近一年使用:0次
22-23高二下·河北石家庄·阶段练习
名校
5 . 铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为
 ;请回答下列问题(不考虑氢、氧的氧化还原):
;请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时,正极的电极反应式是_______ ;当外电路通过1mol电子时,理论上负极板的质量增加_______ g。
(2)在完全放电耗尽 和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
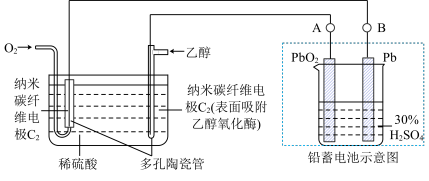
①生物燃料电池(BFC)中 极的电极反应式为:
极的电极反应式为:_______ 。
②在A电极上生成_______ 。
(3) 不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出
不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出 ,并用纯碱吸收。
,并用纯碱吸收。
① 与氢溴酸反应的离子方程式为
与氢溴酸反应的离子方程式为_______ 。
②碱吸收溴的主要反应是 ,吸收1mol
,吸收1mol  时,转移的电子数为
时,转移的电子数为_______ mol。
③请写出 溶液与足量的澄清石灰水反应的离子方程式
溶液与足量的澄清石灰水反应的离子方程式_______ 。

 ;请回答下列问题(不考虑氢、氧的氧化还原):
;请回答下列问题(不考虑氢、氧的氧化还原):(1)放电时,正极的电极反应式是
(2)在完全放电耗尽
 和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
和Pb后,若按图连接,利用燃料电池(BFC)电解一段时间后。
①生物燃料电池(BFC)中
 极的电极反应式为:
极的电极反应式为:②在A电极上生成
(3)
 不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出
不仅可用于制作铅蓄电池,同时可与氢溴酸共热制备单质溴,并采用“空气吹出法”从上述反应的混合液吹出 ,并用纯碱吸收。
,并用纯碱吸收。①
 与氢溴酸反应的离子方程式为
与氢溴酸反应的离子方程式为②碱吸收溴的主要反应是
 ,吸收1mol
,吸收1mol  时,转移的电子数为
时,转移的电子数为③请写出
 溶液与足量的澄清石灰水反应的离子方程式
溶液与足量的澄清石灰水反应的离子方程式
您最近一年使用:0次
22-23高二上·重庆北碚·开学考试
名校
解题方法
6 . 能源、材料、环境和健康等领域与化学息息相关。
(1)如图为利用甲烷燃料电池电解AlCl3溶液的装置,电极材料均为石墨。秋林同学用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。

①x为图2电池的_______ (填“正”“负”“阴”“阳”)极;图1电池工作时,OH-向_______ (填“a”或“b”)极移动。
②a极电极反应式为_______ 。
③每消耗3molCH4,理论上生成_______ g白色沉淀。
(2)A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。
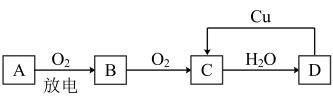
写出D→C的化学方程式:_______ ;其中D表现出_______ 性。
(3)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2工艺的主要反应机理如图所示。
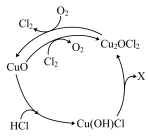
①X为_______ 。
②总反应化学方程式式为_______ 。
(1)如图为利用甲烷燃料电池电解AlCl3溶液的装置,电极材料均为石墨。秋林同学用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。

①x为图2电池的
②a极电极反应式为
③每消耗3molCH4,理论上生成
(2)A、B、C、D四种物质之间有如图所示的转化关系。已知:A是空气中的主要成分之一,B、C、D均为化合物,且C为一种红棕色气体。

写出D→C的化学方程式:
(3)一种在恒温、恒定气流流速下,催化氧化HCl生产Cl2工艺的主要反应机理如图所示。

①X为
②总反应化学方程式式为
您最近一年使用:0次
名校
7 . 请仔细观察下列五种装置的构造示意图,回答下列问题。
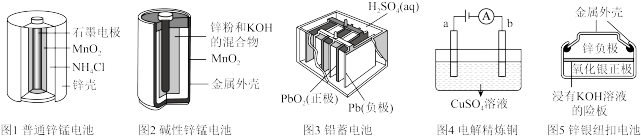
(1)碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应为_______ 。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素角度分析其原因:_______ 。
(3)图3中铅蓄电池放电过程中,H2SO4溶液浓度_______ (填“变大”“变小”或“不变”),充电时阴极的电极反应为_______ 。
(4)图4中电解精炼铜时,a极是_______ (填“纯铜”或“粗铜”)。锌银钮扣电池在工作过程中_______ (填物质名称)被还原。

(1)碱性锌锰电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应为
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素角度分析其原因:
(3)图3中铅蓄电池放电过程中,H2SO4溶液浓度
(4)图4中电解精炼铜时,a极是
您最近一年使用:0次
2022-04-14更新
|
77次组卷
|
2卷引用:海南省农垦中学2023-2024学年高二上学期期末考试化学试题(B卷)
名校
解题方法
8 .
(1)用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到更多
溶液进行电解,可循环再生NaOH,同时得到更多 ,其原理如图所示
,其原理如图所示 电极材料为石墨
电极材料为石墨 。
。

①图中a极要连接电源的___________________  填“正”或“负”
填“正”或“负” 极,上图中硫酸的质量分数比较a%
极,上图中硫酸的质量分数比较a%__________ b%(填“>”“<”或“=”)。
② 在b极上的电极反应式为
在b极上的电极反应式为______________________________________________ 。
③电解过程中阴极区pH_____________ (填“增大”或“降低”或“不变”) 。
(2)有人设想以 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,电池装置如图所示。该电池在正极生成
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,电池装置如图所示。该电池在正极生成 的电极反应式为
的电极反应式为___________________________ ,A物质是____________________ 。

(1)用NaOH溶液吸收烟气中的
 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到更多
溶液进行电解,可循环再生NaOH,同时得到更多 ,其原理如图所示
,其原理如图所示 电极材料为石墨
电极材料为石墨 。
。
①图中a极要连接电源的
 填“正”或“负”
填“正”或“负” 极,上图中硫酸的质量分数比较a%
极,上图中硫酸的质量分数比较a%②
 在b极上的电极反应式为
在b极上的电极反应式为③电解过程中阴极区pH
(2)有人设想以
 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,电池装置如图所示。该电池在正极生成
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,电池装置如图所示。该电池在正极生成 的电极反应式为
的电极反应式为
您最近一年使用:0次
名校
解题方法
9 . 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
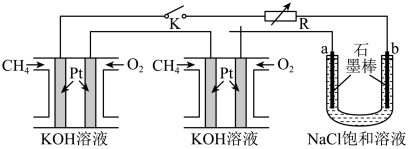
回答下列问题:
(1)闭合K开关后,a、b电极上均有气体产生。其中b电极为___________ 极(填“阴”或“阳”),得到的气体是___________ ,电解一段时间后,附近溶液的pH ___________ (填“升高”、“降低”、“不变”),要使溶液复原,应向溶液中加入 ___________ ,电解氯化钠溶液的总反应方程式为___________ 。如把氯化钠饱和溶液换成熔融氯化钠,则该池的总反应方程式为___________ 。
(2)甲烷燃料电池负极的电极反应为___________ 。
(3)若每个电池甲烷通入量为4.48 L(标准状况),且反应完全,则理论上通过电解池的电子数目为___________ (标准状况)。

回答下列问题:
(1)闭合K开关后,a、b电极上均有气体产生。其中b电极为
(2)甲烷燃料电池负极的电极反应为
(3)若每个电池甲烷通入量为4.48 L(标准状况),且反应完全,则理论上通过电解池的电子数目为
您最近一年使用:0次
名校
解题方法
10 . 如图表示一个电解池,装有电解液a、X、Y是两块电极板,通过导线与直流电源相连,请回答以下问题:
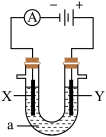
(1)若X、Y是惰性石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,在X极附近观察到的现象是______________________________ ;Y电极上的电极反应式是 ___________________ ,电解NaCl溶液的离子方程式是________________________________ 。
(2)若要在铜制品上镀Ag,则电解质溶液a可为___________________ ,Y电极反应式为_________________________________ 。
(3)若上图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式_________________ ,电池工作过程中,正极附近的pH将______ (填“增大、减小或不变”)。

(1)若X、Y是惰性石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,在X极附近观察到的现象是
(2)若要在铜制品上镀Ag,则电解质溶液a可为
(3)若上图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式
您最近一年使用:0次



