名校
解题方法
1 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为离子交换膜。请按要求回答相关问题:
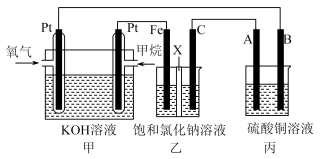
(1)甲烷燃料电池负极反应式是___________ 。
(2)Fe电极的电极反应式为___________ 。
(3)X选择___________ 离子交换膜(填“阴”,“阳”)。
(4)丙模拟粗铜的精炼,那么粗铜放在___________ (填“A”,“B”)极,反应结束后硫酸铜溶液的浓度___________ (填“变大”,“变小”,“不变”)。
(5)若在标准状况下,有1.12 L氧气参加反应,则乙装置中铁极上生成的气体体积为___________ L。
(6)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
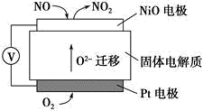
①Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式:___________ 。

(1)甲烷燃料电池负极反应式是
(2)Fe电极的电极反应式为
(3)X选择
(4)丙模拟粗铜的精炼,那么粗铜放在
(5)若在标准状况下,有1.12 L氧气参加反应,则乙装置中铁极上生成的气体体积为
(6)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是
②写出NiO电极的电极反应式:
您最近一年使用:0次
名校
解题方法
2 . 电化学装置可实现化学能与电能的直接转化,是助力实现“30、60”双碳目标的一种重要路径。回答下列问题:
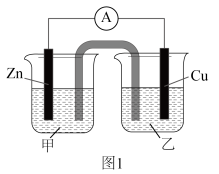
(1)①盐桥是电池发展史上一项重要技术突破,极大地提高了化学能→电能的转化效率,同时使电流更加稳定。若图1装置能形成铜锌原电池,则甲烧杯盛装:_______ [填ZnSO4(aq)或CuSO4(aq)];盐桥中装的是含有琼脂的KCl饱和溶液。
②将图1右池中的Cu电极材料换成_______ ,电解质溶液换成_______ ,可实现Zn+2Fe3+=Zn2++2Fe2+中能量直接转化为电能。
(2)电解池在工业及生产中广泛应用,其原理如图2和图3所示。
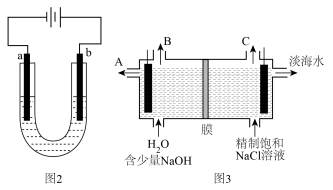
①电镀时,b电极应为_______ (选填“待镀金属”或“镀层金属”);精炼铜时,Cu2+的浓度变化是_______ (填“增大”,“不变”,“减小”)。
②图3氯碱工业中,选择的离子交换膜是_______ ,离子交换膜右侧电极产物是_______ ,左侧电极上发生的电极反应式为_______ 。
(3)二甲醚(CH3OCH3)燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质Ni的原理如图所示(反应中Ⅱ室NaCl溶液浓度变大)。
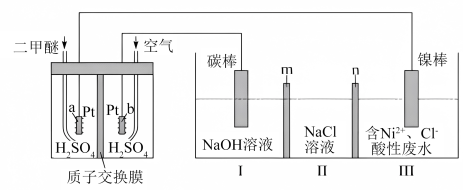
①a电极反应式为_______ ,发生_______ 反应。
②写出镍棒电极上发生的电极反应式为_______ 。m,n是否可以选择同种交换膜_______ (填“是”或“否”)请说明原因:_______ 。
(1)①盐桥是电池发展史上一项重要技术突破,极大地提高了化学能→电能的转化效率,同时使电流更加稳定。若图1装置能形成铜锌原电池,则甲烧杯盛装:

②将图1右池中的Cu电极材料换成
(2)电解池在工业及生产中广泛应用,其原理如图2和图3所示。

①电镀时,b电极应为
②图3氯碱工业中,选择的离子交换膜是
(3)二甲醚(CH3OCH3)燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质Ni的原理如图所示(反应中Ⅱ室NaCl溶液浓度变大)。

①a电极反应式为
②写出镍棒电极上发生的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。
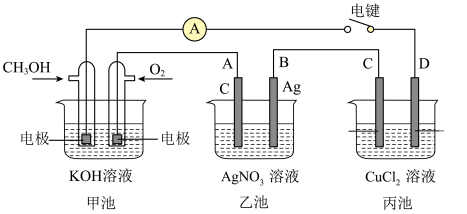
请回答下列问题:
(1)甲池中,通入CH3OH电极的电极反应式为___________ 。
(2)设乙池的体积为200mL,反应一段时间后,乙池中A、B两极都产生22.4mL(已换算成标准状况)的气体时,乙池中pH约为___________ ,反应开始前乙池中的AgNO3的浓度为___________ ,甲池中理论上消耗O2的体积为___________ mL(标准状况)。
(3)若要电解精炼铜,丙池中,粗铜应为___________ (填C或D)电极。
(4)若丙池中C、D两电极都为惰性电极,将其溶液换成NaCl溶液,总电池反应方程式为___________ ,为了获得氢气和氯气,该装置中需使用___________ (填阳离子、阴离子或质子)交换膜。

请回答下列问题:
(1)甲池中,通入CH3OH电极的电极反应式为
(2)设乙池的体积为200mL,反应一段时间后,乙池中A、B两极都产生22.4mL(已换算成标准状况)的气体时,乙池中pH约为
(3)若要电解精炼铜,丙池中,粗铜应为
(4)若丙池中C、D两电极都为惰性电极,将其溶液换成NaCl溶液,总电池反应方程式为
您最近一年使用:0次
2024-01-13更新
|
111次组卷
|
2卷引用:湖南省长沙市麓山国际实验学校2023-2024学年高二上学期第三次月考化学试题
名校
解题方法
4 . 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。
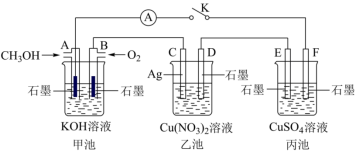
请回答下列问题:
(1)A电极的电极反应式为:___________ 。
(2)丙池中F电极为___________ (填“正极”、“负极”、“阴极”或“阳极”),写出电解时总反应的离子方程式___________ 。
(3)当乙池中C极质量变化10.8 g时,甲池中B电极理论上消耗O2的体积为___________ mL(标准状况)。
(4)若丙池通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和PH(不考虑CO2的溶解),则电解过程中转移的电子___________ mol, 若电解后溶液的体积为400ml,则所得溶液中氢离子的浓度___________ 。

请回答下列问题:
(1)A电极的电极反应式为:
(2)丙池中F电极为
(3)当乙池中C极质量变化10.8 g时,甲池中B电极理论上消耗O2的体积为
(4)若丙池通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和PH(不考虑CO2的溶解),则电解过程中转移的电子
您最近一年使用:0次
名校
5 . 用 燃料电池连接成如下装置。
燃料电池连接成如下装置。
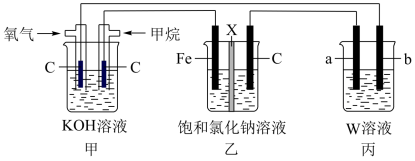
(1)乙池中X为阳离子交换膜,石墨电极(C)作______ 极,写出乙池总反应的离子方程式______ 。
(2)若将乙装置中两电极用导线直接相连,则铁发生______ 腐蚀,写出碳棒的电极反应式:______ 。若将乙装置中两电极连接电源的正负两极,铁连接电源的______ 极(填“正”或“负”)可防止铁腐蚀,该种防护方法叫______ 。
(3)若乙池中X为钠离子交换膜(只允许钠离子通过),则当甲池中消耗标准状况下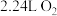 时,乙装置中阳极室溶液质量减少
时,乙装置中阳极室溶液质量减少______ 克。
(4)若丙中要实现铁上镀银,b电极材料为______ 。
 燃料电池连接成如下装置。
燃料电池连接成如下装置。
(1)乙池中X为阳离子交换膜,石墨电极(C)作
(2)若将乙装置中两电极用导线直接相连,则铁发生
(3)若乙池中X为钠离子交换膜(只允许钠离子通过),则当甲池中消耗标准状况下
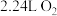 时,乙装置中阳极室溶液质量减少
时,乙装置中阳极室溶液质量减少(4)若丙中要实现铁上镀银,b电极材料为
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题
(1)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为___________ 。
②通电开始后,阳极附近溶液pH会___________ (填“变大”、“变小”或“不变”)
③出口A获得___________ 产品,离子交换膜b是___________ 离子交换膜(填“阳”或“阴”)。
(2)电化学在化学工业中有着广泛应用。根据图示电化学装置,回答下列问题:

①甲池通入乙烷(C2H6)一极的电极反应式为___________ 。
②乙池中,若X、Y都是石墨,A是饱和食盐水,乙池中的离子反应方程式为___________ 。
③若使用铜棒、铁质钥匙等材料用该装置实现在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:铁质钥匙应放在___________ 极(填X或Y),电镀一段时间后,CuSO4溶液浓度___________ (“减小”“不变”“增大”)。
④乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为2L,电解一段时间后,甲池消耗1.12LO2(标准状况下),则乙池溶液的pH为___________ (忽略溶液体积的变化)。
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阳极的电极反应式为___________ ,当制备0.5molNa2FeO4时,阴极产生气体质量为___________ 。
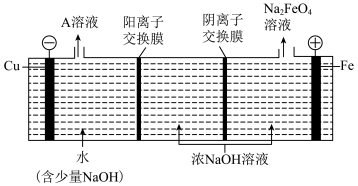
(1)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为
②通电开始后,阳极附近溶液pH会
③出口A获得
(2)电化学在化学工业中有着广泛应用。根据图示电化学装置,回答下列问题:

①甲池通入乙烷(C2H6)一极的电极反应式为
②乙池中,若X、Y都是石墨,A是饱和食盐水,乙池中的离子反应方程式为
③若使用铜棒、铁质钥匙等材料用该装置实现在铁质钥匙表面镀一层金属铜,CuSO4溶液作电解液,则乙池中:铁质钥匙应放在
④乙池中,若X、Y都是石墨,A是足量AgNO3溶液,体积为2L,电解一段时间后,甲池消耗1.12LO2(标准状况下),则乙池溶液的pH为
(3)工业上通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图所示,则阳极的电极反应式为

您最近一年使用:0次
名校
解题方法
7 . 电化学在生产、生活和科学研究中应用十分广泛,认识和研究化学能与电能相互转化的原理和规律具有重要意义。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。

①图2为液态肼 燃料电池,c电极发生的电极反应式为
燃料电池,c电极发生的电极反应式为_______ 。
②图1、图2相连时a电极为_______ (填“正”“负”“阴”或“阳”)极。生成 的离子方程式为
的离子方程式为_______ 。
③通过离子交换膜的离子是_______ (填离子符号):当电路中转移 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积_______ ,电解池左室质量变化_______ g。
(2)碳排放是影响气候变化的重要因素之一、最近,科学家开发出一种新系统,“溶解”水中的二氧化碳,以触发电化学反应,生成电能和氢气,其工作原理如图所示。请用化学方程式表示该电池的原理:_______ 。

(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。

①图2为液态肼
 燃料电池,c电极发生的电极反应式为
燃料电池,c电极发生的电极反应式为②图1、图2相连时a电极为
 的离子方程式为
的离子方程式为③通过离子交换膜的离子是
 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积(2)碳排放是影响气候变化的重要因素之一、最近,科学家开发出一种新系统,“溶解”水中的二氧化碳,以触发电化学反应,生成电能和氢气,其工作原理如图所示。请用化学方程式表示该电池的原理:

您最近一年使用:0次
2023高三·全国·专题练习
8 . 高铁电池作为新型可充电电池,具有放电曲线平坦,高能高容量,原料丰富,绿色无污染等优点。如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。
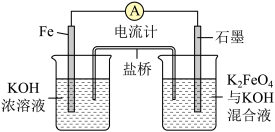
请回答下列问题:
(1)该电池放电时的总反应为___________ 。
(2)该电池充电时阳极反应的电极反应方程式为___________ 。
(3)放电时,此盐桥中阴离子的运动方向是___________ (填“从左向右”或“从右向左”)。

请回答下列问题:
(1)该电池放电时的总反应为
(2)该电池充电时阳极反应的电极反应方程式为
(3)放电时,此盐桥中阴离子的运动方向是
您最近一年使用:0次
名校
解题方法
9 . 完成下列问题。
(1)电解精制饱和食盐水制取氯气、氢气、烧碱和氯的含氧酸盐等一系列化工产品。如图是离子交换膜法电解食盐水的示意图。电解精制饱和食盐水的离子方程式为___________ 。

(2)氨电解法制氢气
利用电解原理,将氨转化为高纯氮气,其装置如图所示。

电解过程中,阳极的电极方程式为___________ 。
(3)图甲是一种将废水中的氯乙烯(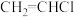 )转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。
)转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。

①M为_______ (填写“正极、负极、阴极、阳极”),镀铜时,______ (填写X或Y)与铁电极相连,工作过程中,N极电极反应式___________ ,当N极有3.2g O2完全反应时,通过质子交换膜的H+的数目为___________ 。
②若M极消耗0.1mol氯乙烯,则铁电极增重___________ g,硫酸铜溶液的浓度将___________ (填写“增大、减小、不变”)
(1)电解精制饱和食盐水制取氯气、氢气、烧碱和氯的含氧酸盐等一系列化工产品。如图是离子交换膜法电解食盐水的示意图。电解精制饱和食盐水的离子方程式为

(2)氨电解法制氢气
利用电解原理,将氨转化为高纯氮气,其装置如图所示。

电解过程中,阳极的电极方程式为
(3)图甲是一种将废水中的氯乙烯(
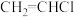 )转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。
)转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。
①M为
②若M极消耗0.1mol氯乙烯,则铁电极增重
您最近一年使用:0次
名校
解题方法
10 . 电池和电解池在日常生活中有着广泛的应用。根据所学知识完成下列题目。
Ⅰ.电化学装置如图所示
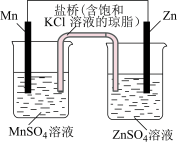
(1)已知金属活泼性: 。若如图装置中负极金属的消耗速率为
。若如图装置中负极金属的消耗速率为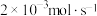 ,则盐桥中
,则盐桥中 流向
流向___________ (填“ ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为___________  。
。
Ⅱ.电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
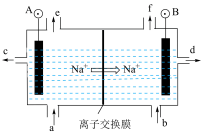
(2)①电解饱和食盐水的总反应的离子方程式是___________ 。
②在b口加入的物质为___________ (写化学式)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,氨水式燃料电池工作原理如图所示:
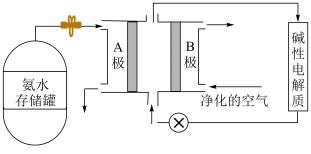
①氨气燃料电池的反应原理是氨气与氧气反应生成一种常见的无毒气体和水,该电池负极上的电极反应式是___________ 。
②“净化的空气”是指在进入电池装置前除去___________ (填化学式)的气体。
Ⅲ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
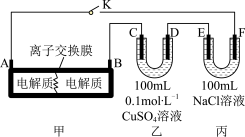
(4)装置甲中A电极为电池的___________ 极,B电极的电极反应式为___________ 。
(5)装置乙中D电极产生的气体是___________ (写化学式),体积为___________  (标准状况)。
(标准状况)。
(6)若将装置丙中的 溶液改换成
溶液改换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是___________ 。

Ⅰ.电化学装置如图所示

(1)已知金属活泼性:
 。若如图装置中负极金属的消耗速率为
。若如图装置中负极金属的消耗速率为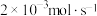 ,则盐桥中
,则盐桥中 流向
流向 ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为 。
。Ⅱ.电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

(2)①电解饱和食盐水的总反应的离子方程式是
②在b口加入的物质为
(3)氨气是一种富氢燃料,可以直接用于燃料电池,氨水式燃料电池工作原理如图所示:

①氨气燃料电池的反应原理是氨气与氧气反应生成一种常见的无毒气体和水,该电池负极上的电极反应式是
②“净化的空气”是指在进入电池装置前除去
Ⅲ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为
 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
(4)装置甲中A电极为电池的
(5)装置乙中D电极产生的气体是
 (标准状况)。
(标准状况)。(6)若将装置丙中的
 溶液改换成
溶液改换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
您最近一年使用:0次



