1 . 下列有关电化学装置的叙述中,正确的是
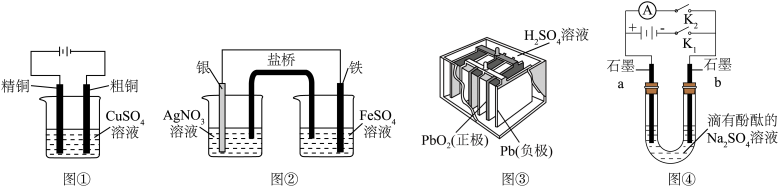
| A.图①装置可实现粗铜的电解梢炼 |
B.图②装置右侧溶液中的 会经过盐桥迁移到左侧 会经过盐桥迁移到左侧 溶液中 溶液中 |
C.图③装置充电时,若电中通过 电子,理论上阴极区溶液中生成 电子,理论上阴极区溶液中生成 的质量为 的质量为 |
D.图④装置闭合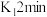 后,打开 后,打开 闭合 闭合 ,石墨a电极反应式为: ,石墨a电极反应式为: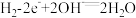 |
您最近一年使用:0次
2024-04-29更新
|
103次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
2 . 电化学技术的发展是近年来科技的热点。请结合电化学知识回答下列问题:
(1)如图甲所示的电化学装置。盐桥为浸泡了饱和氯化钾溶液的琼脂。反应一段时间,向两烧杯中分别滴加几滴酚酞,___________ (填“m”或“ 烧杯中溶液变红,盐桥中的K+向
烧杯中溶液变红,盐桥中的K+向___________ (填“m”或“n”)烧杯移动。 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 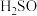 4和NaOH。
4和NaOH。___________ 。
②电解池中同时制备 和NaOH的总反应为
和NaOH的总反应为___________ 。
③d膜为___________ (填“阳”或“阴”)离子交换膜。
④当电解池中产生标准状况下22.4L H2时,理论上正极区CuSO4浓度变为___________ mol/L。
⑤从电池开始工作到停止放电,制备NaOH的质量为204g。若该电化学装置的工作效率= 。则该过程的工作效率为
。则该过程的工作效率为___________ 。
(1)如图甲所示的电化学装置。盐桥为浸泡了饱和氯化钾溶液的琼脂。反应一段时间,向两烧杯中分别滴加几滴酚酞,
 烧杯中溶液变红,盐桥中的K+向
烧杯中溶液变红,盐桥中的K+向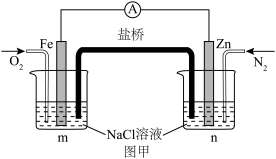
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 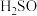 4和NaOH。
4和NaOH。
②电解池中同时制备
 和NaOH的总反应为
和NaOH的总反应为③d膜为
④当电解池中产生标准状况下22.4L H2时,理论上正极区CuSO4浓度变为
⑤从电池开始工作到停止放电,制备NaOH的质量为204g。若该电化学装置的工作效率=
 。则该过程的工作效率为
。则该过程的工作效率为
您最近一年使用:0次
解题方法
3 . 双极膜是一种复合膜,在直流电作用下,能把中间界面内的H2O解离为H+和OH-,并使离子定向通过。

以铅蓄电池为电源(放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O),利用双极膜电解获得NaOH与H3PO4的原理如图所示。下列说法正确的是

以铅蓄电池为电源(放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O),利用双极膜电解获得NaOH与H3PO4的原理如图所示。下列说法正确的是
| A.N膜为阳离子交换膜 |
| B.产品室2中溶液pH逐渐增大 |
C.产品室1中反应为 +2OH-= +2OH-= +2H2O +2H2O |
| D.双极膜共解离4molH2O时,理论上铅蓄电池中生成2molPbSO4 |
您最近一年使用:0次
解题方法
4 . 氧化铋( )作为镍/铋电池的负极材料,因其理论容量高、易制备而受到广泛关注。下图为该电池的示意图,下列说法正确的是
)作为镍/铋电池的负极材料,因其理论容量高、易制备而受到广泛关注。下图为该电池的示意图,下列说法正确的是
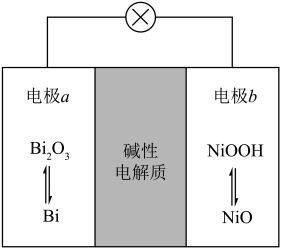
 )作为镍/铋电池的负极材料,因其理论容量高、易制备而受到广泛关注。下图为该电池的示意图,下列说法正确的是
)作为镍/铋电池的负极材料,因其理论容量高、易制备而受到广泛关注。下图为该电池的示意图,下列说法正确的是
A.放电时, 从电极a移向电极b 从电极a移向电极b |
| B.充电时,电子从电源负极→电极a→电极b→电源正极 |
C.放电时,总反应为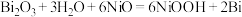 |
D.充电时,电路转移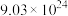 个电子,阳极质量增加255g 个电子,阳极质量增加255g |
您最近一年使用:0次
解题方法
5 . 松山湖材料实验室李洪飞首次研究了碘正极在水系铝离子电池中的转化反应化学( )。下列叙述错误的是
)。下列叙述错误的是
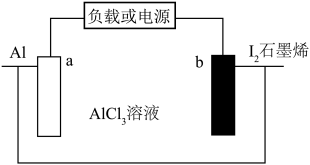
 )。下列叙述错误的是
)。下列叙述错误的是
A.放电时, 在正极上发生还原反应 在正极上发生还原反应 |
B.放电时, 极质量减少 极质量减少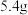 理论上转移约 理论上转移约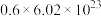 个电子 个电子 |
C.充电时, 极反应之一为 极反应之一为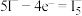 |
D.充电时, 参与反应生成 参与反应生成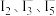 物质的量之比一定为 物质的量之比一定为 |
您最近一年使用:0次
解题方法
6 . 含镍废水对环境和人体健康均会造成巨大的影响。某化学小组在实验室设计了以下装置模拟工业含镍废水处理,图中电极均为惰性电极。错误 的是
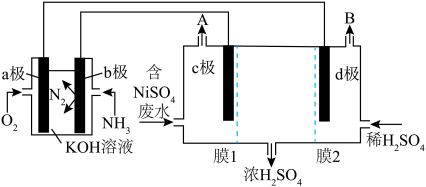
A.a极为正极, 极为阴极 极为阴极 |
B. 极的电极反应为2H2O-4e-=O2+4H+↑ 极的电极反应为2H2O-4e-=O2+4H+↑ |
| C.膜1为阴离子交换膜 |
D.b极消耗22.4LNH3,理论上 极上析出88.5gNi单质 极上析出88.5gNi单质 |
您最近一年使用:0次
2024-03-23更新
|
151次组卷
|
2卷引用:甘肃省白银市靖远县第二中学2023-2024学年高二上学期12月期末化学试题
解题方法
7 . 一种钠离子电池的工作原理如图所示。充电过程中,磷酸钒钠[Na3V2(PO4)3]在外电压的作用下脱嵌部分Na+形成Na3-xV2(PO4)3,脱出的Na+进入电解液中,再传输到硬碳材料形成化合物NaxC。下列说法正确的是
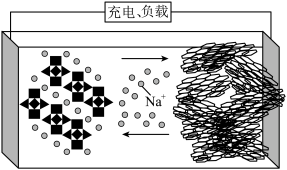

| A.充电时Na3V2(PO4)3为阴极 |
| B.充电时,电解液的质量增大 |
| C.放电时Na+由负极迁移到正极材料中 |
| D.放电时的正极反应为Na3V2(PO4)3-xe-=Na3-xV2(PO4)3+xNa+ |
您最近一年使用:0次
2024-03-16更新
|
38次组卷
|
2卷引用:陕西省安康市高新中学2023-2024学年高三12月月考理科综合试题
解题方法
8 . 回答下列问题。
(1)氧气在不同电解质溶液的电极方程式的书写
①酸性溶液:___________ ;
②碱性溶液:___________ ;
③允许O2-通过的高温固体:___________ ;
④熔融的碳酸盐:___________ 。
(2)甲醇燃料电池(铂为两电极,电解质为氢氧化钠溶液)
电池反应式:___________ ;
负极反应式:___________ 。
(3)用石墨电极电解硫酸铜溶液
阴极反应式:___________ ;
阳极反应式:___________ 。
(4)用石墨电极电解氢氧化钠溶液
阴极反应式:___________ ;
阳极反应式:___________ 。
(1)氧气在不同电解质溶液的电极方程式的书写
①酸性溶液:
②碱性溶液:
③允许O2-通过的高温固体:
④熔融的碳酸盐:
(2)甲醇燃料电池(铂为两电极,电解质为氢氧化钠溶液)
电池反应式:
负极反应式:
(3)用石墨电极电解硫酸铜溶液
阴极反应式:
阳极反应式:
(4)用石墨电极电解氢氧化钠溶液
阴极反应式:
阳极反应式:
您最近一年使用:0次
9 . 用电化学知识回答下列问题。
(1)“电絮凝-电气浮法”污水处理装置原理如图所示。在外电压作用下,可溶性阳极产生阳离子体对胶体污染物发生凝聚效应,同时另一极产生气体,在气体上浮过程中将絮体上浮,从而实现污染物的分离和水的净化。

①外接电源a端为___________ 极。
②石墨极电极反应为___________ 。
③铝电极___________ 用铁电极替换(填“能”或“不能”)。
(2)一种新型 可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、
可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、 和
和 ,不同区域由离子交换膜(a、b)隔开。
,不同区域由离子交换膜(a、b)隔开。
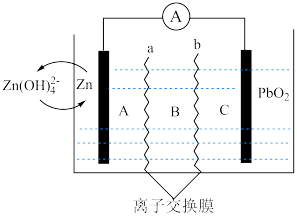
①Zn发生极___________ 反应(填“氧化”或“还原”)。
②a为极___________ 离子交换膜(填“阳”或“阴”,下同),b为极___________ 离子交换膜。
③ 的电极反应式为极
的电极反应式为极___________ 。
(3)一种二氧化碳的富集装置如图所示。

①电极材料采用多孔碳酸锂,“多孔”的优点是___________ 。
②电极a的电极反应式为___________ 。
(1)“电絮凝-电气浮法”污水处理装置原理如图所示。在外电压作用下,可溶性阳极产生阳离子体对胶体污染物发生凝聚效应,同时另一极产生气体,在气体上浮过程中将絮体上浮,从而实现污染物的分离和水的净化。

①外接电源a端为
②石墨极电极反应为
③铝电极
(2)一种新型
 可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、
可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、 和
和 ,不同区域由离子交换膜(a、b)隔开。
,不同区域由离子交换膜(a、b)隔开。
①Zn发生极
②a为极
③
 的电极反应式为极
的电极反应式为极(3)一种二氧化碳的富集装置如图所示。

①电极材料采用多孔碳酸锂,“多孔”的优点是
②电极a的电极反应式为
您最近一年使用:0次
10 . 为了实现“碳中和”,研发 的利用技术成为热点。
的利用技术成为热点。
反应I:
反应Ⅱ:
请回答:
(1)反应I能够自发进行的条件是__________ 。
(2)向 的恒容密闭容器中充入
的恒容密闭容器中充入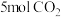 和
和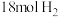 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
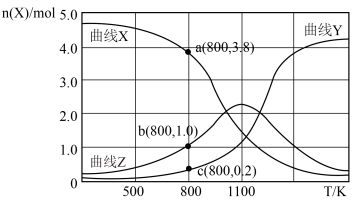
①写出曲线Y表示的含碳元素物质的化学式__________ 。
② 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
__________ [对于气相反应,用某组分 的平衡压强
的平衡压强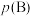 代替物质的量浓度
代替物质的量浓度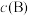 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如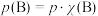 ,
, 为平衡总压强,
为平衡总压强,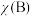 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。
(3)可用 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: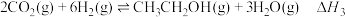 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示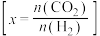 :
:

①上述反应的活化能 (正)
(正)__________  (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
② 、
、 、
、 由大到小的顺序是
由大到小的顺序是__________ 。
③从平衡角度分析,随温度升高,不同投料比时 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因__________ 。
(4)科学家提出由 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为__________ 。

(5)水系可逆 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:

①放电时复合膜中向 极移动的离子是
极移动的离子是__________ 。
②充电时多孔 纳米片电极的电极反应式为
纳米片电极的电极反应式为__________ 。
 的利用技术成为热点。
的利用技术成为热点。反应I:

反应Ⅱ:

请回答:
(1)反应I能够自发进行的条件是
(2)向
 的恒容密闭容器中充入
的恒容密闭容器中充入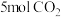 和
和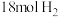 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
①写出曲线Y表示的含碳元素物质的化学式
②
 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
 的平衡压强
的平衡压强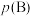 代替物质的量浓度
代替物质的量浓度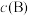 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如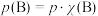 ,
, 为平衡总压强,
为平衡总压强,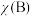 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。(3)可用
 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: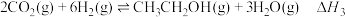 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示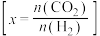 :
:
①上述反应的活化能
 (正)
(正) (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。②
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③从平衡角度分析,随温度升高,不同投料比时
 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因(4)科学家提出由
 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为
(5)水系可逆
 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
①放电时复合膜中向
 极移动的离子是
极移动的离子是②充电时多孔
 纳米片电极的电极反应式为
纳米片电极的电极反应式为
您最近一年使用:0次



