名校
解题方法
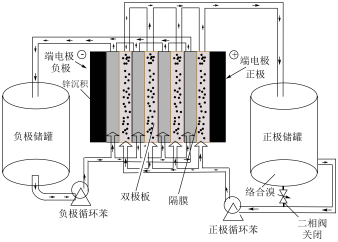
1 . 中科院大连化物所储能技术研究部将锌溴液流电池电堆面容量提高至140mAh/cm2,从而大幅度提高了电池能量密度。其原理如图所示(已知:络合溴为Br 、Br
、Br 等),下列说法正确的是
等),下列说法正确的是
 、Br
、Br 等),下列说法正确的是
等),下列说法正确的是
A. 端电极电势比 端电极电势比 端电极电势低 端电极电势低 |
B.放电时,负极电极反应为 |
| C.充电时,负极材料每增重65g,正极发生还原反应产生160g Br2 |
| D.放电时,电极表面之间的微孔隔膜阻止了络合溴向锌沉积物的扩散,减少了电池的自放电 |
您最近一年使用:0次
2 . 2020年9月中国明确提出“双碳”目标。因此,研发 资源化利用技术、降低空气中
资源化利用技术、降低空气中 含量成为科学家的研究热点。图1为我国科学家利用
含量成为科学家的研究热点。图1为我国科学家利用 和金属
和金属 成功发明的
成功发明的 电池的工作示意图。通入
电池的工作示意图。通入 一极的反应产物为
一极的反应产物为 和单质碳;图2为采用“两室”膜电解法将
和单质碳;图2为采用“两室”膜电解法将 转化为
转化为 的示意图。请回答下列问题:
的示意图。请回答下列问题: 电池中:
电池中:
(1) Li为______ (填“正”或“负”)极,正极的电极反应为____________ 。
(2)研究表明, 电还原后与
电还原后与 结合形成
结合形成 的反应历程如下,反应II的离子方程式为
的反应历程如下,反应II的离子方程式为____________
I.
II._________________
III.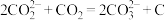
IV.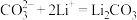
II、利用 电池作为图2装置的中源。
电池作为图2装置的中源。
(3) 片连接
片连接 电池的
电池的_______ (填“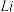 ”或“
”或“ ”)电极,电解过程中,
”)电极,电解过程中,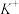 通过阳离子交换膜由
通过阳离子交换膜由_______ (填“左室移向右室”或“右室移向左室”),阴极发生的电极反应为_______ 。
(4)电解一段时间后, 电池中生成
电池中生成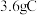 时,图2中阳极区产生气体的体积(标准状况)为
时,图2中阳极区产生气体的体积(标准状况)为_______ L。
 资源化利用技术、降低空气中
资源化利用技术、降低空气中 含量成为科学家的研究热点。图1为我国科学家利用
含量成为科学家的研究热点。图1为我国科学家利用 和金属
和金属 成功发明的
成功发明的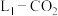 电池的工作示意图。通入
电池的工作示意图。通入 一极的反应产物为
一极的反应产物为 和单质碳;图2为采用“两室”膜电解法将
和单质碳;图2为采用“两室”膜电解法将 转化为
转化为 的示意图。请回答下列问题:
的示意图。请回答下列问题: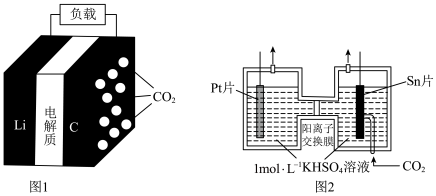
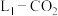 电池中:
电池中:(1) Li为
(2)研究表明,
 电还原后与
电还原后与 结合形成
结合形成 的反应历程如下,反应II的离子方程式为
的反应历程如下,反应II的离子方程式为I.

II._________________
III.
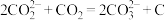
IV.
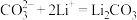
II、利用
 电池作为图2装置的中源。
电池作为图2装置的中源。(3)
 片连接
片连接 电池的
电池的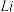 ”或“
”或“ ”)电极,电解过程中,
”)电极,电解过程中,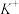 通过阳离子交换膜由
通过阳离子交换膜由(4)电解一段时间后,
 电池中生成
电池中生成 时,图2中阳极区产生气体的体积(标准状况)为
时,图2中阳极区产生气体的体积(标准状况)为
您最近一年使用:0次
名校
3 . 某小组为研究电化学原理,设计如图所示装置,回答下列问题:
(1)若a和b不连,c是铜片、d是锌片、m是稀硫酸,则锌片上的现象是_______ 。
(2)若a和b用导线相连,c、d均是Pt电极,m是稀硫酸,分别向两极通入甲烷和氧气,通入氧气一极的电极反应式是_______ 。
(3)若a和b分别连接直流电源的两电极:
①利用该装置实现铁件上镀铜,铁件应作_______ (填“阴极”或“阳极”)。
②c、d是石墨电极,m是NaCl溶液,向溶液中滴加几滴酚酞试液。实验开始后d极周围溶液首先出现红色,则b连接直流电源的_______ (填“正极”或“负极”),通电时总反应的化学方程式是_______ ,电解后溶液的pH_______ 。(填“增大”或“减小”或“不变”)
③c、d均是石墨电极,m是KNO3溶液,阴极的电极反应式是_______ 。

(1)若a和b不连,c是铜片、d是锌片、m是稀硫酸,则锌片上的现象是
(2)若a和b用导线相连,c、d均是Pt电极,m是稀硫酸,分别向两极通入甲烷和氧气,通入氧气一极的电极反应式是
(3)若a和b分别连接直流电源的两电极:
①利用该装置实现铁件上镀铜,铁件应作
②c、d是石墨电极,m是NaCl溶液,向溶液中滴加几滴酚酞试液。实验开始后d极周围溶液首先出现红色,则b连接直流电源的
③c、d均是石墨电极,m是KNO3溶液,阴极的电极反应式是
您最近一年使用:0次
名校
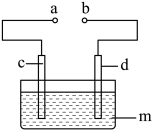
4 . CO2的资源化利用不仅可以减少CO2的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
I.科学家致力于CO2电催化合成甲醇的研究,其工作原理如图:
(1)a电极与电源的_______ 极相连,其中c为质子交换膜,写出b电极的电极反应式_______ 。
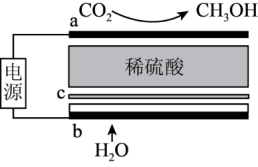
II. 燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
请回答下列问题:
(2)通入CH3OH电极的电极反应式为_______ 。
(3)当丙池某个电极增重25.6g时,乙池中收集到了标况下11.2L气体。则乙池中析出_______ gAg。
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后_______ (填C或D)极首先变红,写出电解时总离子反应式_______ 。
(5)CH4—CO2催化重整对温室气体的减排具有重要意义,其反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。已知相关物质的燃烧热(25℃、101kPa):
则CH4—CO2催化重整反应的ΔH=_______ kJ·mol-1。
I.科学家致力于CO2电催化合成甲醇的研究,其工作原理如图:

(1)a电极与电源的
II.
 燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
请回答下列问题:
(2)通入CH3OH电极的电极反应式为
(3)当丙池某个电极增重25.6g时,乙池中收集到了标况下11.2L气体。则乙池中析出
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后
(5)CH4—CO2催化重整对温室气体的减排具有重要意义,其反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。已知相关物质的燃烧热(25℃、101kPa):
| 物质 | CH4(g) | CO(g) | H2(g) |
| 燃烧热(ΔH/kJ·mol-1) | -890.3 | -283.0 | -285.8 |
您最近一年使用:0次
名校
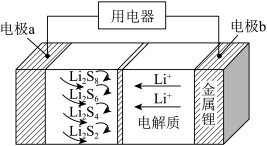
5 . 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的 材料,电池反应为
材料,电池反应为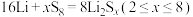 。下列说法正确的是
。下列说法正确的是
 材料,电池反应为
材料,电池反应为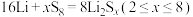 。下列说法正确的是
。下列说法正确的是
A.电池工作时,正极可发生反应: |
B.电池充电时间越长,电池中的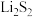 量越多 量越多 |
| C.电解质中加入硫酸能增强导电性 |
| D.电池工作时,外电路中流过0.2mol电子,负极材料减重0.7g |
您最近一年使用:0次
名校
解题方法
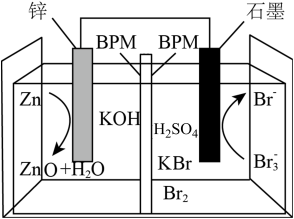
6 . 科学家研制出一种高性能水系酸碱双液锌-溴二次电池,其总反应为: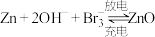
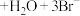 ,中间的双极性膜(BPM)能隔开酸碱双液且能允许
,中间的双极性膜(BPM)能隔开酸碱双液且能允许 通过,如图所示。下列说法正确的是
通过,如图所示。下列说法正确的是
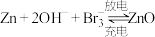
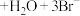 ,中间的双极性膜(BPM)能隔开酸碱双液且能允许
,中间的双极性膜(BPM)能隔开酸碱双液且能允许 通过,如图所示。下列说法正确的是
通过,如图所示。下列说法正确的是
A.放电时, 向锌极电极迁移 向锌极电极迁移 |
| B.放电时,负极区的pH减小 |
| C.充电时,锌与外接电源正极相连,将电能转化为化学能 |
D.充电时,石墨电极发生反应: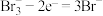 |
您最近一年使用:0次
名校
解题方法
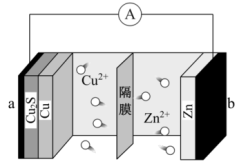
7 . 中国科学家构建水系级联二次电池,实现了在同一个反应腔体中耦合不同的氧化还原反应。如图所示电池以S、Zn为电极,以 溶液和
溶液和 溶液为离子导体,分两步放电,在a极首先生成
溶液为离子导体,分两步放电,在a极首先生成 ,后生成Cu。下列说法正确的是
,后生成Cu。下列说法正确的是
 溶液和
溶液和 溶液为离子导体,分两步放电,在a极首先生成
溶液为离子导体,分两步放电,在a极首先生成 ,后生成Cu。下列说法正确的是
,后生成Cu。下列说法正确的是
A.放电过程中,每生成1mol 的同时消耗1molZn 的同时消耗1molZn |
B.充电时 通过隔膜向b极移动 通过隔膜向b极移动 |
C.充电时a作阳极,Cu和 失电子生成单质硫和 失电子生成单质硫和 |
| D.用此电池为铅酸蓄电池充电,电极a应连接铅电极 |
您最近一年使用:0次
2022-12-14更新
|
274次组卷
|
4卷引用:辽宁省沈阳市第二中学2022-2023学年高三上学期12月阶段测试化学试题
辽宁省沈阳市第二中学2022-2023学年高三上学期12月阶段测试化学试题(已下线)河北省部分学校2022-2023学年高三上学期期末考试变式汇编(10-13)(已下线)广东省广州市2022届高三一模考试(选择题11-16)吉林省白山市抚松县第一中学2022-2023学年高三上学期期末考试化学试题
名校
解题方法
8 . 某同学设计用NO—空气质子交换膜燃料电池探究将雾霾中的SO2、NO转化为(NH)2SO4的原理。

下列说法正确的是

下列说法正确的是
| A.甲、乙装置中NO均被氧化、物质A为HNO3 |
| B.若甲装置中消耗22.4LO2(标况)则乙装置中SO2和NO转化的物质的量共有2.8mol |
C.燃料电池放电过程中正极电极反应式为NO-3e-+2H2O= +4H+ +4H+ |
| D.该装置中,电子的转移方向为Pt(1)→石墨(II)→电解质溶液→石墨(1)→Pt(II) |
您最近一年使用:0次
2022-11-23更新
|
468次组卷
|
3卷引用:辽宁省沈阳市第二中学2022-2023学年高三上学期期中考试化学试题
辽宁省沈阳市第二中学2022-2023学年高三上学期期中考试化学试题(已下线)化学(云南,安徽,黑龙江,山西,吉林五省通用A卷)-学易金卷:2023年高考第一次模拟考试卷辽宁省北镇市第二高级中学、第三高级中学2023-2024学年高三上学期第四次月考化学试题
名校
解题方法
9 . 应用电化学原理,回答下列问题。
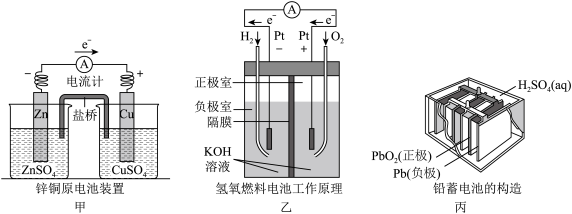
(1)甲中电流计指针偏移时,盐桥(装含琼脂的饱和 溶液)中离子移动的方向:
溶液)中离子移动的方向:_______ 离子移向硫酸锌溶液。
(2)乙中正极反应式为_______ ;若将 换成
换成 ,则负极反应式为
,则负极反应式为_______ 。
(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池_______ 极相连接。
(4)海水中锂元素储量非常丰富,锂是制造化学电源的重要原料,如 电池某电极的工作原理如下图所示:
电池某电极的工作原理如下图所示:

该电池电解质为传导 的固体材料。放电时
的固体材料。放电时 电极是电池的
电极是电池的_______ 极(填“正”或“负”),电极反应式为_______ 。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。现连接如图装置并加入药品(盐桥中的物质不参与反应),进行实验:
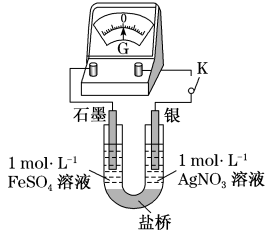
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U形管左侧逐渐加入浓 溶液,发现电流表指针的变化依次为偏移减小→回到零点→逆向偏移。
溶液,发现电流表指针的变化依次为偏移减小→回到零点→逆向偏移。
①实验ⅰ中银作_______ 极。
②综合实验i、ii的现象,得出 和
和 反应的离子方程式是
反应的离子方程式是_______ 。

(1)甲中电流计指针偏移时,盐桥(装含琼脂的饱和
 溶液)中离子移动的方向:
溶液)中离子移动的方向:(2)乙中正极反应式为
 换成
换成 ,则负极反应式为
,则负极反应式为(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池
(4)海水中锂元素储量非常丰富,锂是制造化学电源的重要原料,如
 电池某电极的工作原理如下图所示:
电池某电极的工作原理如下图所示:
该电池电解质为传导
 的固体材料。放电时
的固体材料。放电时 电极是电池的
电极是电池的(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。现连接如图装置并加入药品(盐桥中的物质不参与反应),进行实验:

ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U形管左侧逐渐加入浓
 溶液,发现电流表指针的变化依次为偏移减小→回到零点→逆向偏移。
溶液,发现电流表指针的变化依次为偏移减小→回到零点→逆向偏移。①实验ⅰ中银作
②综合实验i、ii的现象,得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
2022-11-17更新
|
284次组卷
|
3卷引用:辽宁省沈阳市东北育才学校高中部2022-2023学年高二上学期第二次月考化学试题
名校
解题方法
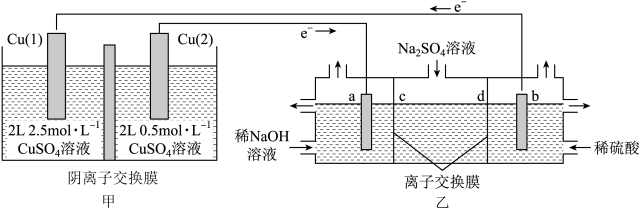
10 . 某化学兴趣小组将两个完全相同的铜片分别放入体积相同、浓度不同的 溶液中形成浓差电池,当两极附近电解质溶液浓度相等时停止放电,利用浓差电池电解
溶液中形成浓差电池,当两极附近电解质溶液浓度相等时停止放电,利用浓差电池电解 溶液(a、b电极均为石墨电极),可制得
溶液(a、b电极均为石墨电极),可制得 、
、 、
、 和NaOH,反应原理如图所示。下列说法正确的是
和NaOH,反应原理如图所示。下列说法正确的是
 溶液中形成浓差电池,当两极附近电解质溶液浓度相等时停止放电,利用浓差电池电解
溶液中形成浓差电池,当两极附近电解质溶液浓度相等时停止放电,利用浓差电池电解 溶液(a、b电极均为石墨电极),可制得
溶液(a、b电极均为石墨电极),可制得 、
、 、
、 和NaOH,反应原理如图所示。下列说法正确的是
和NaOH,反应原理如图所示。下列说法正确的是
A.b电极的电极反应为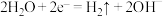 |
| B.c、d分别为阳离子交换膜和阴离子交换膜 |
C.浓差电池放电结束时,甲装置中有 通过阴离子交换膜向右移动 通过阴离子交换膜向右移动 |
| D.当阴极产生2.24L气体时,电路中转移0.2mol电子 |
您最近一年使用:0次
2022-11-14更新
|
352次组卷
|
3卷引用:辽宁省大连市第八中学2022-2023学年高二上学期12月月考化学试题



