名校
解题方法
1 . 以粗 溶液(含
溶液(含 、
、 等杂质)为原料制备
等杂质)为原料制备 的过程。
的过程。
(1)“沉铜”时,溶液的
_______ (填“增大”“减小”或“不变”)。
(2) 、
、 均能与
均能与 反应:
反应: ,
,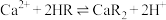 ,
, 、
、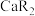 存在于有机相中。“萃取”时用一定量的HR充分萃取,能实现
存在于有机相中。“萃取”时用一定量的HR充分萃取,能实现 与
与 的分离,原因是
的分离,原因是_______ 。HR用量不宜过大,原因是_______ 。
(3)“反萃取”时,向有机相 中加入一定量的稀
中加入一定量的稀 ,可以获得
,可以获得 浓度较大的水溶液。适当增加
浓度较大的水溶液。适当增加 浓度,所得水溶液中
浓度,所得水溶液中 浓度增大,原因是
浓度增大,原因是_______ 。
(4)锌镍二次电池放电时的工作原理如下图所示。_______ (填“正极”或“负极”)。
②在电极材料充足条件下,使用储液罐并让一定量电解质溶液进入电池循环的优点是____ (填序号)。
A.使电池内电解质浓度较为稳定
B.加快电池充、放电的速率
C.获得较为稳定的电流
D.有利于 与
与 直接反应
直接反应
 溶液(含
溶液(含 、
、 等杂质)为原料制备
等杂质)为原料制备 的过程。
的过程。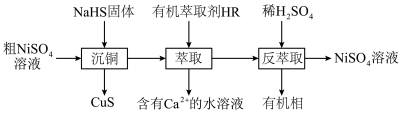
(1)“沉铜”时,溶液的

(2)
 、
、 均能与
均能与 反应:
反应: ,
,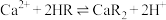 ,
, 、
、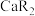 存在于有机相中。“萃取”时用一定量的HR充分萃取,能实现
存在于有机相中。“萃取”时用一定量的HR充分萃取,能实现 与
与 的分离,原因是
的分离,原因是(3)“反萃取”时,向有机相
 中加入一定量的稀
中加入一定量的稀 ,可以获得
,可以获得 浓度较大的水溶液。适当增加
浓度较大的水溶液。适当增加 浓度,所得水溶液中
浓度,所得水溶液中 浓度增大,原因是
浓度增大,原因是(4)锌镍二次电池放电时的工作原理如下图所示。
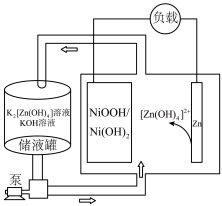
②在电极材料充足条件下,使用储液罐并让一定量电解质溶液进入电池循环的优点是
A.使电池内电解质浓度较为稳定
B.加快电池充、放电的速率
C.获得较为稳定的电流
D.有利于
 与
与 直接反应
直接反应
您最近一年使用:0次
名校
解题方法
2 . 下列电化学相关的说法正确的是
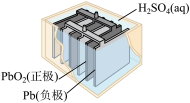 |  | 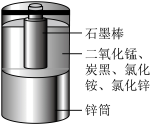 | 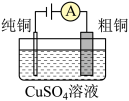 |
铅蓄电池放电时,负极反应为: | 离子交换膜为阴离子交换膜 | 锌筒因发生氧化反应而变薄 |  溶液的浓度始终不变 溶液的浓度始终不变 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 由于钠与锂具有相似的物理和化学性质,因此钠离子电池与锂离子电池的工作原理相似。有机钠离子电池一般采用对苯二甲酸钠(结构简式如图)作为电极材料。有机钠离子电池的工作原理图如图(SEI代表钠离子交换膜)。下列说法中正确的是
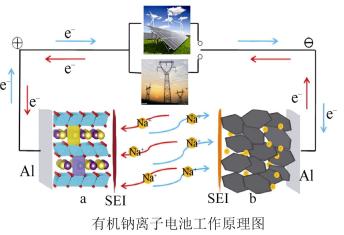
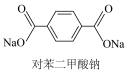
| A.充电时,a连接电源的负极 |
B.放电时,电解质溶液中 向右移动 向右移动 |
C.有机钠离子电池工作时,正极反应式为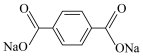 +2Na++2e- +2Na++2e- 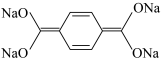 |
| D.用铅蓄电池对该有机钠离子电池充电,每消耗20.7g铅,有机钠离子电池正极区域质量增加4.6g |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
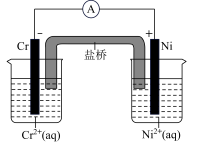

| A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| B.钢铁水闸可用外加电流的阴极保护法防止其腐蚀 |
| C.从电解精炼铜的阳极泥中回收锌、金、银等金属 |
D.如图所示,可判断发生反应为 |
您最近一年使用:0次
2023-07-23更新
|
250次组卷
|
3卷引用:江苏省扬州市高邮市2022-2023学年高二上学期10月月考化学试题
名校
解题方法
5 . 电化学在生产、生活和科学研究中应用十分广泛,认识和研究化学能与电能相互转化的原理和规律具有重要意义。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。
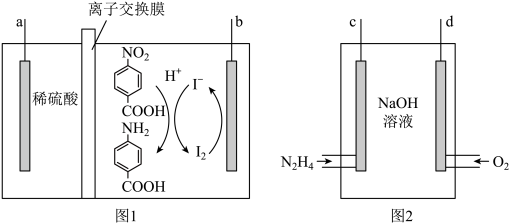
①图2为液态肼 燃料电池,c电极与
燃料电池,c电极与_______ (填“a”或“b”)相连,c电极发生的电极反应式为________ 。
②图1、图2相连时a电极为___________ (填“正”“负”“阴”或“阳”)极。生成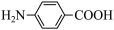 的离子方程式为
的离子方程式为___________ 。
③通过离子交换膜的离子是___________ (填离子符号);当电路中转移 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积___________ ,电解池左室质量变化___________ g。
(2)氮氧化物和 排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的
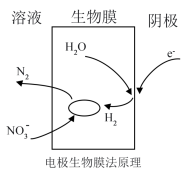
排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为___________ 。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。

①图2为液态肼
 燃料电池,c电极与
燃料电池,c电极与②图1、图2相连时a电极为
 的离子方程式为
的离子方程式为③通过离子交换膜的离子是
 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积(2)氮氧化物和
 排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的
排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
您最近一年使用:0次
2023-07-17更新
|
299次组卷
|
2卷引用:江苏省徐州市铜山区2022-2023学年高二上学期11月期中考试(选择考)化学试题
6 . Al-Te电池是一种二次电池,电解质为 与有机离子液体(
与有机离子液体(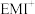 ),该电池放电时在正极生成
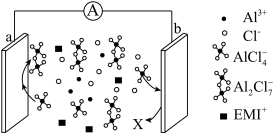
),该电池放电时在正极生成 ,放电过程的示意图如下所示,下列说法
,放电过程的示意图如下所示,下列说法不正确 的是
 与有机离子液体(
与有机离子液体(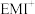 ),该电池放电时在正极生成
),该电池放电时在正极生成 ,放电过程的示意图如下所示,下列说法
,放电过程的示意图如下所示,下列说法
| A.充电时,b电极应与外接电源正极相连 |
B.放电时,图中X表示 |
| C.充电时,a电极的质量将增加 |
| D.放电时,a、b两电极消耗单质的物质的量之比为3:2 |
您最近一年使用:0次
7 . 绿色电源“直接二甲醚( )燃料电池”的工作原理示意图如图所示:
)燃料电池”的工作原理示意图如图所示:
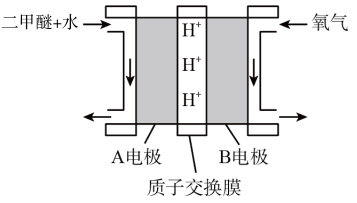
(1)正极为_______ 电极(填“A”或“B”), 移动方向为
移动方向为_______ (填“由A到B”或“由B到A”),写出A电极的电极反应式:_______ 。
(2) 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
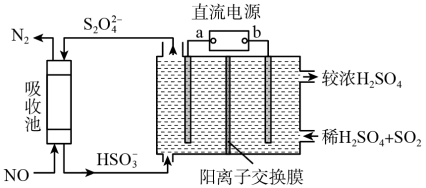
①a是直流电源的_______ 极。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为_______ 。
(3) —空气电池是目前储电能力最高的电池。以
—空气电池是目前储电能力最高的电池。以 —空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为
—空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为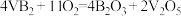 ,
, 极发生的电极反应为
极发生的电极反应为_______ 。
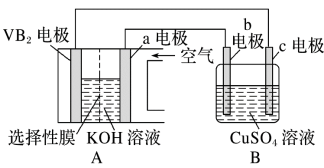
当外电路中通过0.04 mol电子时,B装置内共收集到0.448 L气体(标准状况),若B装置内的液体体积为200 mL(电解前后溶液体积不变),则电解前 溶液的物质的量浓度是
溶液的物质的量浓度是_______ ?(写出计算过程)
 )燃料电池”的工作原理示意图如图所示:
)燃料电池”的工作原理示意图如图所示:
(1)正极为
 移动方向为
移动方向为(2)
 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
(3)
 —空气电池是目前储电能力最高的电池。以
—空气电池是目前储电能力最高的电池。以 —空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为
—空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为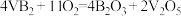 ,
, 极发生的电极反应为
极发生的电极反应为
当外电路中通过0.04 mol电子时,B装置内共收集到0.448 L气体(标准状况),若B装置内的液体体积为200 mL(电解前后溶液体积不变),则电解前
 溶液的物质的量浓度是
溶液的物质的量浓度是
您最近一年使用:0次
解题方法
8 . 二氧化氯( )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下图是目前已开发出的用电解法制取
)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下图是目前已开发出的用电解法制取 的新工艺。装置如图所示:
的新工艺。装置如图所示:
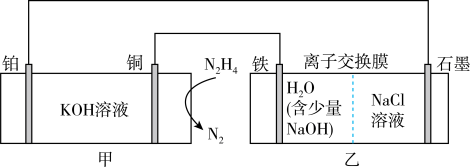
(1)肼( )-空气碱性燃料电池放电效率高,以该电池为电源模拟此工艺。
)-空气碱性燃料电池放电效率高,以该电池为电源模拟此工艺。
①甲装置的能量转化形式主要是_______ 。
②乙装置中离子交换膜的类型是_______ (填字母)。
A.质子交换膜 B.阳离子交换膜 C.阴离子交换膜
③铂电极为_______ 极(填“正”或“负”),石墨电极为_______ 极(填“阴”或“阳”)。
④写出铜电极的电极反应式:_______ 。
⑤写出产生 的电极反应式:
的电极反应式:_______ 。
当铁电极产生标准状况下336mL气体时,通过离子交换膜离子的物质的量为_______ 。
(2)若将肼( )-空气碱性燃料电池改为甲醇燃料电池,原理如下图所示:
)-空气碱性燃料电池改为甲醇燃料电池,原理如下图所示:
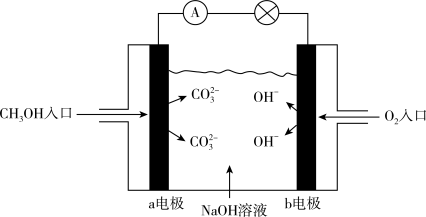
该电池的正极反应式为_______ 。
(3)肼也可作发射火箭时的燃料,以 作氧化剂,两者反应生成氮气和气态水。已知16g
作氧化剂,两者反应生成氮气和气态水。已知16g 在上述反应中放出284kJ的热量,写出该反应的热化学方程式
在上述反应中放出284kJ的热量,写出该反应的热化学方程式_______ 。
 )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下图是目前已开发出的用电解法制取
)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下图是目前已开发出的用电解法制取 的新工艺。装置如图所示:
的新工艺。装置如图所示:
(1)肼(
 )-空气碱性燃料电池放电效率高,以该电池为电源模拟此工艺。
)-空气碱性燃料电池放电效率高,以该电池为电源模拟此工艺。①甲装置的能量转化形式主要是
②乙装置中离子交换膜的类型是
A.质子交换膜 B.阳离子交换膜 C.阴离子交换膜
③铂电极为
④写出铜电极的电极反应式:
⑤写出产生
 的电极反应式:
的电极反应式:当铁电极产生标准状况下336mL气体时,通过离子交换膜离子的物质的量为
(2)若将肼(
 )-空气碱性燃料电池改为甲醇燃料电池,原理如下图所示:
)-空气碱性燃料电池改为甲醇燃料电池,原理如下图所示:
该电池的正极反应式为
(3)肼也可作发射火箭时的燃料,以
 作氧化剂,两者反应生成氮气和气态水。已知16g
作氧化剂,两者反应生成氮气和气态水。已知16g 在上述反应中放出284kJ的热量,写出该反应的热化学方程式
在上述反应中放出284kJ的热量,写出该反应的热化学方程式
您最近一年使用:0次
名校
解题方法
9 . 铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
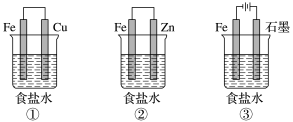
为防止金属Fe被腐蚀,可以采用上述____ (填装置序号)装置原理进行防护:装置③中总反应的离子方程式为_____ 。
(2)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则____ 极的电极反应式为CnH2nOn-4ne-+nH2O=nCO2+4nH+。
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。
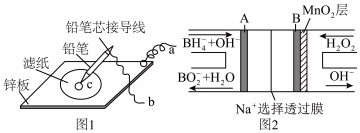
图2电池负极区的电极反应为____ ;若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现____ 色,c位置的电极反应式为____ ,若用淀粉-KI溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯c点处出现蓝色,则b接的是____ (填“A”或“B”)电极。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。

图2电池负极区的电极反应为
您最近一年使用:0次
名校
10 . 电化学普遍应用于生活和生产中,前途广泛,是科研的重点方向。
(1)铅蓄电池为常见的二次电池,其原理为 ,放电时铅蓄电池的正极反应式为
,放电时铅蓄电池的正极反应式为_______ ,放电过程中负极质量_______ (填“增大”、“减小”或“不变”),该电池充电时原负极应接外接电源的_______ 极。
(2)丙烷燃料电池为绿色化学电源,以KOH溶液为电解质溶液时,负极的电极反应式为_______ ,该电池工作时,外电路每流过1mol ,消耗标准状况下的
,消耗标准状况下的
_______ L。
(3)工业上采用Fe、C为电极电解 溶液制
溶液制 。电解时,应以
。电解时,应以_______ 作阴极,电解过程中阴极附近溶液pH将会_______ (填“增大”、“减小”或“不变”),电解时阳极反应式为_______ ,总反应的化学方程式为_______ 。
(4)用原电池原理可以除去酸性废水中的三氯乙烯和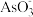 ,其原理如图所示(导电壳内部为纳米铁)。
,其原理如图所示(导电壳内部为纳米铁)。
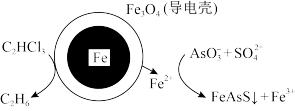
正极电极反应式为:_______ 。
(1)铅蓄电池为常见的二次电池,其原理为
 ,放电时铅蓄电池的正极反应式为
,放电时铅蓄电池的正极反应式为(2)丙烷燃料电池为绿色化学电源,以KOH溶液为电解质溶液时,负极的电极反应式为
 ,消耗标准状况下的
,消耗标准状况下的
(3)工业上采用Fe、C为电极电解
 溶液制
溶液制 。电解时,应以
。电解时,应以(4)用原电池原理可以除去酸性废水中的三氯乙烯和
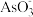 ,其原理如图所示(导电壳内部为纳米铁)。
,其原理如图所示(导电壳内部为纳米铁)。
正极电极反应式为:
您最近一年使用:0次



