名校
解题方法
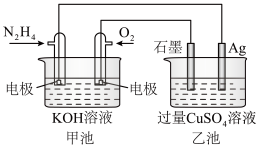
1 . 如图所示,甲池的总反应式为 ,下列关于该装置工作时的说法正确的是
,下列关于该装置工作时的说法正确的是
 ,下列关于该装置工作时的说法正确的是
,下列关于该装置工作时的说法正确的是
| A.该装置工作时,Ag电极上有气体生成 |
B.甲池中负极反应式为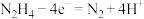 |
| C.甲池和乙池中的溶液的pH均减小 |
D.当甲池中消耗3.2g  时,乙池中理论上最多产生12.8g铜 时,乙池中理论上最多产生12.8g铜 |
您最近一年使用:0次
2023-10-06更新
|
64次组卷
|
2卷引用:黑龙江省哈尔滨市松北区第九中学校2022-2023学年高二上学期12月期中考试化学试题
名校
2 . 电化学在生产、生活中应用广泛。根据原理示意图,回答下列问题:
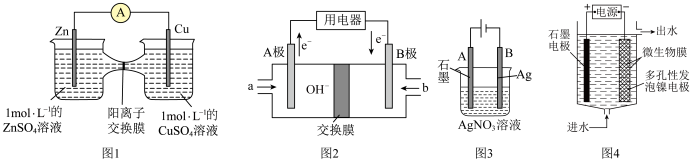
(1)图1为_____ (填“原电池”或“电解池”)装置,若开始时,两电极质量相等,当电路有0.1mole-转移时,两极的质量相差_____ g。
(2)图2为燃料电池,A极为电池的_____ (填“正极”或“负极”),b通入的是_____ (填“燃料”或“空气”),若以甲醇为燃料电池,写出负极的电极反应式:_____ 。
(3)图3中总反应化学方程式为_____ ,若电解池中溶液体积为500mL,当B电极质量增加5.4g时,其pH为_____ (忽略溶液体积变化);
(4)电极生物膜电解脱硝是电化学和微生物工艺的组合。某微生物膜能利用电解产生的活性原子将NO 还原为N2,工作原理如图4所示。若阳极生成标准状况下2.24L气体,理论上可除去NO
还原为N2,工作原理如图4所示。若阳极生成标准状况下2.24L气体,理论上可除去NO 的物质的量为
的物质的量为_____ mol。

(1)图1为
(2)图2为燃料电池,A极为电池的
(3)图3中总反应化学方程式为
(4)电极生物膜电解脱硝是电化学和微生物工艺的组合。某微生物膜能利用电解产生的活性原子将NO
 还原为N2,工作原理如图4所示。若阳极生成标准状况下2.24L气体,理论上可除去NO
还原为N2,工作原理如图4所示。若阳极生成标准状况下2.24L气体,理论上可除去NO 的物质的量为
的物质的量为
您最近一年使用:0次
名校
3 . 我国科学家研发了一种Na—CO2二次电池,将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料。充电时的总反应为:2Na2CO3+C=3CO2+4Na.下列说法错误的是


| A.充电时,镍网与电源的正极相连 |
B.放电时,ClO 向钠电极移动 向钠电极移动 |
C.充电时,阴极反应为:2CO +C-4e-=3CO2 +C-4e-=3CO2 |
| D.充电时释放CO2,放电时吸收CO2 |
您最近一年使用:0次
4 . 我国科学家研发了一种水系可逆Al-CO2电池,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充电、放电时,复合膜层间的H2O解离成H+和OH—,工作原理如图所示。下列说法正确的是
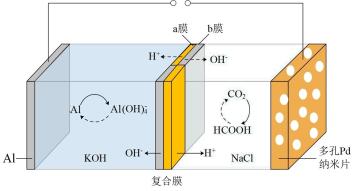

| A.a膜是阴离子交换膜,b膜是阳离子交换膜 |
B.放电时负极的电极反应式为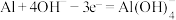 |
| C.放电时多孔Pd纳米片附近pH不变 |
| D.充电时Al与外接直流电源正极相连,将电能转化为化学能 |
您最近一年使用:0次
解题方法
5 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)丙池中E电极为_______ (填“正极”、“负极”、“阴极”或“阳极”)
(2)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为_______ mL(标况)。
(3)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______ 。
(4)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O=Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。
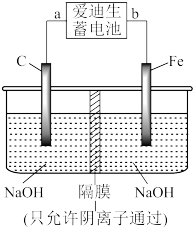
①此装置中爱迪生蓄电池的正极是_______ (填“a”或“b”)
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为_______ 。

(1)丙池中E电极为
(2)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为
(3)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______ 。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |

①此装置中爱迪生蓄电池的正极是
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为
您最近一年使用:0次
名校
解题方法
6 . 粗铜中一般含有锌、铁、银、金等杂质。在如图所示的装置中,甲池的总反应方程式为2CH3OH+3O2+4KOH=2K2CO3+6H2O。接通电路一段时间后,精Cu电极质量增加了3.2 g。在此过程中,下列说法正确的是
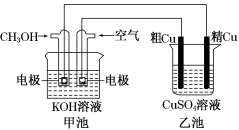
| A.乙池中CuSO4溶液的浓度减小 |
| B.甲池中理论上消耗标准状况下空气的体积是2.8 L(空气中O2体积分数以20%计算) |
| C.甲池是电能转化为化学能的装置,乙池是化学能转化为电能的装置 |
D.甲池通入CH3OH一极的电极反应为CH3OH-6e-+2H2O=CO +8H+ +8H+ |
您最近一年使用:0次
2022-12-11更新
|
233次组卷
|
3卷引用:黑龙江省哈尔滨市第九中学2022-2023学年高二上学期期末化学试题
名校
解题方法
7 .  转化是环保和资源利用的研究课题。将烧碱吸收
转化是环保和资源利用的研究课题。将烧碱吸收 后的溶液加入如图装置,可以回收单质硫,甲为二甲醚(
后的溶液加入如图装置,可以回收单质硫,甲为二甲醚( )-空气燃料电池。已知常温下,
)-空气燃料电池。已知常温下, 的电离常数
的电离常数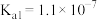 ,
,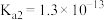 ;S可与NaOH溶液反应。回答下列问题:
;S可与NaOH溶液反应。回答下列问题: KHS溶液中,含硫微粒浓度由大到小顺序为
KHS溶液中,含硫微粒浓度由大到小顺序为_______ 。
(2)X极电极反应式____ 。
(3)电解一段时间后,甲池溶液pH_______ (填“增大”、“减小”或“不变”)。
(4)M交换膜为_______ 离子交换膜(填“阳”、“阴”或“质子”)。
(5)乙池总反应方程式为_______ 。
(6)当Y极消耗3.2g气体时,标准状况下W极生成气体的体积为_______ 。
 转化是环保和资源利用的研究课题。将烧碱吸收
转化是环保和资源利用的研究课题。将烧碱吸收 后的溶液加入如图装置,可以回收单质硫,甲为二甲醚(
后的溶液加入如图装置,可以回收单质硫,甲为二甲醚( )-空气燃料电池。已知常温下,
)-空气燃料电池。已知常温下, 的电离常数
的电离常数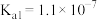 ,
,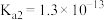 ;S可与NaOH溶液反应。回答下列问题:
;S可与NaOH溶液反应。回答下列问题: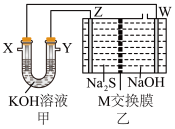
 KHS溶液中,含硫微粒浓度由大到小顺序为
KHS溶液中,含硫微粒浓度由大到小顺序为(2)X极电极反应式
(3)电解一段时间后,甲池溶液pH
(4)M交换膜为
(5)乙池总反应方程式为
(6)当Y极消耗3.2g气体时,标准状况下W极生成气体的体积为
您最近一年使用:0次
2022-11-23更新
|
186次组卷
|
2卷引用:黑龙江省哈尔滨市阿城区第一中学校2022-2023学年高二11月阶段性检测化学试题
解题方法
8 . 如图所示的电化学装置,电极Ⅰ为Al,其它电极均为Cu,下列说法正确的是


| A.电极Ⅱ质量逐渐减小 |
| B.盐桥中装有含氯化钾饱和溶液的琼胶,其作用是传递电子 |
C.电极Ⅲ的电极反应: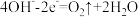 |
| D.若用该装置电解精炼铜,电极Ⅲ为粗铜,电极Ⅳ为精铜 |
您最近一年使用:0次
2022-11-06更新
|
238次组卷
|
4卷引用:黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期期中化学试题
黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期期中化学试题浙江省温州十校联合体2022-2023学年高二上学期期中联考化学试题(已下线)【2022】【高二上】【期中考】【温州十校】【高中化学】【李鼎收集】浙江省温州市2022-2023学年高二上学期11月期中考试化学试题
名校
9 . 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
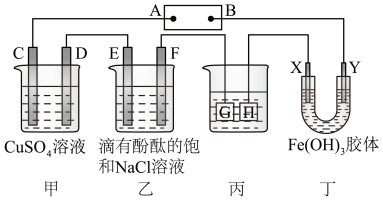
(1)B极是电源的____ (填“正极”或“负极”),一段时间后,丁中X极附近的颜色逐渐____ (填“变深”或“变浅”)。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为___ 。
(3)现用丙装置给铜件镀银,则H应是___ 。若乙溶液体积为500mL,当乙中溶液的pH=13时,丙中镀件上析出银的质量为___ ,甲中溶液的pH____ (填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为____ 。

(1)B极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应是
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为
您最近一年使用:0次
2022-10-25更新
|
161次组卷
|
2卷引用:黑龙江省大庆市东风中学2022-2023学年高二10月月考化学试题
解题方法
10 . 某兴趣小组设计以甲烷、氧气酸性燃料电池为电源电解 溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
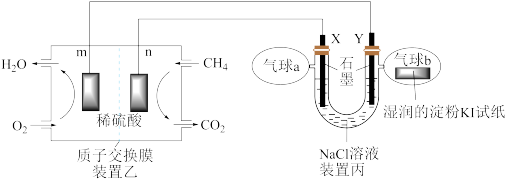
(1)m极为_______ 极,该电极发生的电极反应式为_______
(2)装置丙Y极电极反应式为_______ ;装置乙中n电极发生反应的电极反应式为:_______
(3)另一化学兴趣小组利用已知浓度的酸性KMnO4标准溶液,测定某亚磷酸溶液的浓度。已知亚磷酸(H3PO3)具有较强的还原性,能被酸性高锰酸钾溶液氧化为磷酸。
①该小组用移液管准确量取25.00mL亚磷酸溶液于锥形瓶中,选用0.1mol/L的酸性KMnO4标准溶液进行滴定,则滴定终点的现象为:_______ 。
②已知三次滴定数据如下表,该亚磷酸溶液的物质的量浓度为_______  。(保留小数点后两位)
。(保留小数点后两位)
③某研究性学习小组在实验室中配制1mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是_______ 。
A. 实验中所用到的滴定管、容量瓶,在使用前均需要检漏;
B. 如果实验中需用60mL的稀硫酸标准溶液,配制时应选用100mL容量瓶;
C. 容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小;
D. 酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大。
 溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
(1)m极为
(2)装置丙Y极电极反应式为
(3)另一化学兴趣小组利用已知浓度的酸性KMnO4标准溶液,测定某亚磷酸溶液的浓度。已知亚磷酸(H3PO3)具有较强的还原性,能被酸性高锰酸钾溶液氧化为磷酸。
①该小组用移液管准确量取25.00mL亚磷酸溶液于锥形瓶中,选用0.1mol/L的酸性KMnO4标准溶液进行滴定,则滴定终点的现象为:
②已知三次滴定数据如下表,该亚磷酸溶液的物质的量浓度为
 。(保留小数点后两位)
。(保留小数点后两位)| 试验编号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 22.00 |
| 2 | 0.50 | 22.50 |
| 3 | 0.50 | 25.50 |
A. 实验中所用到的滴定管、容量瓶,在使用前均需要检漏;
B. 如果实验中需用60mL的稀硫酸标准溶液,配制时应选用100mL容量瓶;
C. 容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小;
D. 酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大。
您最近一年使用:0次



