名校
解题方法
1 . 一种简单的原电池装置如图所示。据图回答下列问题。
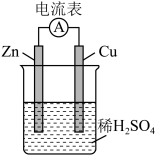
(1)锌是该电池的_______ (填“正”或“负”)极。Zn片上发生的电极反应为___________ 。Cu片上发生的电极反应为_________ 。能证明化学能转化为电能的实验现象为___________ 。
(2)装置中稀硫酸的作用是___________。
(3)某原电池的总反应是Zn+Cu2+=Zn2+ +Cu,该原电池的正确组成是______ 。
(4)下列反应通过原电池装置,不能实现把化学能直接转化为电能的是___________ (填序号)。
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O

(1)锌是该电池的
(2)装置中稀硫酸的作用是___________。
| A.电极材料 | B.电极反应物 | C.电子导体 | D.离子导体 |
(3)某原电池的总反应是Zn+Cu2+=Zn2+ +Cu,该原电池的正确组成是
| A | B | C | D |
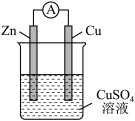 | 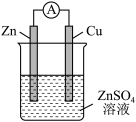 |  | 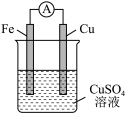 |
(4)下列反应通过原电池装置,不能实现把化学能直接转化为电能的是
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O
您最近一年使用:0次
名校
2 . 电化学及其产品与能源、材料、环境和健康等领域紧密联系,被广泛地应用于生产、生活的许多方面。
(1)如图为氢氧燃料电池的构造示意图。
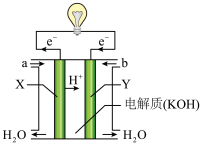
①氧气从___________ (填“a”或“b”)口通入;电池工作时,OH-向___________ (填“X”或“Y”)极移动。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,则电池工作时负极电极反应式为___________ 。
(2)王航同学用石墨作电极电解Cu(NO3)2溶液。
①电解过程中,阳极的电极反应式为___________ 。
②电解一段时间后,溶液蓝色变浅。若要将电解质溶液恢复到电解前的状态,可加入的物质是___________ (任填一种)。
(3)铅酸蓄电池有电压稳定、安全、价格低廉等优点而广泛应用于生产生活中,其电池反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水,电化学降解NO
2PbSO4+2H2O。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水,电化学降解NO 的原理如图所示。
的原理如图所示。
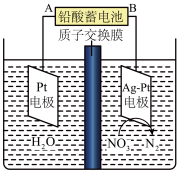
①A为铅酸蓄电池的___________ (填“Pb”或“PbO2”)极。
②Ag-Pt电极上的电极反应式为___________ 。
③若电路中转移了2mole-,则铅酸蓄电池的正极增重___________ g;质子交换膜两侧电解液的质量变化差(|Δm左|-|Δm右|)为___________ g。
(1)如图为氢氧燃料电池的构造示意图。

①氧气从
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,则电池工作时负极电极反应式为
(2)王航同学用石墨作电极电解Cu(NO3)2溶液。
①电解过程中,阳极的电极反应式为
②电解一段时间后,溶液蓝色变浅。若要将电解质溶液恢复到电解前的状态,可加入的物质是
(3)铅酸蓄电池有电压稳定、安全、价格低廉等优点而广泛应用于生产生活中,其电池反应为Pb+PbO2+2H2SO4
 2PbSO4+2H2O。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水,电化学降解NO
2PbSO4+2H2O。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水,电化学降解NO 的原理如图所示。
的原理如图所示。
①A为铅酸蓄电池的
②Ag-Pt电极上的电极反应式为
③若电路中转移了2mole-,则铅酸蓄电池的正极增重
您最近一年使用:0次
名校
3 . Ⅰ.一定条件下,容积2L的密闭容器中,将2 L气体和3
L气体和3 M气体混合,发生如下反应:
M气体混合,发生如下反应: ,10s末,生成2.4
,10s末,生成2.4 R,测得Q的浓度为0.4
R,测得Q的浓度为0.4 。
。
(1)前10s内用M表示的化学反应速率为_______ 。
(2)化学方程式中x值为_______ 。
(3)10s末L的转化率是_______ 。
(4)下列说法可以说明该反应已达平衡的是_______ 。(填序号)
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④单位时间内消耗3 M的同时生成3
M的同时生成3 R
R
⑤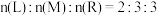
Ⅱ.乙醇燃料电池因其无污染,且原料来源广可再生被人们青睐。现有如下图所示装置,所有电极均为 ,请按要求回答下列问题:
,请按要求回答下列问题:
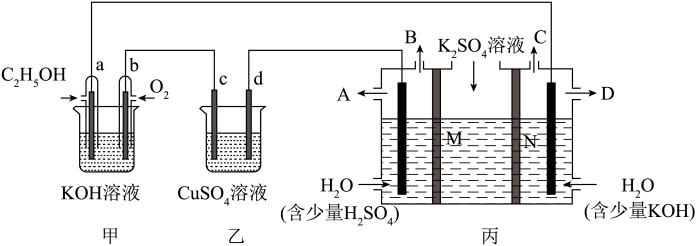
(5)写出甲装置a极的电极反应式_______ 。
(6)若乙池中 溶液足量,当b极消耗标准状况下
溶液足量,当b极消耗标准状况下 11.2
11.2 时,d电极增重
时,d电极增重_______ g。
(7)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则N为_______ 离子交换膜(填“阴”或“阳”),产生B气体的电极反应式为_______ 。
 L气体和3
L气体和3 M气体混合,发生如下反应:
M气体混合,发生如下反应: ,10s末,生成2.4
,10s末,生成2.4 R,测得Q的浓度为0.4
R,测得Q的浓度为0.4 。
。(1)前10s内用M表示的化学反应速率为
(2)化学方程式中x值为
(3)10s末L的转化率是
(4)下列说法可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④单位时间内消耗3
 M的同时生成3
M的同时生成3 R
R⑤
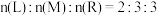
Ⅱ.乙醇燃料电池因其无污染,且原料来源广可再生被人们青睐。现有如下图所示装置,所有电极均为
 ,请按要求回答下列问题:
,请按要求回答下列问题:
(5)写出甲装置a极的电极反应式
(6)若乙池中
 溶液足量,当b极消耗标准状况下
溶液足量,当b极消耗标准状况下 11.2
11.2 时,d电极增重
时,d电极增重(7)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则N为
您最近一年使用:0次
解题方法
4 . 科学家近年发明了一种新型Zn-CO2水介质可充电电池,放、充电时可以实现CO2和HCOOH的互相转化。其电池结构如图所示,电池中间由反向放置的双极膜分隔两极的电解质溶液,双极膜中的H2O可解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列关于该电池的说法错误 的是
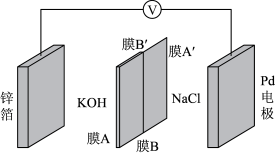

A.放电时锌箔电极的反应式为:Zn-2e-+4OH-=Zn(OH) |
| B.若放电时外电路通过1mol电子,则理论上通过双极膜向两极迁移的离子数为2NA |
| C.若膜A和A'、B和B'分别为阳、阴离子交换膜,则放电时膜A、B工作 |
| D.充电时Pd电极的反应式为:HCOOH+2OH--2e-=CO2+2H2O |
您最近一年使用:0次
2022-11-10更新
|
432次组卷
|
3卷引用:陕西省延安市第一中学2021-2022学年高一下学期期末考试化学试题
陕西省延安市第一中学2021-2022学年高一下学期期末考试化学试题(已下线)第05讲 化学能转化为电能-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)辽宁省部分省级示范性高中2022-2023学年高二下学期3月测试化学试题
名校
解题方法
5 . 电化学原理在工业生产、物质制备、污染物理处理等方面应用广泛,请按要求回答下列问题。
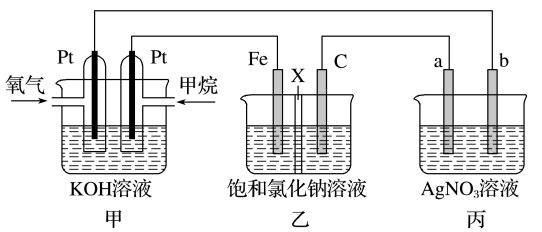
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是___________ 。
(2)乙中X是___________ 交换膜,向乙中加入几滴酚酞溶液,工作一段时间后___________ 电极(填“铁”或“碳”)附近溶液变红,该电极的电极反应式为___________ 。
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为___________ 。
(4)欲用丙装置给铜镀银,b应是___________ (填化学式)。
(5)将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为___________ L
Ⅱ.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统原理示意图。
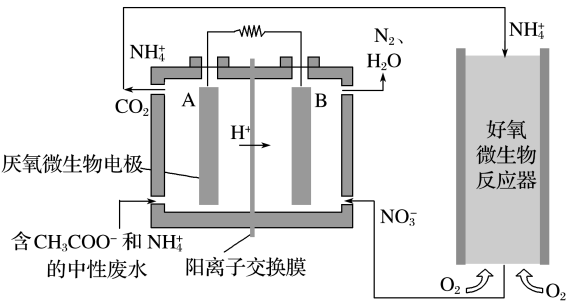
(6)A极的电极反应式为___________ ,A、B两极生成CO2和N2的物质的量之比为___________ 。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。

请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为
(4)欲用丙装置给铜镀银,b应是
(5)将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为
Ⅱ.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统原理示意图。

(6)A极的电极反应式为
您最近一年使用:0次
2022-08-27更新
|
393次组卷
|
2卷引用:黑龙江省大庆铁人中学2021-2022学年高一下学期期末考试化学试题
解题方法
6 . 用如图实验装置进行相应实验,能达到实验目的的是
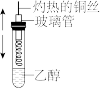 | 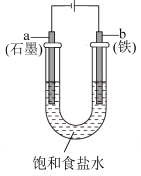 |  |  |
| 甲 | 乙 | 丙 | 丁 |
| A.装置甲:乙醇可以被氧化为乙醛 |
| B.装置乙:电解饱和食盐水制金属钠 |
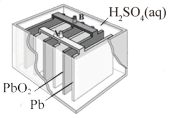
| C.装置丙:铅蓄电池负极的质量减小 |
D.装置丁:用 气体和饱和 气体和饱和 溶液能出现喷泉现象 溶液能出现喷泉现象 |
您最近一年使用:0次
解题方法
7 . 根据电化学原理回答下列问题:
(1)一种电化学装置如图所示,能溶解辉铜矿石(主要成分是Cu2S)制得硫酸铜。其电池总反应为Cu2S+5Fe2(SO4)3+4H2O=10FeSO4+2CuSO4+4H2SO4。
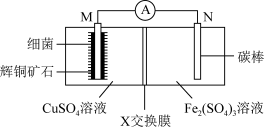
①电极M的电极反应式为____ ,电极N上发生____ (填“氧化”或“还原”)反应。
②X交换膜为____ (填“阳”或“阴”)离子交换膜。工作过程中,左室溶液质量____ (填“增大”或“减小”),电路中每转移2mol电子,右室溶液变化的____ g。
(2)一种将废水中的氯乙烯(C2H3Cl)转化成对环境无害的微生物电池装置如图,同时利用此装置在铁上镀铜。

①I极为____ (填“正极”、“负极”、“阴极”或“阳极”);镀铜时,____ (填“X”或“Y”)与铁电极相连。
②若I极消耗0.1mol氯乙烯(反应中生成CO2、H+、Cl-),则铁电极增重____ g,硫酸铜溶液的浓度将___ (填“增大”、“减小”或“不变”)。
(1)一种电化学装置如图所示,能溶解辉铜矿石(主要成分是Cu2S)制得硫酸铜。其电池总反应为Cu2S+5Fe2(SO4)3+4H2O=10FeSO4+2CuSO4+4H2SO4。

①电极M的电极反应式为
②X交换膜为
(2)一种将废水中的氯乙烯(C2H3Cl)转化成对环境无害的微生物电池装置如图,同时利用此装置在铁上镀铜。

①I极为
②若I极消耗0.1mol氯乙烯(反应中生成CO2、H+、Cl-),则铁电极增重
您最近一年使用:0次
名校
解题方法
8 . 利用氢气燃料电池电解CuSO4溶液、MgCl2溶液,装置如图所示:
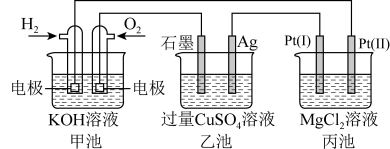
下列说法错误的是

下列说法错误的是
| A.甲池是将化学能转化为电能的装置,乙、丙池是将电能转化为化学能的装置 |
| B.反应一段时间后,向乙池中加入一定量CuO能使CuSO4溶液恢复到原浓度 |
| C.丙池的Pt(II)电极发生的电极反应为2Cl--2e-=Cl2↑ |
| D.甲池中消耗280mLO2,此时丙池中理论上最多产生1.45g固体 |
您最近一年使用:0次
2022-07-11更新
|
276次组卷
|
2卷引用:河北省承德市2021-2022学年高一下学期期末考试化学试题
名校
解题方法
9 . I.如图所示,A、B、C、D为惰性电极,回答下列问题:_______ (填“原电池”或“电解池”)。
(2)工作一段时间后,甲中出现浑浊,甲中发生反应的化学方程式为_______ 。
(3)丁装置欲在铁上镀银,则极板M的材料为_______ 。
(4)工作一段时间后,丙中C、D两极上都产生2.24L气体(标准状况), C极气体为_______ (填化学式),欲使溶液恢复到起始状态,可向溶液中加入_______ ( 填序号)。
A. CuO B. Cu2(OH)2CO3 C. Cu(OH)2 D. CuCO3
(5)当A电极产生22.4L气体(标准状况) ,理论上乙中PbO2电极质量改变_______ g。
II.全钒液流电池的寿命远远高于铅酸蓄电池,图为其基本工作原理示意图,两电极可为惰性电极,为保证电池稳定运行,“隔膜”选用质子交换膜,钒电池是以溶解于一定浓度硫酸溶液中的不同种类的钒离子(V2+、V3+、 VO2+、 )为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O
)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O V2++
V2++ +2H+,放电时,H+由B区通过隔膜移动到A区。回答下列问题:
+2H+,放电时,H+由B区通过隔膜移动到A区。回答下列问题: _______ 区(填“正极”或“负极”), B区电解液含有的钒离子为_______ 。
(7)充电时,B 区发生的电极反应式为_______ 。

(2)工作一段时间后,甲中出现浑浊,甲中发生反应的化学方程式为
(3)丁装置欲在铁上镀银,则极板M的材料为
(4)工作一段时间后,丙中C、D两极上都产生2.24L气体(标准状况), C极气体为
A. CuO B. Cu2(OH)2CO3 C. Cu(OH)2 D. CuCO3
(5)当A电极产生22.4L气体(标准状况) ,理论上乙中PbO2电极质量改变
II.全钒液流电池的寿命远远高于铅酸蓄电池,图为其基本工作原理示意图,两电极可为惰性电极,为保证电池稳定运行,“隔膜”选用质子交换膜,钒电池是以溶解于一定浓度硫酸溶液中的不同种类的钒离子(V2+、V3+、 VO2+、
 )为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O
)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O V2++
V2++ +2H+,放电时,H+由B区通过隔膜移动到A区。回答下列问题:
+2H+,放电时,H+由B区通过隔膜移动到A区。回答下列问题: 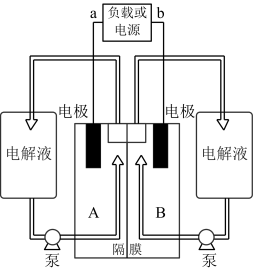
(7)充电时,B 区发生的电极反应式为
您最近一年使用:0次
名校
10 . 一种新型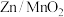 水系电池的工作原理如图所示,放电时锌箔作负极。下列说法正确的是
水系电池的工作原理如图所示,放电时锌箔作负极。下列说法正确的是
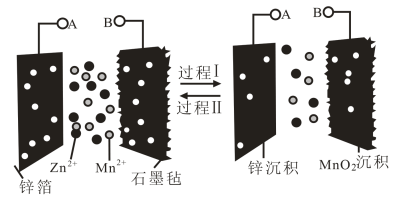
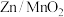 水系电池的工作原理如图所示,放电时锌箔作负极。下列说法正确的是
水系电池的工作原理如图所示,放电时锌箔作负极。下列说法正确的是
A.过程Ⅰ锌箔发生的反应为 |
B.过程Ⅰ石墨毡电极的电极反应为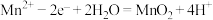 |
| C.过程Ⅱ为充电过程,A连电源的正极 |
| D.过程Ⅱ石墨毡电极和锌箔质量均增加 |
您最近一年使用:0次
2022-07-07更新
|
324次组卷
|
2卷引用:山东省潍坊2021-2022学年高一下学期期末测试化学试题



