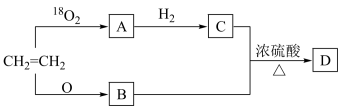
1 . 以乙烯为原料,在一定条件下可以转化为A、B、C,最后合成有机化合物D,转化关系如下图所示:
请回答:
(1)写出有机物B的官能团名称:________________ 。
(2)写出CH3=CH2→A化学方程式:________________ 。
(3)有机化合物D的相对分子质量为:________________ 。
请回答:
(1)写出有机物B的官能团名称:
(2)写出CH3=CH2→A化学方程式:
(3)有机化合物D的相对分子质量为:
您最近一年使用:0次
2017-03-26更新
|
477次组卷
|
4卷引用:2017届浙江省绍兴市高三3月教学质量调测考试化学试卷2
2 .
(1)乙烯是石油裂解气的主要成分,下图是石蜡油在炽热碎瓷片的作用下裂解,下列装置检验其性质,完成下列问题。
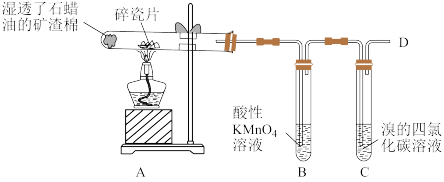
(1)A中碎瓷片的作用是_____________ 。
(2)B中反应类型是_____________ ,C中实验现象是__________________ 。
(2)用如图所示的装置进行实验,回答下列问题:
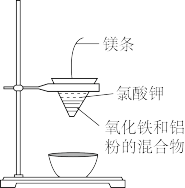
(3)写出该反应的化学方程式:_____________________ 。
(4)选出该实验的实验现象(把序号填写在横线上):________________ 。
①镁条剧烈燃烧;②放出大量的热,并发出耀眼的光芒;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
(5)写出下列操作或物质的作用:镁条________ ;氯酸钾_________ ;蒸发皿盛沙____________ 。
(1)乙烯是石油裂解气的主要成分,下图是石蜡油在炽热碎瓷片的作用下裂解,下列装置检验其性质,完成下列问题。

(1)A中碎瓷片的作用是
(2)B中反应类型是
(2)用如图所示的装置进行实验,回答下列问题:

(3)写出该反应的化学方程式:
(4)选出该实验的实验现象(把序号填写在横线上):
①镁条剧烈燃烧;②放出大量的热,并发出耀眼的光芒;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
(5)写出下列操作或物质的作用:镁条
您最近一年使用:0次
3 . 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:

(1)写出A、B、C、D的结构简式:
A________ ,B________ ,C________ ,D________ 。
(2)写出①、②、③、④四步反应的化学方程式,并注明反应类型
①____________________ ,反应类型________ 。
②____________________ ,反应类型________ 。
③____________________ ,反应类型________ 。
④____________________ ,反应类型________ 。
(3)烃A的燃烧反应方程式___________________________

(1)写出A、B、C、D的结构简式:
A
(2)写出①、②、③、④四步反应的化学方程式,并注明反应类型
①
②
③
④
(3)烃A的燃烧反应方程式
您最近一年使用:0次
4 . (1)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题。
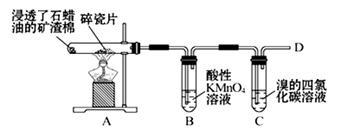
①A中碎瓷片的作用是______________ 。
②B中反应类型是______________ 。C中实验现象是__________________________ 。
③在D处点燃前必须进行的操作是___________________________ 。
(2)制取氯乙烷(CH3CH2Cl)的最佳方法是(用化学方程式表示):________________ 。
(3)来自石油的另一产品是苯,请写出由苯制硝基苯的化学方程式:_______________ 。
(4)该实验中D处乙烯燃烧的化学方程式:_________________________________ 。

①A中碎瓷片的作用是
②B中反应类型是
③在D处点燃前必须进行的操作是
(2)制取氯乙烷(CH3CH2Cl)的最佳方法是(用化学方程式表示):
(3)来自石油的另一产品是苯,请写出由苯制硝基苯的化学方程式:
(4)该实验中D处乙烯燃烧的化学方程式:
您最近一年使用:0次
5 . 已知:2CH2=CH2+O2 2CH3CHO,以乙烯、空气、水为原料在一定条件下能实现如下图所示的转化。
2CH3CHO,以乙烯、空气、水为原料在一定条件下能实现如下图所示的转化。

(1)物质C俗称_______ ,其结构简式为_______ ;
(2)写出由A→B的化学方程式_______ ;
(3)写出由B+C→乙酸乙酯的化学方程式_______ ,该反应是_______ 反应。
 2CH3CHO,以乙烯、空气、水为原料在一定条件下能实现如下图所示的转化。
2CH3CHO,以乙烯、空气、水为原料在一定条件下能实现如下图所示的转化。
(1)物质C俗称
(2)写出由A→B的化学方程式
(3)写出由B+C→乙酸乙酯的化学方程式
您最近一年使用:0次
10-11高一下·海南·阶段练习
6 . (1)下列括号内的物质为杂质,将除去下列各组混合物中杂质所需的试剂填写在横线上:
苯(甲苯)________ ;苯(乙醇)________ ;甲苯(溴)________ 。
(2)实验室由电石中的碳化钙和水反应制取乙炔,该反应的化学方程式为_____ ,实验中为了减缓反应速率,常用______ 代替水,若实验中产生的气体存在难闻的气味,可以用_________________ (填试剂)加以除去。
(3)某兴趣小组的同学在实验室里制取的乙烯中常混有少量二氧化硫,他们设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

1)I、II、III、IV装置可盛放的试剂依次为_______ (填字母)
①品红溶液 ②NaOH溶液 ③浓硫酸 ④酸性KMnO4溶液
2)能说明SO2气体存在的现象是____ 。
3)使用装置III的目的是___________ 。
4)确定含有乙烯的现象是__________ 。
苯(甲苯)
(2)实验室由电石中的碳化钙和水反应制取乙炔,该反应的化学方程式为
(3)某兴趣小组的同学在实验室里制取的乙烯中常混有少量二氧化硫,他们设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

1)I、II、III、IV装置可盛放的试剂依次为
①品红溶液 ②NaOH溶液 ③浓硫酸 ④酸性KMnO4溶液
| A.④②①③ | B.①②①③ | C.①②①④ | D.④②①④ |
2)能说明SO2气体存在的现象是
3)使用装置III的目的是
4)确定含有乙烯的现象是
您最近一年使用:0次
9-10高二下·江苏盐城·期末
7 . 下列实验操作或叙述正确的是_________ (填序号)
A.乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇
B.将无水乙醇和浓硫酸按体积比1∶3混合,加热至140℃制取乙烯
C.为证明溴乙烷分子中溴元素的存在,可向溴乙烷中加入NaOH溶液,加热,加入稀硝酸至溶液呈酸性,加入AgNO3溶液,看是否有淡黄色沉淀
D.向碘水中加入酒精,萃取碘水中的碘
E.用饱和食盐水代替水与电石制备乙炔,目的是为了减缓反应速率
F.将乙烯分别通入酸性KMnO4溶液和溴水中均褪色,褪色原理相同
A.乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇
B.将无水乙醇和浓硫酸按体积比1∶3混合,加热至140℃制取乙烯
C.为证明溴乙烷分子中溴元素的存在,可向溴乙烷中加入NaOH溶液,加热,加入稀硝酸至溶液呈酸性,加入AgNO3溶液,看是否有淡黄色沉淀
D.向碘水中加入酒精,萃取碘水中的碘
E.用饱和食盐水代替水与电石制备乙炔,目的是为了减缓反应速率
F.将乙烯分别通入酸性KMnO4溶液和溴水中均褪色,褪色原理相同
您最近一年使用:0次
9-10高二下·云南昆明·期末
8 . 实验室制乙烯通常采用95%的乙醇与浓硫酸(体积比为1:3)混合加热到170℃制得,请根据实验回答下列问题。
(1)其制备原理可用化学方程式表示为:_______________________________ ,浓硫酸的作用是__________ 。
反应装置中除了加入乙醇和浓硫酸外,还需要加入______ (填物质名称)
(2)请从以下装置中选择该反应的反应装置( )

(3)反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过下图实验装置。(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用。)

A.①②中盛放的试剂分别为①_______ ;②__________ ;(填试剂名称)
B.能说明二氧化硫气体存在的现象是________________________ 。
C.能确认含有乙烯的现象是________________________________ 。
(1)其制备原理可用化学方程式表示为:
反应装置中除了加入乙醇和浓硫酸外,还需要加入
(2)请从以下装置中选择该反应的反应装置

(3)反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过下图实验装置。(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用。)

A.①②中盛放的试剂分别为①
B.能说明二氧化硫气体存在的现象是
C.能确认含有乙烯的现象是
您最近一年使用:0次



