名校
解题方法
1 . 某高分子材料的结构简式可表示为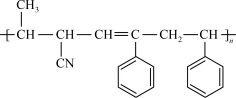 ,则不属于生成该高分子材料的单体是
,则不属于生成该高分子材料的单体是
 ,则不属于生成该高分子材料的单体是
,则不属于生成该高分子材料的单体是A. | B. | C.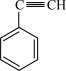 | D.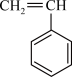 |
您最近一年使用:0次
2021-07-10更新
|
646次组卷
|
7卷引用:广东省肇庆市2020-2021学年高二下学期期末教学质量检测化学(有机化学基础)试题
2 . 克矽平是一种治疗矽肺病的药物,其合成路线如图(反应均在一定条件下进行):

(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以在一定条件下与氢气发生反应生成,该反应类型为__________ ,反应化学方程式为__________ 。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应,则所需另一种反应物的分子式__________ 。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是(填字母)__________ 。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅲ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(填字母)__________ 。
A.乙烷 B.乙烯 C.乙醇 D.苯

(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以在一定条件下与氢气发生反应生成,该反应类型为
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应,则所需另一种反应物的分子式
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是(填字母)
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅲ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(填字母)
A.乙烷 B.乙烯 C.乙醇 D.苯
您最近一年使用:0次
3 . 下列表达方式或说法正确的是
A. 分子模型示意图: 分子模型示意图: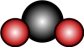 |
B.顺式聚异戊二烯的结构简式: |
C.聚丙烯的结构简式为: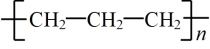 |
D. 的电子式: 的电子式: |
您最近一年使用:0次
4 . I.CO2的循环利用是“碳达峰、碳中和”主要措施。
(1)据VSEPR理论可知CO2中心原子价层电子对数为_______
(2)CO2与环氧丙烷 ( )一定条件下反应生成可降解塑料(
)一定条件下反应生成可降解塑料(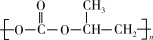 ),写出反应的化学方程式
),写出反应的化学方程式_______
II.工业上用Cu-ZnO作催化剂通过反应①来生产甲醇,同时也会有副反应②发生。
① CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
(3)已知298K时,相关物质的能量如图所示,则ΔH1=_______ kJ/mol,(保留三位有效数字),反应①低温_______ 自发进行(填“能”、“不能”)。

(4)在恒温恒容的容器中,充入0.5mol CO2(g)和1.0mol H2(g),起始压强为p kPa,一段时间后达到平衡测得容器中生成0.3mol H2O(g),压强为 p kPa,反应②的平衡常数Kp=
p kPa,反应②的平衡常数Kp=_______ (列出计算式即可)。(分压=物质的量分数×总压,用平衡分压代替平衡浓度计算的平衡常数即为Kp)。
(5)下列说法中不正确的是_______
III.催化加氢合成乙烯是CO2综合利用研究的热点领域,其反应为:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
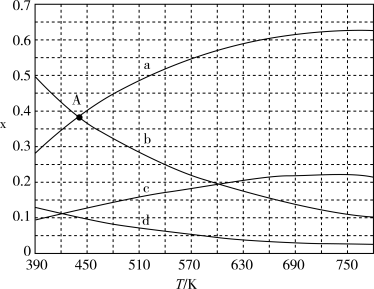
(6)理论计算表明,原料初始组成 ,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是_______ ,该反应△H _______ 0(填“>”、“<”或“=”)
(1)据VSEPR理论可知CO2中心原子价层电子对数为
(2)CO2与环氧丙烷 (
 )一定条件下反应生成可降解塑料(
)一定条件下反应生成可降解塑料(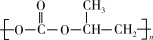 ),写出反应的化学方程式
),写出反应的化学方程式II.工业上用Cu-ZnO作催化剂通过反应①来生产甲醇,同时也会有副反应②发生。
① CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2(3)已知298K时,相关物质的能量如图所示,则ΔH1=

(4)在恒温恒容的容器中,充入0.5mol CO2(g)和1.0mol H2(g),起始压强为p kPa,一段时间后达到平衡测得容器中生成0.3mol H2O(g),压强为
 p kPa,反应②的平衡常数Kp=
p kPa,反应②的平衡常数Kp=(5)下列说法中不正确的是_______
| A.向容器中充入He,使体系压强增大,可增大反应速率 |
| B.向容器中再充入H2可提高CO2转化率 |
C.当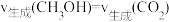 时,说明反应达到了平衡状态 时,说明反应达到了平衡状态 |
| D.选择合适的催化剂,不但可以加快反应速率,还可提高甲醇的平衡产率 |
III.催化加氢合成乙烯是CO2综合利用研究的热点领域,其反应为:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)(6)理论计算表明,原料初始组成
 ,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
您最近一年使用:0次
名校
5 . 丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料,其合成路线如下:
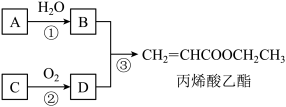
已知:A是石油化工的重要基本原料,还可用于催熟水果;A、C互为同系物,相对分子质量差14。
(1)A的名称为___________ 。
(2)D中含氧官能团名称为___________ 。
(3)写出下列反应的化学方程式及反应类型:
反应①___________ ,反应类型为___________ ;
反应③___________ ,反应类型为___________ 。
(4)下列说法正确的是___________(填字母)。
(5)久置的丙烯酸乙酯自身会发生加聚反应,所得聚合物具有较好的弹性,可用于生产织物和作皮革处理剂,聚丙烯酸乙酯的结构简式为___________ 。

已知:A是石油化工的重要基本原料,还可用于催熟水果;A、C互为同系物,相对分子质量差14。
(1)A的名称为
(2)D中含氧官能团名称为
(3)写出下列反应的化学方程式及反应类型:
反应①
反应③
(4)下列说法正确的是___________(填字母)。
| A.物质A中有6个原子共平面 |
| B.物质A的加聚产物能使溴的四氯化碳溶液褪色 |
| C.物质B可用作燃料,其属于可再生资源 |
| D.C在一定条件下能与HCl发生加成反应,只能得到一种产物 |
您最近一年使用:0次
2023-07-06更新
|
216次组卷
|
2卷引用:广东省梅州市2022-2023学年高一下学期7月期末考试化学试题
6 . 化学创造美好生活。下列生产活动中,涉及的化学知识错误的是
| 选项 | 生产活动 | 化学原理 |
| A | 用热的纯碱溶液清洗油污 |  溶液呈碱性,加热促进油脂水解 溶液呈碱性,加热促进油脂水解 |
| B | 乙烯水化法制工业酒精 | 乙烯可发生加成反应 |
| C | 用丙烯合成聚丙烯制作一次性医用口罩 | 丙烯可发生加聚反应生成聚丙烯 |
| D | 用糯米酿米酒 | 淀粉水解直接生成乙醇 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 丙烯酸乙酯是一种食用香料,用乙烯、丙烯等石油化工产品为原料合成丙烯酸乙酯的路线如图所示。回答下列问题:

(1)CH2=CH2是重要的化工原料,CH2=CH2中C原子的杂化方式为_______ ,CH2=CH2能使溴的四氯化碳溶液褪色,该反应的化学方程式为_______ 。
(2)按照官能团分类,有机物B所属的类别是_______ 。
(3)CH2=CH2→A的反应类型为_______ 。
(4)有机物B中σ键与π键的个数比为_______ ,其所含元素的电负性从大到小的顺序是_______ 。
(5)丙烯酸乙酯一定条件下会发生加成聚合反应,该聚合反应的化学方程式为_______ 。

(1)CH2=CH2是重要的化工原料,CH2=CH2中C原子的杂化方式为
(2)按照官能团分类,有机物B所属的类别是
(3)CH2=CH2→A的反应类型为
(4)有机物B中σ键与π键的个数比为
(5)丙烯酸乙酯一定条件下会发生加成聚合反应,该聚合反应的化学方程式为
您最近一年使用:0次
8 . A、B、C、D、E五种原子序数逐渐增大的短周期元素,A是周期表中原子半径最小的元素,其中B、C同周期,A与D、B与E同主族,E原子核内质子数等于B、C原子电子数之和,E的单质是应用最为广泛的半导体材料。试回答:
(1)E元素在元素周期表位置为_______ 。
(2)A与C形成的两种常见的化合物,这两种化合物含有的电子数为_______ 和_______ ,C与D形成的原子个数比为 的化合物乙的电子式是
的化合物乙的电子式是_______ ,B与E对应的最简单氢化物稳定性更强的是_______ (填化学式)。
(3)A和B形成的化合物甲,甲是一种重要的基本化原料,能够作为水果催熟剂,写出甲与 反应的化学方程式为
反应的化学方程式为_______ 。
(4)A和B形成的化合物乙,乙的分子式为 ,乙能够制得高聚物丙,该反应类型是
,乙能够制得高聚物丙,该反应类型是_______ ,高聚物丙的链节是_______ 。
(5)工业上利用E的氧化物与过量B的单质高温条件下反应制备新型陶瓷材料EB,同时生成B的氧化物,写出制备新型陶瓷材料EB的化学方程式_______ 。
(1)E元素在元素周期表位置为
(2)A与C形成的两种常见的化合物,这两种化合物含有的电子数为
 的化合物乙的电子式是
的化合物乙的电子式是(3)A和B形成的化合物甲,甲是一种重要的基本化原料,能够作为水果催熟剂,写出甲与
 反应的化学方程式为
反应的化学方程式为(4)A和B形成的化合物乙,乙的分子式为
 ,乙能够制得高聚物丙,该反应类型是
,乙能够制得高聚物丙,该反应类型是(5)工业上利用E的氧化物与过量B的单质高温条件下反应制备新型陶瓷材料EB,同时生成B的氧化物,写出制备新型陶瓷材料EB的化学方程式
您最近一年使用:0次
9 . 体育运动体现了科技水平的发展,下列与体育相关的化学知识,说法正确的是
| A.体育赛场上常用于给受伤处快速降温止痛的氯乙烷属于烃类物质 |
| B.“水立方”的外墙采用乙烯-四氟乙烯共聚物膜材,该膜材含有碳碳双键 |
| C.游泳池的水中加入少量硫酸铜能起到达到杀菌消毒的作用 |
| D.“鸟巢”体育场使用了大量高强度合金钢,该合金钢的熔点高于铁单质 |
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题:
I.煤的综合利用,是推进能源革命的重要方向。
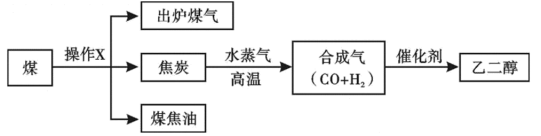
请回答下列问题:
(1)煤经过操作X可获得出炉煤气、焦炭、煤焦油等产品,操作X的名称是_______ 。
(2)出炉煤气中含有丙烯( ),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是
),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是_______ 。
(3)焦炭与水蒸气反应生成合成气,进而可制备乙二醇( ),乙二醇与乙醇
),乙二醇与乙醇_______ (填“是”或“不是”)同系物。
II.乙酸环己酯是一种香料,可用于配制苹果、香蕉等果香型香精。一种制备乙酸环己酯的合成路线如下:

回答下列问题:
(4)由石油获得E的生产工艺称为_______ 。
(5)G中官能团名称是_______ ,在反应①~④中,原子利用率理论上可达100%的是_______ (填序号)。
(6)X是E的同系物,其相对分子质量比E大42,X可能的结构有_______ 种,其中含3个 的X结构简式为
的X结构简式为_______ 。
I.煤的综合利用,是推进能源革命的重要方向。

请回答下列问题:
(1)煤经过操作X可获得出炉煤气、焦炭、煤焦油等产品,操作X的名称是
(2)出炉煤气中含有丙烯(
 ),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是
),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是(3)焦炭与水蒸气反应生成合成气,进而可制备乙二醇(
 ),乙二醇与乙醇
),乙二醇与乙醇II.乙酸环己酯是一种香料,可用于配制苹果、香蕉等果香型香精。一种制备乙酸环己酯的合成路线如下:

回答下列问题:
(4)由石油获得E的生产工艺称为
(5)G中官能团名称是
(6)X是E的同系物,其相对分子质量比E大42,X可能的结构有
 的X结构简式为
的X结构简式为
您最近一年使用:0次



