1 . 实验室常用如图所示装置制取乙炔,并验证乙炔的性质。已知:实验室制备乙炔的化学方程式为CaC2+2H2O→Ca(OH)2+HC≡CH↑,且制备的乙炔气体中常混有H2S气体。回答下列问题:
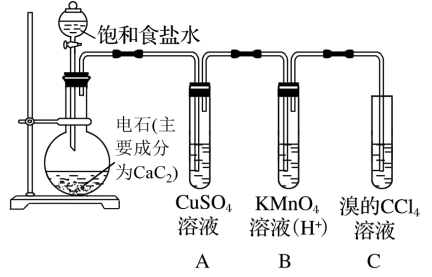
(1)装置A的作用是___________ ,装置B中的现象是___________ 。
(2)如果要进行乙炔的可燃性实验,首先应该___________ 。
(3)若乙炔加氢后得到乙烷,则乙烷在光照条件下与氯气反应,生成的一氯代烷最多有___________ 种。
(4)若称取ag电石,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中,溶液增重bg,则电石的纯度为___________ 。

(1)装置A的作用是
(2)如果要进行乙炔的可燃性实验,首先应该
(3)若乙炔加氢后得到乙烷,则乙烷在光照条件下与氯气反应,生成的一氯代烷最多有
(4)若称取ag电石,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中,溶液增重bg,则电石的纯度为
您最近一年使用:0次
名校
解题方法
2 . 四溴化乙炔(CHBr2-CHBr2)是一种无色液体,常用于合成季铵化合物。某同学在实验室模仿工业生产,以电石(主要成分CaC2,少量CaS,Ca3P2,Ca3As2等)和Br2等为原料制备少量四溴化乙炔,实验装置(夹持装置已省略)如图所示。已知:四溴化乙炔的熔点为1℃,沸点为244℃,密度为2.967g·cm-3,难溶于水。回答下列问题:
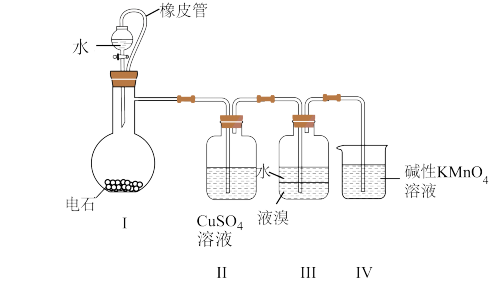
(1)装置Ⅰ中CaC2与水反应生成乙炔(C2H2)和氢氧化钙,写出该反应的化学方程式:___________ ;该反应剧烈,为了得到平缓的C2H2气流,可采取的措施是___________
(2)装置Ⅱ的目的是___________
(3)装置Ⅳ的目的是除去未反应的乙炔。在碱性条件下,KMnO4与C2H2反应生成碳酸盐和MnO2,则该反应中参与反应的氧化剂和还原剂的物质的量之比为___________ 。
(4)橡皮管的作用:___________

(1)装置Ⅰ中CaC2与水反应生成乙炔(C2H2)和氢氧化钙,写出该反应的化学方程式:
(2)装置Ⅱ的目的是
(3)装置Ⅳ的目的是除去未反应的乙炔。在碱性条件下,KMnO4与C2H2反应生成碳酸盐和MnO2,则该反应中参与反应的氧化剂和还原剂的物质的量之比为
(4)橡皮管的作用:
您最近一年使用:0次
2014·上海浦东新·二模
解题方法
3 . (1)实验室利用如图所示装置,用电石为原料,在90℃左右,用HgSO4催化乙炔水化制备乙醛。(已知常温下乙炔在水中溶解度约为1:1(体积比))
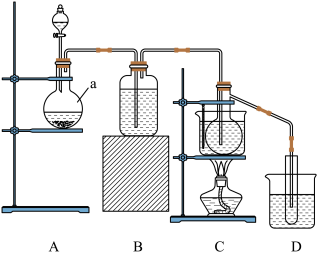
①仪器a的名称是___ ;a底是否需要加设酒精灯?___ (是、否)
②装置B中盛放一种蓝色溶液,该溶液的作用是___ 。
③装置C中所用温度计测量的是___ 的温度。
④D烧杯中使用冰水,主要用于对___ 的冷凝。此外,D试管中收集到的物质主要还有水和__ 。
(2)惰性气体的主要来源是空气,其中含量最高的惰性气体是氩。已知氩的沸点介于氮气和氧气之间(三种气体的沸点从-196到-183℃不等)。以下是从液化空气中获取氩的主要操作流程。
液化空气 剩余液体
剩余液体 蒸馏所得气体
蒸馏所得气体
 含微量杂质的氩气
含微量杂质的氩气
①第一步低温蒸馏过程中除去的物质主要是__ 。
②NaOH溶液、灼热的铜丝、灼热的镁屑依次用于除去气体中少量的___ 、___ 和__ 。

①仪器a的名称是
②装置B中盛放一种蓝色溶液,该溶液的作用是
③装置C中所用温度计测量的是
④D烧杯中使用冰水,主要用于对
(2)惰性气体的主要来源是空气,其中含量最高的惰性气体是氩。已知氩的沸点介于氮气和氧气之间(三种气体的沸点从-196到-183℃不等)。以下是从液化空气中获取氩的主要操作流程。
液化空气
 剩余液体
剩余液体 蒸馏所得气体
蒸馏所得气体
 含微量杂质的氩气
含微量杂质的氩气①第一步低温蒸馏过程中除去的物质主要是
②NaOH溶液、灼热的铜丝、灼热的镁屑依次用于除去气体中少量的
您最近一年使用:0次
4 . 实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH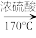 CH2=CH2+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:

有关数据列表如下:
回答下列问题:
(1)在装置c中应加入________ (选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)装置b的作用是___________ 。
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________ (填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________ (填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),但不用冰水进行过度冷却,原因是___________________________ 。
(6)以1,2二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2二溴乙烷通过反应①制得A,A通过反应②制得氯乙烯,由氯乙烯制得聚氯乙烯。
①________________ (填反应类型) ②________________ (填反应类型)
A________________ (填该物质的电子式)
写出第一步反应①的化学方程式_______________________________ 。
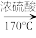 CH2=CH2+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在装置c中应加入
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)装置b的作用是
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的
(4)若产物中有少量未反应的Br2,最好用
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),但不用冰水进行过度冷却,原因是
(6)以1,2二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2二溴乙烷通过反应①制得A,A通过反应②制得氯乙烯,由氯乙烯制得聚氯乙烯。
①
A
写出第一步反应①的化学方程式
您最近一年使用:0次



