名校
1 . 乙炔是重要的化工原料。我校化学研究性学习小组同学进行了如下探究。
I.甲组同学利用电石中的CaC2与H2O反应制C2H2,并通过排水测量出反应产生的气体的体积,从而测定电石中CaC2的含量。
(1)实验装置如图所示,仪器b的名称为___________ ;该反应制取C2H2气体的原理是___________ ;(用化学方程式表示)

(2)研究性学习小组进行实验时,有下列操作(每项操作只进行一次):
①仪器a中注入饱和食盐水,c中注入适量水。
②称取一定量电石,置于仪器b中,塞紧橡皮塞
③检查装置的气密性。
④待仪器b恢复到室温时,量取仪器d中水的体积(导管中水忽略不计)。
⑤慢慢开启仪器a的活塞,使饱和食盐水逐滴滴下至不产生气体为止,关闭活塞。
正确的操作顺序是___________ 。(填写操作编号)
(3)若实验时称取电石的质量为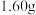 ,测量出排水的体积后,折算成标准状况下C2H2的体积为
,测量出排水的体积后,折算成标准状况下C2H2的体积为 ,则此电石中CaC2的质量分数为
,则此电石中CaC2的质量分数为___________ 。(假设其它物质不反应)
Ⅱ.为探究乙炔与溴的加成反应,乙组同学设计并进行了如下实验:
①先取一定量的工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。
②丙组同学发现在乙组同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能有少量含硫的还原性杂质气体(有臭鸡蛋气味)。由此他提出必须先除去杂质,再与溴水反应。请回答下列问题:
(4)乙组同学设计的实验___________ (填“能”或“不能”)验证乙炔与溴发生加成反应,其理由是___________ 。
A.使溴水褪色的物质,就是乙炔
B.使溴水褪色的物质,未必是乙炔
C.使溴水褪色的反应,就是加成反应
D.使溴水褪色的反应,未必是加成反应
(5)丙组同学推测此乙炔中必定含有的一种杂质气体,该气体与溴水反应的化学方程式是___________ ,在验证过程中必须全部除去。
(6)请你选用下列四个装置(见下图,可重复使用)来实现丙组同学的实验方案,将装置的编号填入方框___________ ,并写出装置内所放的化学药品___________ 。
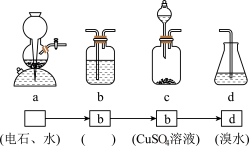
(7)为验证这一反应是加成而不是取代,丙同学提出可用 试纸来测试反应后溶液的酸性。理由是
试纸来测试反应后溶液的酸性。理由是___________ 。
I.甲组同学利用电石中的CaC2与H2O反应制C2H2,并通过排水测量出反应产生的气体的体积,从而测定电石中CaC2的含量。
(1)实验装置如图所示,仪器b的名称为

(2)研究性学习小组进行实验时,有下列操作(每项操作只进行一次):
①仪器a中注入饱和食盐水,c中注入适量水。
②称取一定量电石,置于仪器b中,塞紧橡皮塞
③检查装置的气密性。
④待仪器b恢复到室温时,量取仪器d中水的体积(导管中水忽略不计)。
⑤慢慢开启仪器a的活塞,使饱和食盐水逐滴滴下至不产生气体为止,关闭活塞。
正确的操作顺序是
(3)若实验时称取电石的质量为
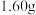 ,测量出排水的体积后,折算成标准状况下C2H2的体积为
,测量出排水的体积后,折算成标准状况下C2H2的体积为 ,则此电石中CaC2的质量分数为
,则此电石中CaC2的质量分数为Ⅱ.为探究乙炔与溴的加成反应,乙组同学设计并进行了如下实验:
①先取一定量的工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。
②丙组同学发现在乙组同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能有少量含硫的还原性杂质气体(有臭鸡蛋气味)。由此他提出必须先除去杂质,再与溴水反应。请回答下列问题:
(4)乙组同学设计的实验
A.使溴水褪色的物质,就是乙炔
B.使溴水褪色的物质,未必是乙炔
C.使溴水褪色的反应,就是加成反应
D.使溴水褪色的反应,未必是加成反应
(5)丙组同学推测此乙炔中必定含有的一种杂质气体,该气体与溴水反应的化学方程式是
(6)请你选用下列四个装置(见下图,可重复使用)来实现丙组同学的实验方案,将装置的编号填入方框

(7)为验证这一反应是加成而不是取代,丙同学提出可用
 试纸来测试反应后溶液的酸性。理由是
试纸来测试反应后溶液的酸性。理由是
您最近一年使用:0次
名校
2 . 按要求填空
(1)下列几组物质中,互为同系物的是___________ ,互为同分异构体的是___________
① 氯气和液氯 ② D 和 T ③ CH3CH3和(CH3)2CHCH3 ④12CO 和14CO
⑤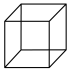 和
和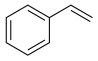 ⑥ CH2=CHCH2CH3和
⑥ CH2=CHCH2CH3和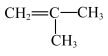
(2)乙炔与水发生反应,其化学方程式为___________ , 该反应的类型是___________ 。
(3)某有机物的键线式为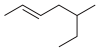 ,按照系统命名法,其名称是
,按照系统命名法,其名称是___________
(4)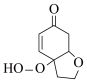 用*标出其中的手性碳
用*标出其中的手性碳___________
(5)分子式为C10H14的芳香烃,仅含一个侧链且能使酸性高锰酸钾褪色的所有可能结构____________
(6)该结构中所有含氧官能团的名称为___________
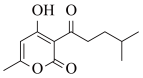
(7)由环己烷、乙醇、乙醚(CH3CH2OCH2CH3)组成的混和物,经测定其中碳的质量分数为72%,则氧的质量分数约为___________
(8)与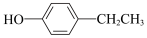 互为同分异构体的,含有苯环的有
互为同分异构体的,含有苯环的有___________ 种((不含C-O-C结构,不考虑立体异构)
(1)下列几组物质中,互为同系物的是
① 氯气和液氯 ② D 和 T ③ CH3CH3和(CH3)2CHCH3 ④12CO 和14CO
⑤
 和
和 ⑥ CH2=CHCH2CH3和
⑥ CH2=CHCH2CH3和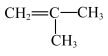
(2)乙炔与水发生反应,其化学方程式为
(3)某有机物的键线式为
 ,按照系统命名法,其名称是
,按照系统命名法,其名称是(4)
 用*标出其中的手性碳
用*标出其中的手性碳(5)分子式为C10H14的芳香烃,仅含一个侧链且能使酸性高锰酸钾褪色的所有可能结构
(6)该结构中所有含氧官能团的名称为

(7)由环己烷、乙醇、乙醚(CH3CH2OCH2CH3)组成的混和物,经测定其中碳的质量分数为72%,则氧的质量分数约为
(8)与
 互为同分异构体的,含有苯环的有
互为同分异构体的,含有苯环的有
您最近一年使用:0次
名校
解题方法
3 . 丙烯腈(CH2=CHCN)是合成纤维、合成橡胶和合成树脂的重要单体,可以由乙炔与HCN反应制得。原理如下CH≡CH+HCN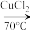 CH2=CHCN
CH2=CHCN
Ⅰ.制备催化剂CuCl2
(1)通过查阅资料有两种方案可以制备
方案1:铜屑与H2O2在浓盐酸中反应
方案2:铜丝在氯气中燃烧
方案1的实验原理如图所示_____
②请写出方案1的反应原理___________ (用离子方程式表达)
(2)用恒压滴液漏斗分批多次滴加H2O2,且H2O2过量,原因是_____
(3)方案2燃烧后的固体溶于水,过滤后发现一些白色固体X,为检测X的成分,某同学将其溶于稀硫酸,白色固体变为红色,且溶液呈蓝色,推测X为_____
Ⅱ.合成丙烯腈
已知:①电石的主要成分是CaC2,还含有少量硫化钙
②HCN易挥发,有毒,具有较强的还原性_____
(5)纯净的乙炔是无色、无臭的气体。但用电石制取的乙炔时常伴有有臭鸡蛋气味,这种物质是_____
(6)从下列选择装置D中可盛放的溶液
(7)工业用200 kg 含CaC2质量分数80%的电石,生产得到丙烯腈79.5 kg,计算产率_____
 CH2=CHCN
CH2=CHCNⅠ.制备催化剂CuCl2
(1)通过查阅资料有两种方案可以制备
方案1:铜屑与H2O2在浓盐酸中反应
方案2:铜丝在氯气中燃烧
方案1的实验原理如图所示
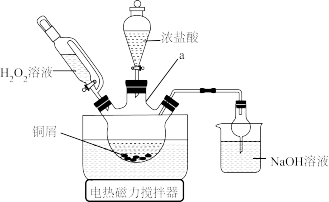
②请写出方案1的反应原理
(2)用恒压滴液漏斗分批多次滴加H2O2,且H2O2过量,原因是
(3)方案2燃烧后的固体溶于水,过滤后发现一些白色固体X,为检测X的成分,某同学将其溶于稀硫酸,白色固体变为红色,且溶液呈蓝色,推测X为
Ⅱ.合成丙烯腈
已知:①电石的主要成分是CaC2,还含有少量硫化钙
②HCN易挥发,有毒,具有较强的还原性
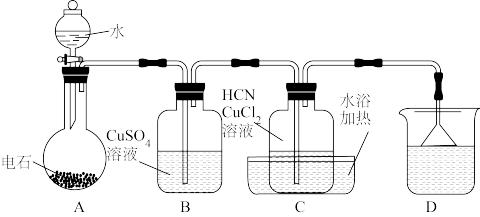
(5)纯净的乙炔是无色、无臭的气体。但用电石制取的乙炔时常伴有有臭鸡蛋气味,这种物质是
(6)从下列选择装置D中可盛放的溶液
| A.高锰酸钾溶液 | B.NaOH溶液 | C.饱和食盐水 | D.盐酸溶液 |
您最近一年使用:0次
2022-04-13更新
|
2082次组卷
|
8卷引用:贵州省遵义市2022届高三模拟卷(二)理综化学试题
贵州省遵义市2022届高三模拟卷(二)理综化学试题(已下线)【直抵名校】04-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)江苏省南京市金陵中学河西分校2022-2023学年高二上学期期末检测化学试题江西省宜春市上高二中2022-2023学年高二下学期第二次月考(期中) 化学试题
4 . 常温下,甲、乙、丙、丁四种气态烃的分子中所含电子数分别为10、14、16和18,下列关于这四种气态烃的推断正确的是
| A.四种气态烃中至少有两种互为同分异构体 |
| B.乙和丁互为同系物 |
| C.乙和丙都可以和H2发生加成反应 |
| D.丙中碳元素的质量分数约为75% |
您最近一年使用:0次
5 . 食品保鲜膜按材质分别为聚乙烯 (PE )、聚氯乙烯 (PVC )、聚偏二氯乙烯 (PVDC )等种类。 其中 PE 和 PVDC 是安全的。PVC 对人体的潜在危害主要来源于两个方面:产品中氯乙烯单体残留量、加工过程中使用的加工助剂的种类及含量。
(1)写出用乙烯、氯乙烯分别生产聚乙烯和聚氯乙烯的化学方程式:乙烯→聚乙烯 (PE ):_____ 氯乙烯→聚氯乙烯 (PVC ):_____ 日常用的食品保鲜膜宜选用_____ 。
(2)目前出现的“不粘锅”、不粘油的吸油烟机等新型厨具,其秘密就是表面有一种叫做“特富龙”的涂层,实际上就是被称为“塑料王”的聚四氟乙烯。它的单体四氟乙烯的结构简式是_____ ,合成特富龙的反应类型是_____ ,反应方程式为_____ 。
(3)聚四氟乙烯的发现源于一次实验意外。1938 年,化学家普鲁凯特与助手们研究四氟乙烯的聚合反应,他们将四氟乙烯贮存在冷藏箱中的加压钢瓶中,当将钢瓶与反应器管道、反应器 (管道 及反应器间隙有空气 )接通后,发生故障,四氟乙烯气体并没有通到反应器中,经称重证明钢瓶中气体一点没减少,打开阀门也没有四氟乙烯气体逸出,但拆卸阀门后却从钢瓶倒出与四氟乙烯等重的白色粉末,即四氟乙烯已在钢瓶中发生了聚合反应。后经确证,该白色粉末就是聚四氟乙烯。1945 年,美国杜邦公司开始在工业规模上生产聚四氟乙烯,由此可以推知该反应的条件是_____ 、_____ 、_____ 引发。
(4 )不粘锅的内壁有一薄层聚四氟乙烯涂层,因此用不粘锅烧饭菜时不易粘锅,下列说法正确的是_____
a.聚四氟乙烯分子中没有双键
b.聚四氟乙烯的单体是不饱和烃
c.聚四氟乙烯的化学性质很不活泼
d.聚四氟乙烯的熔沸点很低
乙炔是一种重要的基本有机原料,在一定条件下其衍变关系如图:
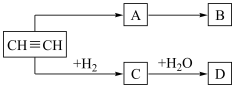
已知:B 是一种塑料,75%的 D 溶液在医药上用作消毒剂。试回答下列问题:
(5)比乙炔多一个碳原子的同系物的结构简式是_____ 。
(6)A 物质的结构简式是_____ ,A→B 反应类型是_____ 反应。
(7)出以下各步反应的化学方程式:乙炔→A:_____ 乙炔→C:_____ C→D:_____
(1)写出用乙烯、氯乙烯分别生产聚乙烯和聚氯乙烯的化学方程式:乙烯→聚乙烯 (PE ):
(2)目前出现的“不粘锅”、不粘油的吸油烟机等新型厨具,其秘密就是表面有一种叫做“特富龙”的涂层,实际上就是被称为“塑料王”的聚四氟乙烯。它的单体四氟乙烯的结构简式是
(3)聚四氟乙烯的发现源于一次实验意外。1938 年,化学家普鲁凯特与助手们研究四氟乙烯的聚合反应,他们将四氟乙烯贮存在冷藏箱中的加压钢瓶中,当将钢瓶与反应器管道、反应器 (管道 及反应器间隙有空气 )接通后,发生故障,四氟乙烯气体并没有通到反应器中,经称重证明钢瓶中气体一点没减少,打开阀门也没有四氟乙烯气体逸出,但拆卸阀门后却从钢瓶倒出与四氟乙烯等重的白色粉末,即四氟乙烯已在钢瓶中发生了聚合反应。后经确证,该白色粉末就是聚四氟乙烯。1945 年,美国杜邦公司开始在工业规模上生产聚四氟乙烯,由此可以推知该反应的条件是
(4 )不粘锅的内壁有一薄层聚四氟乙烯涂层,因此用不粘锅烧饭菜时不易粘锅,下列说法正确的是
a.聚四氟乙烯分子中没有双键
b.聚四氟乙烯的单体是不饱和烃
c.聚四氟乙烯的化学性质很不活泼
d.聚四氟乙烯的熔沸点很低
乙炔是一种重要的基本有机原料,在一定条件下其衍变关系如图:

已知:B 是一种塑料,75%的 D 溶液在医药上用作消毒剂。试回答下列问题:
(5)比乙炔多一个碳原子的同系物的结构简式是
(6)A 物质的结构简式是
(7)出以下各步反应的化学方程式:乙炔→A:
您最近一年使用:0次
2014·上海浦东新·二模
解题方法
6 . (1)实验室利用如图所示装置,用电石为原料,在90℃左右,用HgSO4催化乙炔水化制备乙醛。(已知常温下乙炔在水中溶解度约为1:1(体积比))
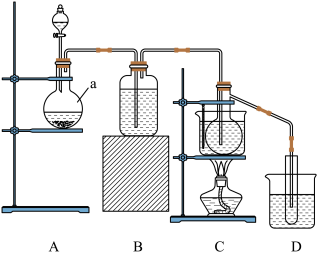
①仪器a的名称是___ ;a底是否需要加设酒精灯?___ (是、否)
②装置B中盛放一种蓝色溶液,该溶液的作用是___ 。
③装置C中所用温度计测量的是___ 的温度。
④D烧杯中使用冰水,主要用于对___ 的冷凝。此外,D试管中收集到的物质主要还有水和__ 。
(2)惰性气体的主要来源是空气,其中含量最高的惰性气体是氩。已知氩的沸点介于氮气和氧气之间(三种气体的沸点从-196到-183℃不等)。以下是从液化空气中获取氩的主要操作流程。
液化空气 剩余液体
剩余液体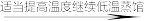 蒸馏所得气体
蒸馏所得气体
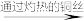
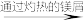 含微量杂质的氩气
含微量杂质的氩气
①第一步低温蒸馏过程中除去的物质主要是__ 。
②NaOH溶液、灼热的铜丝、灼热的镁屑依次用于除去气体中少量的___ 、___ 和__ 。

①仪器a的名称是
②装置B中盛放一种蓝色溶液,该溶液的作用是
③装置C中所用温度计测量的是
④D烧杯中使用冰水,主要用于对
(2)惰性气体的主要来源是空气,其中含量最高的惰性气体是氩。已知氩的沸点介于氮气和氧气之间(三种气体的沸点从-196到-183℃不等)。以下是从液化空气中获取氩的主要操作流程。
液化空气
 剩余液体
剩余液体 蒸馏所得气体
蒸馏所得气体
 含微量杂质的氩气
含微量杂质的氩气①第一步低温蒸馏过程中除去的物质主要是
②NaOH溶液、灼热的铜丝、灼热的镁屑依次用于除去气体中少量的
您最近一年使用:0次



