1 . 实验室制溴苯可用如图装置。回答下列问题:
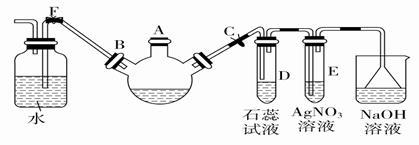
(1)关闭F夹,打开C夹,向装有少量苯的三口烧瓶的A口加少量溴,再加少量铁屑,塞住A口,则三口烧瓶中发生的有机化学反应方程式为_______________________ 。
(2)D试管内出现的现象为________________ ;E试管内出现的现象为________________ 。
(3)待三口烧瓶中仍有气泡冒出时打开F夹,关闭C夹,可看到的现象是_____________________ 。
(4)从溴苯中除去溴,用NaOH溶液处理后再洗涤,反应的离子方程式为_________________ 。

(1)关闭F夹,打开C夹,向装有少量苯的三口烧瓶的A口加少量溴,再加少量铁屑,塞住A口,则三口烧瓶中发生的有机化学反应方程式为
(2)D试管内出现的现象为
(3)待三口烧瓶中仍有气泡冒出时打开F夹,关闭C夹,可看到的现象是
(4)从溴苯中除去溴,用NaOH溶液处理后再洗涤,反应的离子方程式为
您最近一年使用:0次
2016-12-09更新
|
458次组卷
|
3卷引用:2016-2017学年吉林省毓文中学高二上期中化学卷
2016-2017学年吉林省毓文中学高二上期中化学卷河北省张家口市尚义县第一中学2019-2020学年高二下学期期中考试化学试题(已下线)第二章 烃 章末测试(A)-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)
2 . 下列说法正确的是( )
| A.实验室制硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | B.制取溴苯:将铁屑、溴水、苯混合加热 |
| C.证明氯乙烷中含有氯原子,可将氯乙烷溶于 AgNO3 的溶液中 | D.实验室制得的粗溴苯通常呈黄色,是因为溶解了少量的 Br2 |
您最近一年使用:0次
3 . 某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
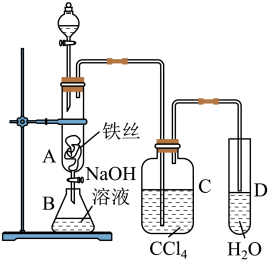
回答下列问题:
(1)写出A中发生主要反应的化学方程式___________________
(2)C中盛放CCl4的作用是_____________ 。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是__________
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,根据产生淡黄色沉淀,则能证明。你还能想出一种其他验证的方法吗?指出加入的试剂和出现的现象即可。
加入的试剂为________________
对应的现象为__________________ 。

回答下列问题:
(1)写出A中发生主要反应的化学方程式
(2)C中盛放CCl4的作用是
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,根据产生淡黄色沉淀,则能证明。你还能想出一种其他验证的方法吗?指出加入的试剂和出现的现象即可。
加入的试剂为
对应的现象为
您最近一年使用:0次
名校
4 . 硝基苯是重要的精细化工原料,是医药和染料的中间体,还可作有机溶剂.实验室中制备硝基苯的过程如下:
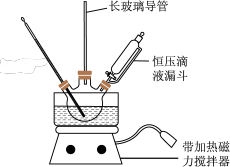
①配制混酸:组装如图反应装置.取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混合酸,加入恒压滴液漏斗中.把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀.
③加热在50~60℃下发生反应,直至反说结束.
④除去混合酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后用蒸馏水洗涤得到粗产品.
⑤为了得到更纯净的硝基苯.还需先向液棒中加入试剂A,静置一段时间后弃去试剂A,然后蒸馏,最终得到17.5g硝基苯
已知:
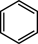 +HNO3(浓)
+HNO3(浓)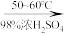
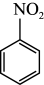 +H2O
+H2O
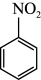 +HNO3(浓)
+HNO3(浓)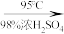
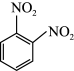 (6%)+
(6%)+  (93%)+
(93%)+ 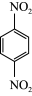 (1%)+H2O
(1%)+H2O
可能用到的有关数据列表如下:
请回答下列问题:
(1)配制混酸应先在烧杯中加入_______ .
(2)恒压滴液漏斗的优点是_______ ,实验装置中长玻璃导管可用____________ 代替(填仪器名称)
(3)要控制反应温度50~60℃,可用水浴加热,其优点为___________________________
(4)反应结束后产品在液体的_____ 层(填"上"或"下"),分离混酸和产品的操作方法为____________
(5)用10% Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?___________
(6)试剂A是________ ,蒸馏过程中需在蒸馏烧瓶中加入沸石,其作用为_______________ 若加热后,发现未加沸石,应采取的正确方法______________________________________
(7)硝基苯的产率为_________ .

①配制混酸:组装如图反应装置.取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混合酸,加入恒压滴液漏斗中.把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀.
③加热在50~60℃下发生反应,直至反说结束.
④除去混合酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后用蒸馏水洗涤得到粗产品.
⑤为了得到更纯净的硝基苯.还需先向液棒中加入试剂A,静置一段时间后弃去试剂A,然后蒸馏,最终得到17.5g硝基苯
已知:
 +HNO3(浓)
+HNO3(浓)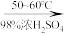
 +H2O
+H2O  +HNO3(浓)
+HNO3(浓)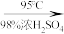
 (6%)+
(6%)+  (93%)+
(93%)+  (1%)+H2O
(1%)+H2O 可能用到的有关数据列表如下:
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/(g•cm-3) | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 1,3-二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
(1)配制混酸应先在烧杯中加入
(2)恒压滴液漏斗的优点是
(3)要控制反应温度50~60℃,可用水浴加热,其优点为
(4)反应结束后产品在液体的
(5)用10% Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?
(6)试剂A是
(7)硝基苯的产率为
您最近一年使用:0次
5 . 制备溴苯的实验装置如图所示,请回答下列问题:
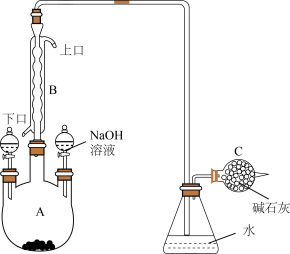
(1)该反应装置中仪器A的名称为__________ ;反应开始前已向仪器A中加入的固体药品是铁粉,而装在左侧分液漏斗中的液体药品是_______ 。
(2)冷凝管B有上、下两口,冷却水应从_____ 口进入。
(3)导管口不能插入锥形瓶中的液面之下,其原因是____________ 。
(4)右侧分液漏斗中的物质在反应_______ 时加入A中(填写反应前、反应中或者反应后),用离子方程式表达其作用是:_________________ 。
(5)反应结束向锥形瓶中的液体中加入硝酸酸化的硝酸银溶液,可见到现象是________________ 。
(6)该反应过程可以如下表述:3Br2+2Fe=2FeBr3;Br2+FeBr3=FeBr4﹣+Br+(不稳定);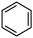 + Br+ + FeBr4﹣→
+ Br+ + FeBr4﹣→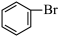 + HBr + FeBr3;由上反应可知:
+ HBr + FeBr3;由上反应可知: +Br2 →
+Br2 →  +HBr中的催化剂为
+HBr中的催化剂为_________ 。
A、Fe B、FeBr3 C、Br+ D、FeBr4﹣

(1)该反应装置中仪器A的名称为
(2)冷凝管B有上、下两口,冷却水应从
(3)导管口不能插入锥形瓶中的液面之下,其原因是
(4)右侧分液漏斗中的物质在反应
(5)反应结束向锥形瓶中的液体中加入硝酸酸化的硝酸银溶液,可见到现象是
(6)该反应过程可以如下表述:3Br2+2Fe=2FeBr3;Br2+FeBr3=FeBr4﹣+Br+(不稳定);
 + Br+ + FeBr4﹣→
+ Br+ + FeBr4﹣→ + HBr + FeBr3;由上反应可知:
+ HBr + FeBr3;由上反应可知: +Br2 →
+Br2 →  +HBr中的催化剂为
+HBr中的催化剂为A、Fe B、FeBr3 C、Br+ D、FeBr4﹣
您最近一年使用:0次
13-14高一下·吉林·期末
解题方法
6 . 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
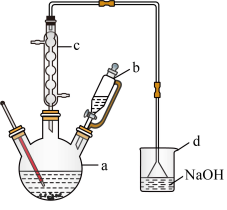
按下列合成步骤回答问题:
(1)写出a中生成溴苯的化学方程式______________________________________ ;
(2)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了__________ 气体,继续滴加至液溴滴完。装置d装置的作用是______________ 。
(3)液溴滴完后,经过下列步骤分离提纯: ①向a中加入10 mL水,然后过滤除去未反应的铁屑; ②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_________ ;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________ 。
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为_________ ;要进一步提纯,下列操作中必须的是______ (填入正确选项前的字母)。
A. 重结晶 B. 过滤 C. 萃取 D. 蒸馏

按下列合成步骤回答问题:
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm—3 | 0.88 | 3.10 | 1.50 |
| 沸点℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(2)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了
(3)液溴滴完后,经过下列步骤分离提纯: ①向a中加入10 mL水,然后过滤除去未反应的铁屑; ②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为
A. 重结晶 B. 过滤 C. 萃取 D. 蒸馏
您最近一年使用:0次
2016-12-09更新
|
884次组卷
|
3卷引用:2013-2014吉林市普通中学高一化学下学期期末教学质量检测试卷
(已下线)2013-2014吉林市普通中学高一化学下学期期末教学质量检测试卷辽宁省实验中学分校2017-2018学年高二上学期期中考试化学试题内蒙古通辽市科尔沁左翼中旗实验高级中学2021-2022学年高二下学期期中考试(A卷)化学试题
名校
7 . 某化学课外小组查阅资料知:验证溴化氢的生成可以证明苯和液溴在溴化铁催化作用下发生的不是加成反应,而是取代反应。因此他们设计了如图装置制取溴苯,并验证溴化氢的生成。试回答:
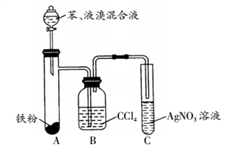
(1)装置A中发生反应的化学反应方程式是:__________________ 。
(2)装置C中看到哪两种现象___________ 、____________ ,证明有溴化氢生成。
(3)装置B的作用是________________________________ 。
(4)实验完毕后,如何分离苯和溴苯的混合物( ) 。
A.过滤 B.蒸馏 C.萃取 D.分液

(1)装置A中发生反应的化学反应方程式是:
(2)装置C中看到哪两种现象
(3)装置B的作用是
(4)实验完毕后,如何分离苯和溴苯的混合物
A.过滤 B.蒸馏 C.萃取 D.分液
您最近一年使用:0次
解题方法
8 . 欲除去下列物质中混有的少量杂质(括号内物质为杂质),错误的是
| A.苯(苯酚):氢氧化钠溶液,充分振荡静置后,分液 |
| B.乙醇(水):加入新制生石灰,蒸馏 |
| C.溴苯(溴):加入氢氧化钠溶液,充分振荡静置后,分液 |
| D.乙酸(乙醇):加入金属钠,蒸馏 |
您最近一年使用:0次
2017-04-21更新
|
254次组卷
|
2卷引用:吉林省洮南市第一中学2020-2021学年高二下学期期中考试化学试题
9 . 下列叙述错误的是
| A.乙烯和苯使溴水褪色的原因不同 |
| B.苯和氢气在一定条件下生成环己烷的反应为还原反应 |
| C.硝基苯和乙酸乙酯的制备都发生了取代反应 |
| D.由乙醇制取乙烯发生了氧化反应 |
您最近一年使用:0次
10 . 实验室用下面(右图)装置制取少量溴苯,试填写下列空白。
(1)在烧瓶a中反应的化学方程式是________________________________________________ 。
(2)长直导管b的作用:一是_______________________ ,二是________________________ 。
(3)分析导管c的下口能不能浸没于液面中?为什么?____________
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液有淡黄色沉淀生成,
此现象说明这种获得溴苯的反应属于____________ (填有机反应类型)。
(5)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色不溶于水的液体生成,这可能是因为_______ 的缘故。获得纯净的溴苯所用的主要试剂是_______ 。纯溴苯为________ 色液体,它的密度比水_____ (轻或重)。将溴苯和苯的混合物分离的操作是___________ 。
(6)采用(左图)装置进行实验,比较两个实验,请指出(左图)的两个优点
_________________________________ 、_____________________________________ 。

(1)在烧瓶a中反应的化学方程式是
(2)长直导管b的作用:一是
(3)分析导管c的下口能不能浸没于液面中?为什么?
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液有淡黄色沉淀生成,
此现象说明这种获得溴苯的反应属于
(5)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色不溶于水的液体生成,这可能是因为
(6)采用(左图)装置进行实验,比较两个实验,请指出(左图)的两个优点

您最近一年使用:0次



