名校
1 . 我国科学家成功合成抗新冠肺炎新药Ebselen。一种合成Ebselen的流程如下(已知:氨基 具有强还原性):
具有强还原性):
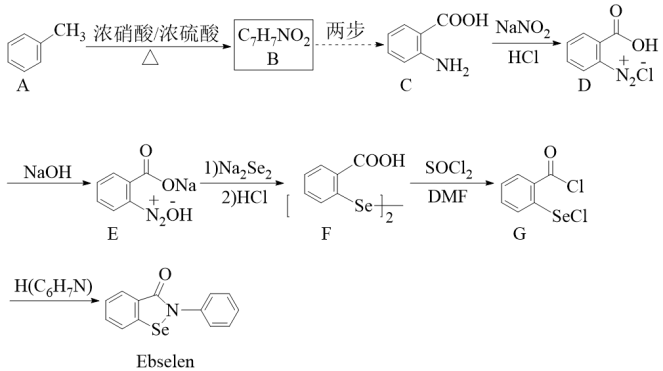
请回答下列问题:
(1)D是一种重氮盐,易分解生成N2和 ,含氯有机产物的化学名称是
,含氯有机产物的化学名称是_______ 。H的结构简式为_______ 。
(2)一定条件下,E能与苯酚、NaOH反应生成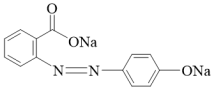 。写出该反应的化学方程式:
。写出该反应的化学方程式:_______ 。其有机反应类型是_______ 。
(3)生成G时,F中所断裂化学键是_______(填标号)。
(4)已知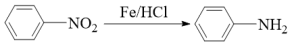 (具有强还原性),B、C之间两步反应的顺序设计中,要考虑
(具有强还原性),B、C之间两步反应的顺序设计中,要考虑_______ 。
(5)在C的芳香族同分异构体中,同时具备下列条件的结构有_______ 种。
①能发生银镜反应;②苯环上含氨基
(6)以邻二甲苯和对氨基苯甲酸为主要原料制备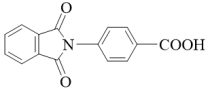 的微流程如下:
的微流程如下: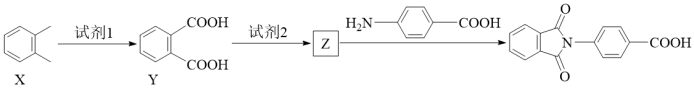
试剂2是_______ (填化学式)。
 具有强还原性):
具有强还原性):
请回答下列问题:
(1)D是一种重氮盐,易分解生成N2和
 ,含氯有机产物的化学名称是
,含氯有机产物的化学名称是(2)一定条件下,E能与苯酚、NaOH反应生成
 。写出该反应的化学方程式:
。写出该反应的化学方程式:(3)生成G时,F中所断裂化学键是_______(填标号)。
A.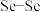 | B.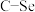 | C. | D.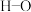 |
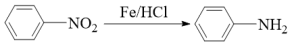 (具有强还原性),B、C之间两步反应的顺序设计中,要考虑
(具有强还原性),B、C之间两步反应的顺序设计中,要考虑(5)在C的芳香族同分异构体中,同时具备下列条件的结构有
①能发生银镜反应;②苯环上含氨基
(6)以邻二甲苯和对氨基苯甲酸为主要原料制备
 的微流程如下:
的微流程如下:
试剂2是
您最近一年使用:0次
2 . 某药物K的合成路线如图:

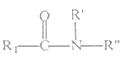
已知:①R1CH2COOR2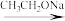
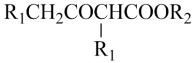
②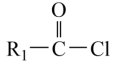

(1)下列说法正确的是____ 。
(2)I的结构简式是____ 。
(3)F→G的化学方程式为____ 。
(4)已知有机物L是H的同系物,且比H少1个C原子。写出同时符合下列条件的L所有同分异构体的结构简式____ 。
①属于芳香族化合物
②核磁共振氢谱显示4个吸收峰
③红外光谱谱图显示不含氢氧键、氧氧键、碳氮键
(5)根据题目所给信息,以A(丙烯)为原料,设计合成B(丙烯酸)的反应路线(用流程图表示,无机试剂任选):____ 。
CH2=CHCH3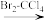 ____。
____。

已知:①R1CH2COOR2
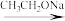
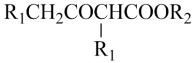
②
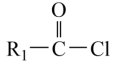


(1)下列说法正确的是
| A.1molG最多可以和3molH2发生加成反应 |
| B.化合物H既能和HCl溶液发生反应又能和NaOH溶液反应 |
| C.化合物J的分子式为C15H20N2 |
| D.K中有1个手性碳原子 |
(3)F→G的化学方程式为
(4)已知有机物L是H的同系物,且比H少1个C原子。写出同时符合下列条件的L所有同分异构体的结构简式
①属于芳香族化合物
②核磁共振氢谱显示4个吸收峰
③红外光谱谱图显示不含氢氧键、氧氧键、碳氮键
(5)根据题目所给信息,以A(丙烯)为原料,设计合成B(丙烯酸)的反应路线(用流程图表示,无机试剂任选):
CH2=CHCH3
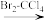 ____。
____。
您最近一年使用:0次
3 . 抗病毒药物瑞得西韦的结构如图,下列说法正确的是


| A.该物质含有碱基结构,属于核酸 |
| B.该物质结构中存在5个手性碳原子 |
| C.该物质在碱性条件下水解后的产物中含有丙氨酸 |
D.1mol该物质与足量盐酸反应,最多可消耗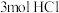 |
您最近一年使用:0次
4 . 下列说法不正确 的是
| A.淀粉和纤维素都属于高分子化合物,都能发生水解反应和酯化反应 |
| B.油脂在酸性条件下的水解可以得到高级脂肪酸盐,常用于生产肥皂 |
C.塑料中植入微量蛋白酶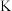 ,有助于塑料降解,高温、紫外线均能使该蛋白酶变性 ,有助于塑料降解,高温、紫外线均能使该蛋白酶变性 |
| D.甘氨酸既能与盐酸反应,又能与氢氧化钠溶液反应 |
您最近一年使用:0次
5 . 如图所示 研究中的常用分子。下列有关该化合物的说法正确的是
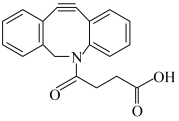
| A.不能发生加成反应 | B.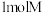 最多能与 最多能与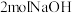 反应 反应 |
C.不能使酸性 溶液褪色 溶液褪色 | D.不能与氨基酸中的氨基反应 |
您最近一年使用:0次
2024-02-10更新
|
178次组卷
|
2卷引用:安徽师范大学附属中学2024届高三1月月考化学试卷
6 .  、氨基酸均既能与酸反应,又能与碱反应。(_____)
、氨基酸均既能与酸反应,又能与碱反应。(_____)
 、氨基酸均既能与酸反应,又能与碱反应。(_____)
、氨基酸均既能与酸反应,又能与碱反应。(_____)
您最近一年使用:0次
名校
解题方法
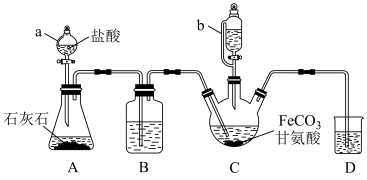
7 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如图所示(夹持和加热、搅拌仪器已省略)。
有关物质性质如下表:
实验过程:
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是_______ 。
(2)装置B中盛有的试剂是_______ ;实验过程中装置D的导管需要一直浸入液面下的必要性是_______ 。
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和_______ 。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)可以用_______ 试剂(写化学式)检验产品中是否含有Fe3+。
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是_______ 。

有关物质性质如下表:
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
| 两性化合物 | 强酸性、强还原性 |
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是
(2)装置B中盛有的试剂是
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为
(5)过程II中加入无水乙醇的目的是
(6)可以用
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是
您最近一年使用:0次
8 . 我们在进行体育锻炼、享受户外时光时,大脑会产生5-羟色胺,有益于防止焦虑、抑郁。5-羟色氨酸在一定条件下可生成5-羟色胺,下列说法错误的是
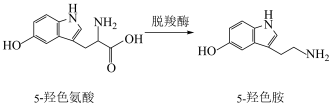
A.5-羟色胺分子式为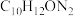 |
| B.5-羟色氨酸分子中含3种官能团 |
C.5-羟色胺既能与盐酸又能与 溶液反应 溶液反应 |
| D.5-羟色氨酸可以发生缩聚反应 |
您最近一年使用:0次
9 . 下列叙述不正确 的是
A.味精( )既有酸性又有碱性 )既有酸性又有碱性 |
| B.误食重金属盐中毒时,服用牛奶可减轻毒性 |
| C.低温下保存疫苗,可防止蛋白质变性 |
D.驱蚊酯( )属于高分子化合物 )属于高分子化合物 |
您最近一年使用:0次
10 . 甘氨酸亚铁是营养性饲料添加剂。实验室利用FeCO3与甘氨酸(H2NCH2COOH)制备甘氨酸亚铁[(H2NCH2COO)2Fe],实验装置如图所示(夹持和加热仪器已省略)
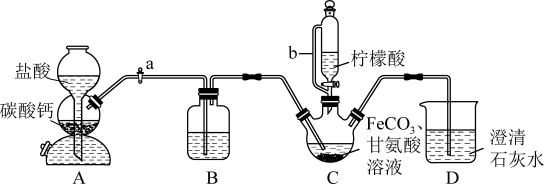
查阅资料:①甘氨酸易溶于水,微溶于乙醇。
②甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性。
实验过程:
I装置C中盛有17.4gFeCO3和200mL1.0mol·L-1甘氨酸溶液。实验时,先打开活塞a,待装置C中空气排尽后,再向三颈烧瓶中滴加柠檬酸溶液,加热。
II.经过一系列操作得到产品。
(1)A仪器是启普发生器,该仪器的特点是“随开随用、随关随停”,下列实验中可利用该仪器制备气体的是___________ (填序号)。
①二氧化锰与浓盐酸反应制备氯气
②锌粒与稀盐酸反应制备氢气
③亚硫酸钠固体与浓硫酸反应制备二氧化硫
④硫化亚铁固体与稀盐酸反应制备硫化氢
(2)过程1中,先打开活塞a,待___________ 时说明装置c中空气排尽,再向三颈烧瓶中滴加柠檬酸溶液,加热。仪器b的名称___________ 。
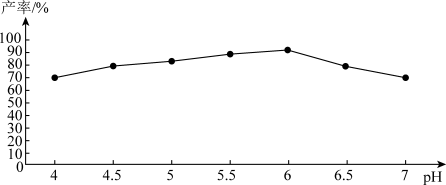
(3)过程I中,加入柠檬酸可促进FeCO3溶解并调节溶液pH,体系pH与甘氨酸亚铁产率的关系如图。由图象可知pH过低或过高均会导致产率下降,写出pH过低时有关的离子方程式___________ , 柠檬酸除了可以促进FeCO3溶解并调节溶液pH外,还可以___________ 。
(4)完成过程II的实验操作:反应结束后过滤,将滤液进行蒸发浓缩加入___________ 、过滤、洗涤、干燥。
(5)已知浓度为0.1mol·L-1的甘氨酸亚铁溶液的导电能力远小于0.1mol·L-1的FeSO4溶液的导电能力,其原因可能是___________ 。
(6)最终得到的产品质量为16. 32g,该实验产率为___________ 。

查阅资料:①甘氨酸易溶于水,微溶于乙醇。
②甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性。
实验过程:
I装置C中盛有17.4gFeCO3和200mL1.0mol·L-1甘氨酸溶液。实验时,先打开活塞a,待装置C中空气排尽后,再向三颈烧瓶中滴加柠檬酸溶液,加热。
II.经过一系列操作得到产品。
(1)A仪器是启普发生器,该仪器的特点是“随开随用、随关随停”,下列实验中可利用该仪器制备气体的是
①二氧化锰与浓盐酸反应制备氯气
②锌粒与稀盐酸反应制备氢气
③亚硫酸钠固体与浓硫酸反应制备二氧化硫
④硫化亚铁固体与稀盐酸反应制备硫化氢
(2)过程1中,先打开活塞a,待
(3)过程I中,加入柠檬酸可促进FeCO3溶解并调节溶液pH,体系pH与甘氨酸亚铁产率的关系如图。由图象可知pH过低或过高均会导致产率下降,写出pH过低时有关的离子方程式

(4)完成过程II的实验操作:反应结束后过滤,将滤液进行蒸发浓缩加入
(5)已知浓度为0.1mol·L-1的甘氨酸亚铁溶液的导电能力远小于0.1mol·L-1的FeSO4溶液的导电能力,其原因可能是
(6)最终得到的产品质量为16. 32g,该实验产率为
您最近一年使用:0次



